
охт (6sem) / методички митхт / GCT practicum 2013
.pdf111
Как видно из рис. 3.1.2, до температуры 600 – 650 ОС выход целевого продукта растет как за счёт увеличения степени превращения метанола, так и за счёт возрастания селективности образования формальдегида на метанол. Происходит это вследствие того, что скорость реакций образования формальдегида увеличивается с повышением температуры значительней, чем скорость побочных реакций вследствие действия катализатора. При
температуре |
600 – 700 |
ОС выход формальдегида |
||
достигает |
максимального |
значения. |
В |
этом |
температурном интервале |
серебряный |
катализатор |
||
избирательно ускоряет основные реакции. Причем в пределах температурного интервала работы катализатора с ростом температуры увеличивается доля формальдегида, образующегося по реакции дегидрирования (3.1.2). При дальнейшем повышении
температуры |
выход |
формальдегида |
уменьшается. |
Объясняется |
это |
тем, что значительная часть |
|
поступающего кислорода начинает расходоваться на глубокое окисление метилового спирта до оксида углерода(IV) по реакции (3.1.3), с возрастающей скоростью идет окисление и распад образовавшегося формальдегида по реакциям (3.1.4), (3.1.6).
Такое резкое снижение селективности процесса приводит к уменьшению выхода формальдегида. Следовательно, оптимальный температурный режим процесса – 600 - 700ОС.
Окислительное дегидрирование метанола в формальдегид в промышленности осуществляют в адиабатических реакторах, где совмещается экзотермическая реакция окисления метанола с эндотермической реакцией дегидрирования. В этом состоит одно из основных преимуществ рассматриваемого процесса.
Состав реакционной смеси. Превращение метанола в формальдегид проводят с использованием кислорода воздуха. При выборе соотношения между кислородом и метанолом учитывают, что часть
112
формальдегида образуется по реакции дегидрирования без затраты кислорода. Поэтому количество кислорода, рассчитанное по реакции окисления на поступающий в процесс метанол, оказывается избыточным, что приводит к образованию продуктов глубокого окисления и чрезмерному увеличению температуры в реакционной зоне. Максимальный выход формальдегида достигается при соотношении O2:CH3OH0,35:1. Следовательно, оптимальное соотношение
кислорода и метанола составляет 70% от стехиометрического, рассчитанного по реакции (3.1.1). Для поддержания устойчивого температурного режима разбавляют спирто-воздушную смесь парами воды. Рекомендуется вводить 20 - 25% воды от массы метанола. При таком соотношении содержание метанола в паро-воздушной смеси составляет 45% объем., что находится за верхним пределом взрываемости метанола в воздухе (34,7% объем.). При оптимальном соотношении кислорода и метанола (70% от стехиометрического) основное количество формальдегида образуется по реакции окисления, поэтому с некоторой долей приближения синтез формальдегида можно отнести к необратимым процессам.
Время контактирования. Зависимость выхода формальдегида от времени контактирования представляет собой кривую с максимумом, что характерно для сложных процессов с последовательными побочными реакциями. Оптимальное время контактирования - 0,01 - 0,03 сек. При уменьшении времени контактирования ниже 0,01 сек падает степень превращения метанола, т.е. наблюдается его «проскок» через слой катализатора. При времени контакта, превышающем оптимальное, заметную роль начинают играть последовательные побочные реакции, главным образом распад формальдегида на оксид углерода(II) и водород по реакции (3.1.6). Для сохранения получившегося формальдегида проводят «закалку» образовавшейся
113
парогазовой смеси, т.е. резко снижают ее температуру с 600 - 700ОС до 100 ОС. Быстрое
снижение |
температуры |
предотвращает |
распад |
|
формальдегида. |
«Закалка» |
продуктов |
реакции |
|
является |
эффективным |
способом |
повышения |
|
селективности |
процесса в |
тех случаях, когда |
||
процесс идет при высокой температуре и целевой
продукт склонен к вторичным превращениям. |
|
|||
В |
выбранных |
условиях |
процесс |
синтеза |
формальдегида можно классифицировать как сложный, необратимый, гетерогенный, каталитический процесс, идущий во внешнедиффузионной области. Выход формальдегида в оптимальных условиях достигает 70 - 80% при селективности 85 - 90%. Средний состав газообразных продуктов реакции после
охлаждения |
и |
поглощения |
формальдегида |
||||
(в % объем.): 75 N2, 10 - 20 H2, 3 - 5 CO2, 0,5 - |
|||||||
1,5 CO и до 0,4 O2. |
|
|
|
|
|
||
3.1.5. Описание лабораторной установки. |
|
||||||
Лабораторная |
установка |
состоит |
из |
трех |
|||
основных |
элементов: |
испарителя-смесителя |
1, |
||||
контактного |
аппарата |
2 |
и |
«закалочного» |
|||
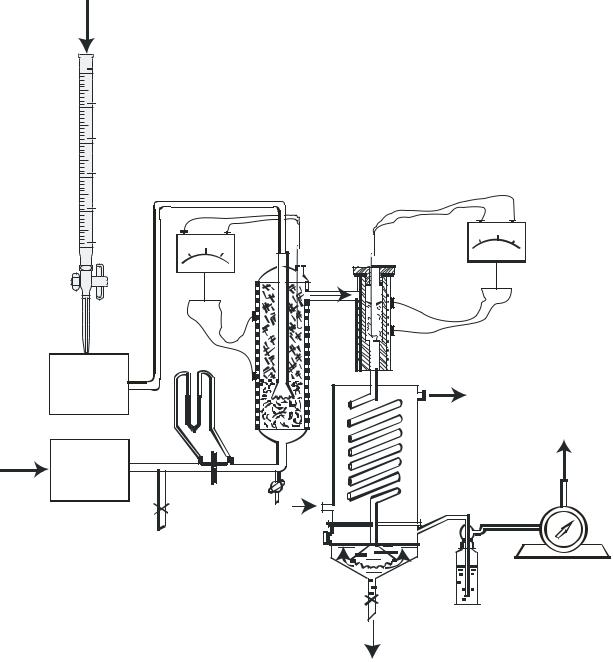
холодильника-поглотителя 3 (рис. 3.1.3). Воздух, подаваемый компрессором 11, поступает через диафрагму 5, перепад давления на которой измеряют с помощью дифференциального манометра 10, в нижнюю часть испарителя-смесителя 1. Сверху в него из бюретки 12 дозирующим насосом 9 подают метанол. Спирт по внутренней трубке попадает в нижнюю часть испарителя, испаряется на нагретой металлической стружке и, смешавшись с воздухом, проходит насадку из минеральной ваты для улавливания капель неиспарившегося спирта. Испаритель имеет внешний электрообогрев, интенсивность нагрева регулируют с помощью терморегулятора 6. Нагретая спиртовоздушная смесь поступает в контактный аппарат 2.
114
метиловый
спирт
12
|
|
6 |
7 |
|
|
|
|
|
|
|
2 |
|
10 |
1 |
|
|
|
|
|
9 |
|
|
|
|
|
|
сброс |
|
5 |
|
3 |
воздух |
|
|
|
|
|
|
|
11 |
А |
2 |
8 |
|
|
H O |
|
|
|
|
4 |
|
|
конденсат |
|
Рис. |
|
3.1.3 |
Схема лабораторной |
установки для |
|||
получения |
формальдегида: |
1 |
- |
испаритель; |
|||
2 |
- |
контактный аппарат; 3 - холодильник-поглотитель; |
|||||
4 |
|
- |
дрексель-поглотитель; |
5 |
- |
диафрагма; |
|
6, |
|
7 |
- |
терморегуляторы; |
8 |
– |
газосчетчик; |
9 |
- |
|
дозирующий насос; 10 |
– |
дифференциальный |
||
манометр; 11 - компрессор; 12 - бюретка .
115
Внутри аппарата на сетке помещен катализатор -
серебро, нанесенное на пемзу. |
|
|
|
Контактный |
аппарат |
изготовлен |
из |
хромоникелевой стали или кварца и снабжен внешним
электрообогревом |
для предварительного |
подогрева |
|||
катализатора. |
|
Интенсивность |
нагрева |
реактора |
|
регулируют |
с |
помощью |
терморегулятора |
7. |
|
Температуру реакционной зоны измеряют термопарой. Продукты контактирования из контактного аппарата поступают в закалочный холодильник-поглотитель 3.
Парогазовая |
смесь |
проходит |
по |
змеевику, |
||
охлаждаемому |
водой, |
в |
нижнюю |
|
часть, |
где |
барботирует |
через слой |
дистиллированной воды. В |
||||
воде растворяются формальдегид, непрореагировавший метанол, муравьиная кислота. Для более полного поглощения метанола и формальдегида парогазовую
смесь пропускают |
через слой воды в склянке |
||
Дрекселя |
4. |
Несконденсировавшиеся |
и |
нерастворившиеся газы проходят газосчетчик 8, с помощью которого измеряют их расход и объем, и поступают в линию сброса в вытяжной шкаф.
3.1.6. |
Предварительные расчеты. |
|
|
||
Рассчитывают |
расход |
воздуха |
в |
л/ч |
при |
температуре и давлении в лаборатории по заданному расходу водного метанола и заданному проценту от стехиометрического количества кислорода. Расчет ведут по реакции (3.1.1), т.е. считают, что по стехиометрии на 1 моль поступающего в контактный аппарат метанола приходится 0,5 моля кислорода (11,2 л кислорода или 53,3 л воздуха при нормальных условиях).
3.1.7.Порядок проведения опыта.
Водный раствор метанола в количестве 100 мл заливают в бюретку 12. В нижнюю часть поглотителя 3 и в склянку Дрекселя 4 наливают по 100 мл дистиллированной воды. Включают подачу охлаждающей воды в холодильный аппарат 3.
116
Включают электрообогрев испарителя 1 и контактного аппарата 2. С помощью терморегуляторов 6 и 7 поддерживают следующие температуры:
а) |
в испарителе 100 10ОС; |
|
|
|
б) |
в контактном аппарате |
в |
момент |
начала |
подачи спирта 250 10ОС, |
а |
в течение |
опыта |
|
500 - 700ОС. |
|
|
|
|
При открытом зажиме А включают компрессор 11. Количество подаваемого воздуха регулируют тем же зажимом А, а контролируют с помощью дифференциального манометра 10 и газосчетчика 8. Для измерения расхода воздуха необходимо сделать несколько замеров объема воздуха, поступающего в установку в течение 1 мин. С помощью зажима А установить расчетный расход воздуха.
По достижении необходимых температур в испарителе и контактном аппарате и установления необходимого расхода воздуха начинают подавать спирт. Расход спирта контролируют по изменению объема спирта в бюретке за определенные интервалы времени (5 мин). Момент начала подачи спирта в испаритель (после заполнения шланга, идущего от насоса 9) фиксируют как время начала опыта. Продолжительность опыта 40 – 60 мин. (задается преподавателем). Во время проведения опыта непрерывно следят за ходом процесса. С момента начала опыта через каждые 5 мин записывают в таблицу: скорости подачи спирта (изменение объема спирта в бюретке 12) и воздуха (по дифференциальному манометру 10), значения температуры в испарителе и контактном аппарате (высвечиваются на шкалах терморегуляторов 6 и 7, соответственно), скорость выделения контактного газа (показания газосчетчика 8) (см. Табл. 3.1.1).
Скорости подачи воздуха и спирта в ходе опыта должны оставаться постоянными и соответствовать расчетным значениям. Скорость выделения контактного газа не должна отличаться от скорости подачи воздуха более чем на 10 – 15 % (почему?).
117
Обо всех отклонениях от режима необходимо как можно быстрее сообщить преподавателю.
В ходе опыта с помощью лаборанта или преподавателя необходимо провести хроматографический анализ состава контактного газа
(см. ниже).
По истечении времени опыта фиксируют конечные показания приборов и уровень спирта в бюретке(см.
выше), |
прекращают подачу спирта (выключают насос |
9) и |
через 5 минут перестают подавать воздух |
(выключают компрессор 11). Эти «лишние» пять минут подачи воздуха необходимы для продувки системы от паров формальдегида, метанола и реакционных газов. Выключают нагрев испарителя и контактного аппарата и ждут 15 - 20 мин для охлаждения
контактного аппарата до 100 - 150 С.
Формалин из поглотителя 3 сливают в мерную колбу на 250 мл. Слабым раствором формалина, образовавшимся в склянке Дрекселя, промывают поглотитель 3. Промывные воды сливают в ту же колбу, доводят до метки дистиллированной водой, тщательно перемешивают и определяют количество полученного формальдегида титрованием в присутствие солянокислого гидроксиламина (методику см. ниже).
Исходные и экспериментальные данные
Дата __.______.____г.
Концентрация водного раствора метанола Плотность водного раствора
метанола при 20 ОС Расход метанола
Поданное в испаритель количество водного раствора метанола Поданный за время опыта объем воздуха
Объем контактного газа, полученный за время опыта
Заданное соотношение между О2 и СН3ОН
118 |
|
|
Полученное соотношение между О2 и СН3ОН |
_____ |
|
Температура в лаборатории |
|
_____ОС |
Атмосферное давление |
_____мм.рт.ст.(_____Мпа) |
|
Объем катализатора |
|
_____мл |
Доля свободного объема |
|
_____ |
Технологические параметры и критерии процесса |
||
Время контактирования |
|
_____сек |
Конверсия метанола |
|
_____% |
Выход формальдегида на метанол |
_____% |
|
Селективность образования |
|
|
формальдегида на метанол |
|
_____% |
Интенсивность работы катализатора |
_____кг/мЗ ч |
|
Таблица 3.1.1
Экспериментальные данные.
Вре- |
Подача спирта |
|
Расход |
Температура, |
Расход контактного |
|||||
мя от |
|
|
|
воздуха |
|
оС |
|
газа |
|
|
нача- |
Уровень |
Разность |
Рас- |
Ндм, |
л/ч |
В |
В реак- |
Показ. |
Раз- |
л/ч |
ла, |
спирта в |
уровней, |
ход, |
мм |
|
испа- |
торе |
газо- |
ность, |
|
мин |
бюретке, |
мл |
мл/ч |
|
|
рите- |
|
счетч. |
л |
|
|
мл |
|
|
|
|
ле |
|
л |
|
|
|
|
|
|
|
|
|
|
|
|
|
0 |
|
|
|
|
|
|
|
|
|
|
5 |
|
|
|
|
|
|
|
|
|
|
10 |
|
|
|
|
|
|
|
|
|
|
15 |
|
|
|
|
|
|
|
|
|
|
20 |
|
|
|
|
|
|
|
|
|
|
30 |
|
|
|
|
|
|
|
|
|
|
40 |
|
|
|
|
|
|
|
|
|
|
50 |
|
|
|
|
|
|
|
|
|
|
60 |
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
Vвозд при н.у. = _____л
Vгаза при н.у. = _____л

119
3.1.8.Контроль процесса.
Определение содержания формальдегида в формалине. К 5 мл анализируемого раствора, помещенным в колбу для титрования, добавляют 10 мл 10%-ного раствора солянокислого гидроксиламина и 3 – 4 капли индикатора - бромфенолсинего. Реакция протекает по уравнению
NH2OH ∙ HCl + CH2O CH2NOH + H2O + HСl
По истечении не менее 5 мин образовавшуюся в результате реакции соляную кислоту титруют 0,5 н раствором едкого натра в присутствии индикатора бромфенолсинего до светло-сиреневого окрашивания. Предварительно необходимо провести холостое титрование 5 мл дистиллированной воды по той же методике для определения кислотности раствора гидроксиламина.
Количество формальдегида, полученного за время опыта, в граммах рассчитывают по формуле:
G
( a a' ) N 30 ,0 V
b 1000
где а - объем раствора NaOH, израсходованного на титрование раствора формальдегида, мл;
a'– объем раствора щелочи, пошедший на титрование холостой пробы;
N - нормальность раствора щелочи;
b - объем раствора, взятого на анализ, 5 мл;
V - общий объем раствора в мерной колбе, 250 мл; 30,0 - масса эквивалента формальдегида, г.
Хроматографический анализ состава контактного газа и обработка хроматограммы. Определение состава контактного газа проводят методом газоадсорбционной хроматографии. Для разделения
|
|
120 |
|
|
газа |
используют |
насадочную |
колонку |
с |
активированным углем СКТ (фракция 0,25 – 0,5 мм) диаметром 3 мм и длиной 3 м. Температура разделения 80 оС. В качестве детектора применяют катарометр – детектор по теплопроводности. Устройство и принцип действия катарометра см. в 4- ом разделе, посвященном хроматографии. Пробу контактного газа (примерно 1 мл) отбирают стеклянным шприцем из вакуумного шланга после склянки Дрекселя 4 в стационарном режиме процесса, вводят в испаритель хроматографа и отмечают время отбора и номер пробы. Реакционные газы, двигаясь в колонке в токе газа-носителя (аргона), разделяются из-за разной интенсивности взаимодействия с активированным углем и поступают в детектор в следующем порядке:
водород, кислород + азот, оксид углерода (II),
оксид |
углерода |
(IV). |
Из-за |
изменения |
|
теплопроводности |
газа |
при |
изменении |
состава |
|
газовой смеси, поступающей в детектор, появление каждого из перечисленных веществ в детекторе приводит к появлению сигнала и отклонению пера самописца. На хроматограмме появляется «пик», высота (или площадь) которого пропорциональна содержанию данного вещества в смеси. Поскольку разные вещества по-разному влияют на теплопроводность газовой смеси и, следовательно, на величину отклонения пера самописца, для количественного анализа необходима калибровка по высоте или по площади «пиков» с использованием искусственных смесей анализируемых веществ известного состава. В данной работе проведена калибровка по высоте «пиков» и определены калибровочные коэффициенты, отражающие относительную чувствительность катарометра к анализируемым веществам.
При проведении хроматографического анализа необходимо правильно подобрать шкалу чувствительности (масштаб) для регистрации «пика»
