
- •Тема 16. Котельные установки……………..………………………………149
- •Тема 17. Использование вэр и охрана окружающей среды………..…..170
- •Введение
- •Часть 1. Термодинамика
- •Тема 1. Основные понятия и определения
- •Предмет и метод термодинамики
- •Объект изучения термодинамики
- •1.3 Параметры состояния термодинамической системы
- •1.4 Уравнение состояния идеального газа. Понятие об идеальных и реальных газах
- •1.5 Газовые смеси
- •1.6 Термодинамический процесс
- •Тема 2. Первый закон термодинамики
- •2.1 Аналитическое выражение первого закона термодинамики. Частные случаи закона
- •2.2 Внутренняя энергия системы
- •2.3 Работа расширения и pv-диаграмма для изображения работы
- •2.4 Работа и теплота
- •2.5 Теплоемкость газов
- •2.6 Энтальпия
- •Тема3. Второй закон термодинамики
- •3.1 Общая характеристика
- •3.2 Энтропия и математическое выражение второго закона
- •3.3 III начало термодинамики
- •3.4 Т,s диаграмма для изображения теплоты
- •3.5 Физический смысл энтропии
- •3.6 Основное уравнение термодинамики и вычисление энтропии
- •Тема. 4 термодинамические процессы идеальных газов в закрытых системах
- •4.1 Изохорный процесс
- •4.2 Изобарный процесс
- •4.3 Изотермический процесс
- •4.4 Адиабатный процесс
- •4.5 Политропный процесс
- •Тема 5. Термодинамические циклы
- •5.1 Круговые процессы
- •5.2 Термодинамическая схема теплового двигателя
- •5.3 Прямой цикл Карно
- •5.4 Обратный цикл Карно
- •Тема 6. Циклы паросиловых, холодильных установок и теплового насоса
- •6.1 Циклы паросиловых установок. Цикл Ренкина
- •6.2 Циклы холодильных установок
- •6.3 Цикл теплового насоса
- •6.4 Эксергия. Эксергический анализ
- •Тема7. Теоретические циклы двигателей внутреннего сгорания
- •7.1 Цикл Отто
- •7.2 Цикл Дизеля
- •7.3 Цикл Тринклера (или Сабатэ)
- •Тема8. Термодинамика потока газов и паров
- •8.1 Уравнение первого закона термодинамики для потока
- •8.2 Истечение газов и паров
- •8.3 Дросселирование. Температура инверсии
- •Часть 2. Теория тепло и массообмена
- •Тема 9. Основы теории теплообмена
- •9.1 Введение. Теплопроводность
- •9.2 Закон Фурье – основной закон теплопроводности
- •9.3 Теплопроводнсть плоской однородной, однослойной стенки
- •9.4 Теплопроводность многослойной стенки
- •9.5 Теплопроводность цилиндрической стенки.
- •Тема10. Конвективный теплообмен
- •10.1 Понятие теплообмена. Закон Ньютона Рихмана
- •10.2 Критерии подобия
- •10.3 Теплоотдача при вынужденном движении теплоносителя
- •10.4 Теплоотдача при свободном движении теплоносителя
- •10.5. Теплоотдача при кипении
- •10.6 Теплоотдача при конденсации пара
- •Тема11. Теплопередача чарез стенку
- •11.1 Понятие теплопередачи, теплопередача через плоскую стенку.
- •11.2 Уравнение теплопередачи.
- •11.3 Теплопередача через цилиндрическую стенку
- •Тема12. Лучистый теплообмен
- •12.1 Понятие лучистого теплообмена
- •12.2 Законы лучистого теплообмена
- •12.3 Теплообмен излучением системы тел в прозрачной среде
- •Тема13. Водяной пар
- •13.1 Процесс парообразования в pv-координатах
- •13.2 Ts и hS диаграмма водяного пара
- •13.3 Параметры состояния жидкости и пара
- •Тема14. Влажный воздух
- •14.1 Понятие влажного воздуха, его характеристики
- •14.3 Сушка материала
- •Тема15. Топливо
- •15.1 Классификация топлива
- •15.2 Состав топлива
- •15.3 Характеристики топлива.
- •15.4. Примеры твердого, жидкого, газообразного топлива.
- •15.5 Процесс горения топлива
- •15.6 Состав и объем продуктов сгорания.
- •15.7 Нефтяные топлива.
- •15.8 Понятие детонации, октанового числа и цетанового числа.
- •Тема16. Котеьные установки
- •16.1 Понятие котла и котельной установки
- •16.1 Паровой котёл и его основные элементы
- •16.3 Паровые и водогрейные котлы
- •16.4 Вспомогательное оборудование
- •16.5 Топка, топочные устройства
- •16.6 Котлы утилизаторы
- •16.7 Тепловой баланс горения
- •Тема17. Использование вэр и охрана окружающей среды
- •17.1 Понятия вэр
- •17.2 Классификация вторичных энергетических ресурсов в промышленности
- •17.3 Использование вторичных энергетических ресурсов промышленности
- •17.4 Расчет вэр на экономическую эффективность
- •Заключение.
2.6 Энтальпия
В термодинамике важную роль играет сумма внутренней энергии системы U и произведения давления системы р на ее объем V, называемая энтальпией и обозначаемая Н:
H = U + pV. (2.32)
Так как входящие в нее величины являются функциями состояния, то и сама энтальпия является функцией состояния. Так же как внутренняя анергия, работа и теплота, она измеряется в джоулях (Дж).
Энтальпия обладает свойством аддитивности. Величина
h = u + pv, (2.33)
называемая удельной энтальпией (h = H/M), представляет собой энтальпию системы, содержащей 1 кг вещества, и измеряется в Дж/кг.
Поскольку энтальпия есть функция состояния, то она может быть представлена в виде функции двух любых параметров состояния:
h = ψ1 (p,v); h = ψ2(v,T); h = ψ3(p,T),
а величина dh является полным дифференциалом.
Изменение энтальпии в любом процессе определяется только начальным и конечным состояниями тела и не зависит от характера процесса.
Физический смысл энтальпии выясним на следующем примере. Рассмотрим расширенную систему, включающую газ в цилиндре и поршень с грузом общим весом G (рисунок 2.3). Энергия этой системы складывается из внутренней энергии газа и потенциальной энергии поршня с грузом в поле внешних сил: E = U + Gy. В условиях равновесия (G = pF) эту функцию можно выразить через параметры газа: E = U + pFy = U + pV. Получаем, что E = H, т.е. энтальпию можно трактовать как энергию расширенной системы.
Уравнение δq = du + pdv в случае, когда единственным видом работы является работа расширения, с учетом очевидного соотношения
pdv = d(pv) – vdp может быть записано в виде δq = d (u + pv) – vdp, или
δq = dh – vdp. (2.34)
Из этого соотношения следует, что если давление системы сохраняется неизменным, т. е. осуществляется изобарный процесс (dp = 0), то
δqp = dh (2.35)
и
qp = h2 – h1 (2.36)
т. е. теплота, подведенная к системе при постоянном давлении, идет только на изменение энтальпии данной системы.
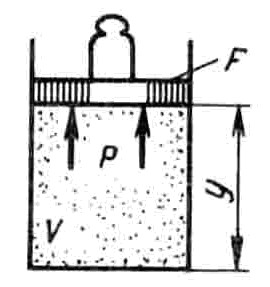
Рис. 2.3 – К определению физического смысла энтальпии
Это выражение очень часто используется в расчетах, так как огромное количество процессов подвода теплоты в теплоэнергетике (в паровых котлах, камерах сгорания газовых турбин и реактивных двигателей, теплообменных аппаратах), а также целый ряд процессов химической технологии и многих других осуществляется при постоянном давлении. Кстати, по этой причине в таблицах термодинамических свойств обычно приводятся значения энтальпии, а не внутренней энергии.
Для идеального газа получим
dh = du + d(pv) = cvdT + RdT = (cv + R)dT = cpdT. (2.37)
Так как между энтальпией и внутренней энергией существует связь (2.33), выбор начала отсчета одной из них не произволен: в точке, принятой за начало отсчета внутренней энергии, h = pv. Например, для воды при t = 0,01 °С и р = 610,8 Па, u = 0, a h = pv = 610,8 · 0.001 = 0,611 Дж/кг.
При расчетах практический интерес представляет изменение энтальпии в конечном процессе:
![]() . (2.38)
. (2.38)
Тема3. Второй закон термодинамики
3.1 Общая характеристика
Формулировки второго закона. Второй закон термодинамики, Как и первый, является опытным законом, основывающимся на многовековых наблюдениях ученых. Однако установлен он был только в середине XIX века.
Для превращения тепла в работу необходимо иметь два источника тепла разной температуры (С.Карно, 1824 г.).
Теплота может переходить сама собой только от горячего тела к холодному; для обратного перехода надо затратить работу (Р. Клазиус, 1850г.).
Невозможно превратить в периодически действующем двигателе в работу теплоту какого–либо тела, не производя никакого другого действия, кроме охлаждения тела (В.Томсон, 1851 г.).
Все естественные процессы являются переходом от менее вероятных к более вероятным состояниям (Л.Больцман, 1870–1876 г.).
Формулировка Больцмана самая широкая и содержательная, с помощью её, путем логических рассуждений, можно получить все остальные.
