
- •Биохимия печени
- •Гомеостатическая функция печени
- •Пигментный обмен
- •Желтухи
- •IV. Обезвреживающая функция печени
- •Микросомальный метаболизм ксенобиотиков.
- •Внемикросомальный метаболизм ксенобиотиков
- •Функциональные пробы печени
- •Исследование обезвреживающей функции печени:
- •Ферментодиагностика
- •2. Индикаторные (клеточные) ферменты.
- •3. Экскреторные ферменты
- •Метаболизм этанола в печени.
- •Токсичность ацетальдегида
- •Литература
ГБОУ ВПО «Ростовский государственный
медицинский университет» министерства здравоохранения и
социального развития Российской Федерации
Кафедра общей и клинической биохимии №1
Биохимия печени
учебно-методическое пособие
для студентов медицинских вузов
Ростов-на-Дону
2012
УДК: 612.035(075.8)
Утверждено на заседании Центральной методической комиссии РостГМУ ____февраля 2012 г., протокол №__.
Биохимия печени. Учебно-методическое пособие для студентов медицинских вузов. – Ростов-на-Дону, Ростовский ГМУ. – 2012. – 37 с.
Составлено на кафедре общей и клинической биохимии №1 с курсом общей и биоорганической химии профессором Микашинович З.И., доцентом Саркисяном О.Г., ассистентом Коваленко Т.Д.
Под редакцией профессора Микашинович З.И.
Рецензенты:
профессор по кафедре нормальной физиологии, ГБОУ ВПО РостГМУ Минздравсоцразвития РФ, д.м.н., Гафиятуллина Г.Ш.
руководитель биохимической лаборатории ФГУ «Ростовский научно-
исследовательский онкологический институт» Минздравсоцразвития России, д.б.н., профессор Горошинская И.А.
© ГОУ ВПО «Ростовский государственный медицинский университет» Минздравсоцразвития России.
© Коллектив авторов.
Гомеостатическая функция печени
Печень занимает центральное место в обмене веществ организма. Это центральная лаборатория организма.
Печень выполняет следующие биохимические функции:
регуляторно-гомеостатическую.
мочевинообразовательную.
жёлчеобразовательную и экскреторную.
обезвреживающую.
РЕГУЛЯТОРНО-ГОМЕОСТАТИЧЕСКАЯ ФУНКЦИЯ.
Регуляция углеводного обмена.
Печень поглощает из воротной вены, главным образом, глюкозу, галактозу и фруктозу. В печени протекают следующие процессы обмена углеводов: биосинтез и распад гликогена, глюконеогенез, гликолиз, пентозофосфатный путь; активно осуществляется обмен фруктозы и галактозы, биосинтез гетерополисахаридов. Глюкоза проникает в гепатоциты по градиенту концентрации.
Активность регулирующих ферментов гликолиза и гликогенолиза повышается под влиянием инсулина (за счёт увеличения их синтеза). Однако печень по шкале инсулинзависимости занимает промежуточное положение. Тиреоидные гормоны также активируют синтез этих ферментов.
Печень является одним из органов, который поддерживает постоянный уровень глюкозы в крови.
Глюкоза, производимая печенью в ходе гликогенолиза и глюконеогенеза, поступает в кровь и расходуется всеми клетками организма, а при избыточном её поступлении из кишечника депонируется в виде гликогена.
Фруктоза, поступающая в печень, может фосфорилироваться в положении 6 во фруктозо-6-фосфат гексокиназой. Однако в печени существуют и другие метаболические пути.
3-ФГА и ДГАФ могут использоваться в глюконеогенезе, а могут включаться в гликолиз с образованием ПВК.
На активность фруктокиназы не влияет ни инсулин, ни голодание, в отличие от глюко- и гексокиназы. Поэтому у больных сахарным диабетом фруктоза поглощается с нормальной скоростью и рекомендуется в пищу вместо глюкозы. Отсутствие в печени фруктокиназы приводит к идиопатической фруктозурии (накопление фруктозы).
Если отсутствует фруктозо-1-фосфатальдолаза, то развивается наследственная непереносимость к фруктозе (накапливается фруктозо-1-фосфат, а он ингибирует фосфорилазу печени, в результате не расщепляется гликоген до глюкозы). Т.о. возникает гипогликемия.
Ф руктоза
руктоза

 Гексокиназа
Гексокиназа
 АТФ
сорбитол ДГ
АТФ
сорбитол ДГ
ф
 р-6-фосфат
АТФ
р-6-фосфат
АТФ
 АДФ
АДФ НАДФ+
АДФ
АДФ НАДФ+
 фруктокиназа
НАДФН+Н+
сорбитол ФФК-1 АТФ
(ключевой фермент)
фруктокиназа
НАДФН+Н+
сорбитол ФФК-1 АТФ
(ключевой фермент)
АДФ
 Фруктозо-1-фосфат
Фруктозо-1-фосфат
 Фр-1-6-дифосфат
фруктозо-1-фосфатальдолаза
Фр-1-6-дифосфат
фруктозо-1-фосфатальдолаза
 (органоспецифический фермент)
(органоспецифический фермент)
ДГАФ
 глицеральдегид
глицеральдегид
ф р-дифосфатальдолаза
триокиназа
р-дифосфатальдолаза
триокиназа
 АТФ
изомераза
АТФ
изомераза
АДФ
3-фосфоглицериновый альдегид
ПВК
Рис. 1. Метаболизм фруктозы в организме
В метаболизме фруктозы принимает участие фермент сорбитол ДГ, который специфичен только для клеток печени.
Схема реакции:
Сорбитол ДГ
с
 орбитол
фруктоза
орбитол
фруктоза
НАДФН2
НАДФ+
В клетках артериальных стенок, клетках Шванна, эритроцитах, хрусталика и сетчатки глаза, а также семенниках имеется фермент альдозоредуктаза (НАДФН-зависимый). Он превращает глюкозу в сорбитол.
Схема реакции:
НАДФН+Н+ НАДФ+
г люкоза
сорбитол
люкоза
сорбитол
альдозоредуктаза
Скорость диффузии сорбитола из клеток невелика.
Клинический аспект:
У больных сахарным диабетом сорбитол накапливается в сетчатке и хрусталике глаза, клетках клубочков почек, в шванновских клетках, в эндотелии. Сорбитол в высоких концентрациях токсичен для клеток. Его накопление в нейронах приводит к увеличению осмотического давления, набуханию клеток и отёку тканей. Помутнение хрусталика может развиваться в результате вызванного накоплением сорбитола набухания хрусталика и нарушения упорядоченной структуры кристаллинов. А клетки печени активно превращают сорбитол во фруктозу.
Метаболизм галактозы.
Галактоза
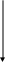
 АТФ
АТФ
1 галактокиназа
АДФ
 Галактозо-1-фосфат
Галактозо-1-фосфат
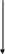
 УДФ-глюкоза
УДФ-глюкоза
2 Галактозо-1-фосфат-уридилтрансфераза
 УДФ-галактоза
УДФ-галактоза
 Гл-1-фосфат
Гл-1-фосфат
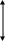 3
эпимераза
3
эпимераза
фосфоглюкомутаза
синтез гликогена

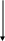 Гл-6-фосфат
Гл-6-фосфат
УДФ-глюкоза
 Гл-6-фосфатаза
Гл-6-фосфатаза
ГЛЮКОЗА гликолиз идёт на синтез гликогена
Рис. 2. Метаболизм галактозы
Галактоза образуется в кишечнике в результате гидролиза лактозы и, попав в печень, включается в следующий метаболический путь.
Обратимость эпимеразной реакции (3) важна для синтеза галактозильных остатков в гликолипидах и гликопротеинах. Кроме того, галактоза необходима для синтеза лактозы в молочных железах. В период лактации галактоза не является незаменимым компонентом пищи, т.к. может синтезироваться из глюкозы. Наследственный дефект любого из трёх ферментов приводит к галактоземии.
В печени активно образуется глюкуроновая кислота. Она участвует в детоксикационной функции печени. Глюкуроновая кислота с ксенобиотиками и с токсическими веществами образует глюкурониды. Образование глюкуроновой кислоты идёт из глюкозы:
Фосфоглюко- уридил-
Киназа изомераза трансфераза
г

 люкоза
гл-6-фосфат
гл-1-фосфат
люкоза
гл-6-фосфат
гл-1-фосфат
АТФ АДФ УТФ 2Фн
УДФ-ДГ
У




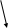 ДФ-глюкоза
УДФ-глюку- глюкуронат-1-
глюкуро-
ДФ-глюкоза
УДФ-глюку- глюкуронат-1-
глюкуро-
роновая фосфат новая
кислота кислота
2НАД+ 2НАДН+Н+ Н2О УМФ Фн
Н2О
Рис. 3. Схема синтеза глюкуроновой кислоты
Помимо этого, глюкуроновая кислота входит в состав гиалуроновой кислоты, хондроитинсульфата и гепарина.
Регуляция липидного обмена.
Для клеток печени характерны следующие процессы обмена липидов: синтез ВЖК, ТАГ, ФЛ, ХС и его эфиров, а также липолиз ТАГ, окисление ВЖК. В печени образуются кетоновые тела, которые используются как источник энергии для других тканей (сердце, мышцы, корковый слой почек и головной мозг, только при голодании). Сама печень кетоновые тела как энергосубстрат не использует.
В печени образуется холестерина больше, чем поступает с пищей: с пищей потребляется 0,3-0,5 г. ХС ежесуточно, а в печени образуется в сутки до 2-4 гр. ХС.
Небольшая часть свободного ХС и его эфиров поступает в кровь. В норме отношение содержания эфиров ХС и свободного ХС равно 0,5 – 0,7. При паренхиматозных поражениях печени синтетическая активность её клеток ослаблена, в связи с чем концентрация ХС и ЭХС в плазме крови снижается. В этом случае коэффициент ЭХС/своб. ХС понижается до 0,3 – 0,4, причём прогрессирующее его снижение является неблагоприятным прогностическим признаком.
Печень является органом, который обеспечивает гомеостаз ХС:
1) в печени локализуется ферментативная система, синтезирующая ХС;
2) в печени формируются ЛПОНП, в составе которых имеется ХС;
3) наряду с этим, формируется поток ЛПВП и синтезируется α и β ЛХАТ, которая катализирует реакцию этерификации ХС в крови на поверхности ЛПВП с ФЛ, входящими в их состав, с образованием эфиров ХС;
4) в мембранах эпителиальных клеток печени встроены различные рецепторы, обеспечивающие улавливание из кровотока ХС в составе “ремнантных” ХМ, ЛПОНП, ЛППП, ЛПНП, ЛПВП и модифицированных ЛП.
80% ХС в печени окисляется в жёлчные кислоты. ХС, трансформированный в жёлчные кислоты, и свободный ХС секретируется в жёлчь и включается в цикл энтерогепатической циркуляции. Ежесуточно из организма удаляется 1 гр. ХС.
В норме содержание ХС в сыворотке крови 3,9 – 6,5 мМоль/л, из них 70% ЭХС, 30% ХС.
Повышение концентрации ХС в крови происходит при заболеваниях печени, сопровождающихся внутри и внепеченочным холестазом, а также при различных поражениях паренхимы печени.
При условии перенасыщенности жёлчи ХС образуется аномальная жёлчь. Избыток ХС выпадает в виде кристалла.
Перенасыщение жёлчи ХС возможно и при условии ↑ синтеза ХС и при ↓ процесса образования солей желчных кислот.
Клинический аспект: хенодезоксихолевая кислота является ингибитором ГМГ-КоА-редуктазы (регуляторный фермент синтеза ХС). Это позволяет использовать эту кислоту в качестве лекарственного препарата при желчнокаменной болезни.
В клинической биохимии имеется понятие литогенность. Литогенность – это отношение фактической концентрации ХС к максимально возможной концентрации.
1) если это отношение меньше 1, то жёлчь представляет собой устойчивую мицеллярную форму.
2) если = 1 – жёлчь насыщена и представлена в виде жидкокристаллической мицеллярной формы.
3) если больше 1 – это перенасыщенная мицеллярная неустойчивая форма.
Ферментативные реакции синтеза ТАГ в печени и жировой ткани сходны.
В печени синтезируются транспортные формы липидов (насцентные хиломикроны, ЛПОНП, ЛВП), а также происходит распад ремнантных ХМ, ЛПОНП, ЛВП.
Печень участвует в поддержании постоянного уровня жирных кислот в крови, если их количество увеличивается, то печень поглощает их и превращает в ТАГ, ФЛ, ЭХС, которые входят в состав ЛПОНП.
Уменьшение образования ЛПОНП, уменьшение биосинтеза ФЛ приводит к увеличению биосинтеза ТАГ и накоплению их в гепатоцитах, что сопровождается жировой дегенерацией печени.
Только в печени происходит синтез жёлчных кислот из ХС, которые затем секретируются в состав жёлчи.
Жёлчегенез – главный путь избавления организма от избытка ХС.
Регуляция обмена белков и аминокислот:
Печень играет центральную роль в обмене белков, выполняя следующие функции:
1) синтез специфических белков плазмы
Все альбумины плазмы, 75 – 90% - α-глобулинов и 50% β-глобулинов синтезируются гепатоцитами. За сутки в печени образуется примерно 12 г альбуминов.
Печень является единственным органом, где синтезируются белки плазмы крови, участвующие в гемостазе: протромбин, фибриноген I, проконвертин и проакцелерин.
Печень синтезирует группу транспортных белков: ферритин, церулоплазмин, транскортин, гаптоглобин и другие белки, участвующие в транспорте различных соединений, белки, входящие в состав липопротеидов различных классов.
Белковый обмен в печени настолько интенсивный, что печень за сутки обновляет 9% собственных белков и около четверти всех альбуминов плазмы. Особенностью обмена белков в печени является то, что скорость синтеза некоторых белков в печени избирательно стимулируется действием глюкокортикоидов (кортизола), в то время как в периферических тканях усиливаются процессы катаболизма и протеолиза белков.
2) синтез специфических белков печёночных клеток (например, органоспецифические ферменты: урокиназа, аргиназа, фруктозо-1-фосфатальдолаза, сорбитол ДГ).
За сутки в организме человека образуется около 80-100 г белка, из них половина в печени.
В гепатоцитах синтезируется лабильный резервный белок, который может расходоваться по мере необходимости для снабжения аминокислотами других органов и тканей при белковом голодании.
Печень занимает центральное место в обмене аминокислот в связи с тем, что здесь интенсивно протекают процессы трансаминирования, дезаминирования, непрямого дезаминирования, декарбоксилирования и окисления.
Печень поставляет в другие органы и ткани сбалансированную смесь аминокислот.
В печени активно идёт синтез небелковых азотистых соединений (креатина, глутатиона, никотиновой кислоты, пуринов и пиримидинов, порфиринов, коферментов), окисление аминокислот с образованием аммиака.
Потери белка в печени составляют ~ 20%, в то время как в других органах не более 4%.
Участие печени в обмене витаминов.
Складывается из процессов депонирования в ней, главным образом жирорастворимых витаминов, синтеза некоторых витаминов (никотиновая кислота) и коферментов, превращения кальциферолов в 25-гидрокальциферолы.
Участие печени в водно-минеральном обмене.
Печень задерживает ионы Na+, K+, Cl-, Ca2+ и воду и выделяет их в кровь. Кроме того, печень депонирует микроэлементы (железо, медь, цинк, свинец) и участвует в их распределении по другим тканям с помощью транспортных белков.
6. Участие печени в обмене азотистых оснований и нуклеиновых кислот проявляется в синтезе их из простых соединений и окислении до мочевой кислоты. Азотистые основания используются другими органами для синтеза нуклеозидов, нуклеотидов, нуклеиновых кислот, а мочевая кислота выделяется как конечный продукт обмена.
МОЧЕВИНООБРАЗОВАТЕЛЬНАЯ ФУНКЦИЯ (УРОГЕНЕЗ).
Печень – единственный орган, имеющий все ферменты цикла образования мочевины из аммиака. Аммиак, образующийся в других тканях, в печени превращается в индифферентный продукт – мочевину, которая выделяется в кровь.
ЖЁЛЧЕОБРАЗОВАТЕЛЬНАЯ И ЭКСКРЕТОРНАЯ ФУНКЦИИ:
Печень образует специальный жидкий экскрет – жёлчь, которая выделяется в тонкий кишечник. Только в печени образуются жёлчные кислоты и их конъюгаты, которые используются при переваривании и всасывании липидов в кишечнике.
В жёлчь входят: жёлчные кислоты, белки (альбумины, глобулины), холестерин и его эфиры, минеральные вещества (Ca, Na, K, Cu, Zn, Pb, Cl), вода, продукты пигментного обмена (билирубиндиглюкуронид), неактивные продукты обмена гормонов и витаминов.
В сутки у человека образуется 500-700 мл жёлчи (~10 мл на кг массы тела).
Жёлчеобразование происходит непрерывно. Различают печёночную жёлчь и пузырную, состоящую из ФЛ, ХС и жёлчных кислот в соотношении 2,5:1:12,5.
Вне пищеварения печёночная жёлчь переходит в жёлчный пузырь, где происходит её сгущение в результате всасывания воды и электролитов. Концентрация компонентов в пузырной жёлчи выше в 5-10 раз выше, чем в печёночной.
Жёлчные кислоты поддерживают и обеспечивают коллоидное состояние жёлчи.
В нормальной жёлчи большинство жёлчных кислот не вновь синтезированы, а реабсорбированы из кишечника и доставлены в печень благодаря энтерогепатической циркуляции. Основная масса всосавшихся в кишечнике жёлчных кислот (95%) поступает в печень по системе воротной вены. Около 2% жёлчных кислот по лимфатическим путям проходит в лимфатический проток, а затем в верхнюю полую вену и разносится током крови по всему организму. В печень жёлчные кислоты возвращаются через печёночную артерию. При однократном прохождении крови через печень извлекается 90-95% жёлчных кислот.
3-5% жёлчных кислот выводятся из организма в составе каловых масс (это литохолевая – вторичная жёлчная кислота).
Нормальное содержание в сыворотке крови жёлчных кислот – 2,5-6,8 мкМ.
Концентрация жёлчных кислот может возрастать в сыворотке крови при уменьшении их экскреции, нарушении их элименирования гепатоцитами, а также при нарушении кровообращения. Следовательно, повышение концентрации жёлчных кислот может быть следствием гепатоцеллюлярной патологии. При остром гепатите концентрация жёлчных кислот ↑ в 25-30 раз. При хроническом гепатите, концентрация жёлчных кислот не всегда достигает чёткого патологического уровня. Повышение в крови содержания жёлчных кислот также является ранним симптомом холестаза.
