
- •План – конспект уроку з теми:
- •Структура уроку:
- •V. Узагальнення і систематизація знань.
- •Vι. Підсумки уроку.
- •Vιι. Домашнє завдання.
- •V. Узагальнення і систематизація знань.
- •Vι. Підсумки уроку.
- •Vιι. Домашнє завдання.
- •План – конспект уроку на тему:
- •V. Узагальнення і систематизація знань.
- •Vι. Підсумки уроку.
- •Vιι. Домашнє завдання.
- •План – конспект уроку На тему: « Практична робота. Виявлення Карбону, Гідрогену і Хлору в органічних речовинах.»
- •Структура уроку:
- •3. Завдання на 9 – 12 балів:
- •V. Узагальнення і систематизація знань:
- •Vι. Підсумки уроку.
- •Vιι. Домашнє завдання.
- •План – конспект урок на тему:
- •V. Узагальнення і систематизація знань.
- •Vι. Підсумки уроку.
- •Vιι. Домашнє завдання.
- •План – конспект уроку на тему:
- •Тема: Поняття про полімери на прикладі поліетилену. Полімери та пластмаси. Застосування поліетилену та інших пластмас на основі вуглеводнів.
- •V. Узагальнення і систематизація знань.
- •Vι. Підсумки уроку.
- •Vιι. Домашнє завдання.
- •План – конспект уроку на тему:
- •Тема: Бензен як представник ароматичних вуглеводнів. Склад молекули. Структурна формула. Фізичні та хімічні властивості.
- •Хімічні властивості бензену
- •V. Узагальнення і систематизація знань.
- •Vι. Підсумки уроку.
- •Vιι. Домашнє завдання.
- •План – конспект уроку на тему:
- •Тема: Застосування бензену, його дія на організм. Поняття про хімічні засоби захисту рослин.
- •V. Узагальнення і систематизація знань.
- •Vι. Підсумки уроку.
- •Vιι. Домашнє завдання.
- •План – конспект уроку на тему:
- •Тема: Нафта, вугілля, природний газ як сировина. Склад і використання природного газу та нафти, їх властивості. Застосування нафтопродуктів.
- •V. Узагальнення і систематизація знань.
- •Vι. Підсумки уроку.
- •Vιι. Домашнє завдання.
- •План – конспект уроку на тему:
- •Тема: Застосування продуктів коксування кам’яного вугілля. Охорона довкілля під час переробки і використання вуглеводневої сировини.
- •Структура уроку:
- •Продукти піролізу кам'яного вугілля
- •V. Узагальнення і систематизація знань.
- •Vι. Підсумки уроку.
- •Vιι. Домашнє завдання.
- •I рівень:
- •II рівень:
- •III рівень:
- •Здійсніть перетворення:
- •4. Розв’яжіть задачу:
- •Vι. Підсумки уроку.
- •Vιι. Домашнє завдання. План – конспект уроку на тему:
- •Тема: Поняття про органічні сполуки. Спільні та відмінні ознаки органічних і неорганічних речовин.Природні і синтетичні органічні речовини.
План – конспект уроку з теми:
«Метан – найпростіша органічна сполука, його склад, структурна формула. Тетраедрична будова молекули. Фізичні властивості. Поширення у природі. Горіння метану, взаємодія з хлором. Застосування метану та його галагенопохідних, їх дія на організм».
Тема: Метан — найпростiша органiчна сполука. Фiзичнi та хімічні властивостi, поширення у природi. Застосування метану та його галогенопохiдних,їх дія на живі органiзми.
Мета: Ознайомити учнів зі складом, будовою, структурною і електронною формулою метану, просторовою будовою молекули, його хімічними і фізичними властивостями; розширити знання учнів про поширення органічних речовин у природі на прикладі метану. Розвинути увагу, спостережливість та мислення; Виховати вміння висловлювати власні думки та поважати думки інших.
Обладнання: Модель молекули метану.
Базові поняття: Структурна і електронна формули, просторова будова молекули.
Тип уроку: Вивчення нового матеріалу.
Структура уроку:
Ι. Організаційний момент
ΙΙ. Актуалізація опорних знань
ΙΙΙ. Мотивація
ΙV. Вивчення нового матеріалу
V. Узагальнення і систематизація
VΙ. Підбиття підсумків
VΙΙ. Домашнє завдання
Ι. Організаційний момент: привітання, перевірка присутніх, підготовка до уроку.
ΙΙ. Актуалізація опорних знань:
Бесіда.
Які елементи входять до складу органічних речовин ?
Які спільні ознаки органічних і неорганічних речовин, ви знаєте?
Які відмінні ознаки органічних і неорганічних речовин, ви знаєте?
Як ви думаєте, які елементи входять до складу органічної речовини, якщо вона належить до групи вуглеводнів ?
ΙΙΙ. Мотивація: Як ви гадаєте, чи може сніг горіти? Нещодавно стало вiдомо, що на днi Свiтового океану знаходяться величезнi запаси метану у виглядi пластiвцiв, що нагадують снiг або пухкий лiд. З погляду хiмiї, цi пластiвцi — газовi гiдрати (наприклад, СН4 . 6Н2О). Метановi гiдрати мають кристалiчну структуру льоду, де в порожнинах розташованi молекули метану. Горiння такої речовини справляє незабутнє враження: здається, що палає сніг. А пiсля згоряння на мiсцi газового гiдрату залишається лише калюжка води. Свiтовi запаси метану у виглядi газових гiдратiв складають 2 1016 м3. Це в десятки разiв бiльше, ниж запаси всiх iнших видiв палива (вугiлля, нафти, торфу).Отож, на даному уроці ми розглянемо групу органічних речовин до якої належить метан і з’ясуємо чим зумовлено його горіння.
ΙV. Вивчення нового матеріалу: Органiчнi речовини подiляються на три групи: вуглеводневi, оксигеновмiснi та нiтрогеновмiснi речовини. Вуглеводнi, у свою чергу, подiляються на насиченi (алкани) та ненасиченіi (алкенiв, алкiни, алкадiєни) та ароматичнi (арени). Насиченi вуглеводнi (алкани) — це органiчнi речовини, загальна формула яких СnH2n + 2
-
О

 рганічні
речовини
рганічні
речовини
Вуглеводні |
|
Оксигеновмістні |
|
Нітрогеновмістні |


 Насичені
(алкани)
Насичені
(алкани)
 Ненасичені
(алкени, алкіни, алкадієни)
Ненасичені
(алкени, алкіни, алкадієни)
Ароматичні (арени)
На даному уроці ми розглянемо будову і властивості органічних речовин на прикладі найпростішого представника насичених вуглеводнів – метану. Одним із факторів, що впливають на властивості хімічних сполук ( і органічних в тому числі), є будова речовини, тому ознайомимося з будовою метану.
Метан термічно (під дією температури) можна розкласти на прості речовини – Карбон і Гідроген. Отже, він складається з цих елементів. Відповідно, на один атом Карбону припадає чотири атоми Гідрогену. Звідси формула метану – CH4.Спробуємо визначити його структурну формулу, ґрунтуючись на понятті валентності.
- Завдання біля дошки:
1)Напишіть, як розподіляються електрони за рівнями і підрівнями атома Карбону.
2p2
|
↑ |
↑ |
|
|
|---|---|---|---|---|
↑↓ |
|
|||
|
|
|||
↑↓ |
|
|||
2s2
6 C
1s2
В атомi Карбону на зовнiшньому енергетичному рiвнi розмiщується чотири електрони: два спаренi та два неспаренi. Якщо атому надається енергiя, вдбувається розпаровування 2S-електронiв i перехід одного з них на вiльний р-рiвень. Такий стан атома Карбону називають – збудженим.
2p3
|
↑ |
↑ |
↑ |
|
|---|---|---|---|---|
↑ |
|
|||
|
|
|||
↑↓ |
|
|||
|
|
|||
2s1
6 C* 1s2
У атома Карбону після отримання додаткової енергії є чотири неспарених електрони, що здатні утворювати хімічні зв’язки. З урахуванням того що всіх органічних сполуках Карбон чотиривалентний, а Гідроген одновалентний, дійдемо висновку, що метан має брутто формулу CH4.
Структурна формула метану:
 Н
Н
 Н С Н
Н С Н
Н
Електронна формула метану:
Н : С : Н
Чотири електрони змiнюють форму свого руху (гiбридизують) i починають рухатися по витягнутiй вiсiмцi (неправильнiй).
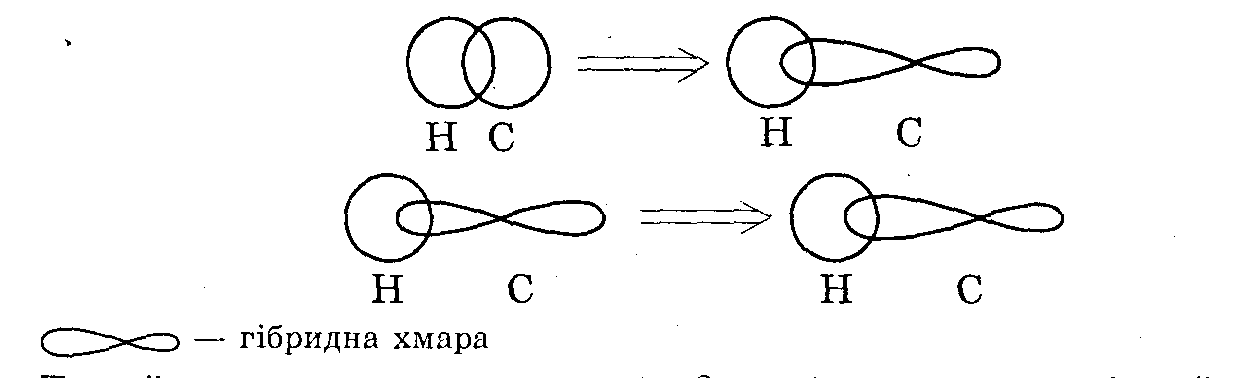
У молекулi вiдбувається sр3 -гiбридизацiя. Гiбридизованi орбiталi розмiщені в просторi вiд кутом 109° 28’ i на вiдстанi 0,154 нм, утворюючи просторову геометричну фiгуру тетраедр.
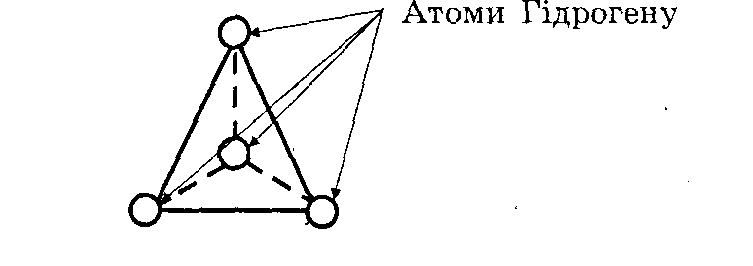
Усi зв’язки в молекулi алканів δ(сiгма)—зв’язки мiж двома атомами, спря - мованi вздовж прямої,що сполуча їхнi ядра та збiгається з вiссю симетрiї електронних хмарин. Атоми Карбону насичені атоми Гідрогену, - дуже міцні, для їхз розриву наобхідна велика енергія, а тому алкани – мало реакційні речовини.
Фізичні властивості метану і його поширення в природі. - самостійна робота у мікрогрупах:
1.Прочитати матеріал § 28 ст. 103-104.
2. Підготувати 5-6 запитань
3.Обмін запитаннями між гупами.
4. В разі неправильної відповіді відповідають бажаючі з інших груп. Якщо правильна відповідь незнайдена, відповідає та група яка склала запитання.
Хімічні властивості алканів на прикладі метану
Властивість |
Рівняння хімічної реакції |
Застосування, що базується на цих властивостях |
1.Повне окислення ( горіння)
|
CH4 +2O2 →CO2 +2H2O
|
Паливо у промисловості, побуті, інтенсифікація доменного процесу. Сажа – для виготовлення друкарських фарб, гумових виробів. |
2.Розклад |
CH4→С +2Н2 2CH4→C2H2 +H2 C4H10→CH4+ C3H6 |
Одержання етіну, водню(для синтезу амоніаку, органічних речовин). |
3.Заміщення
|
а)Галогеном: CH4 +Cl2→CH3 Cl + HCl CH3 Cl +Cl2→CH2 Cl2 +HCl CH2 Cl2 +HCl→CHCl3 + HCl CHCl3 + HCl→CCl4 + HCl
|
Одержання хлорпохідних алканів: CH3 Cl – холодоагент; CH2 Cl2 –анестезія; CHCl3 – розчинник; CCl4 –гасіння пожеж; |
4.Ізомеризація. |
CH3-CH2-CH2-CH3 ( н-бутан) CH3-CH(CH3)-CH3 ( ізобутан) |
|
5.Взаємодія з водою. |
CH4 +H2O→CO +H2 – синтез-газ
|
Одержання синтез-газу для синтезу метанолу. |
6.Синтез В’юрца. |
C2H6 →C3H8 C2H6 +Cl2→C2H5Cl +HCl CH4+Cl2→ CH3 Cl + HCl CH4+2Na+ CH3 Cl→C3H8+2NaCl |
Для одержання з одного алкану іншого |
Демонстрація: « Горіння парафінів»
Одержання метану з натрій ацетату.
У пробірці змішати кристалічні натрія ацетат і натрія гідроксид у співвідношенні 1:1. Закрити пробірку корком з газовідводноютрубкою і прогріти вміст пробірки. Метан, що виходить через газовідвідну трубку, підпалити.
