
- •28. Сравнение хим. Обезжиривания и э.Х. Обезжиривания. М-зм этих процессов. Усл. Реализ. Для цв. И черн. Мет. Пути интенсифик. Проц. Обезжир, сниж. Энергозатр. Методы контроля состояния поверхности.
- •Электрохимическое производство гипохлорита натрия
- •Электрохимическое получение хлоратов
- •Определяющий фактор в выборе технической схемы производства NaClO3 является соотношение на пар и на электричество.
Электрохимическое получение хлоратов
Применение:
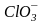 ;
соли используют в органическом синтезе,
пиротехнике, в производстве спичек,
гербецидов, красящих веществ в производстве
перхлоратов (
;
соли используют в органическом синтезе,
пиротехнике, в производстве спичек,
гербецидов, красящих веществ в производстве
перхлоратов ( ).
).
Наиболее применимы NaClO3 и KClO3 (бертолетова соль)
Получение: электролиз раствора NaCl в бездиафрагмовом электролизере.
А:
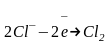
Гидролиз
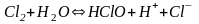
К:
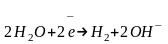
Хлорноватистая кислота взаимодействует со щелочью:
 .
.
Образующиеся
анионы
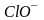 окисляются
на аноде:
окисляются
на аноде:
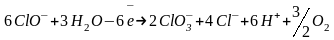 .
.
В растворе протекает химическая реакция:
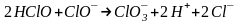 .
.
На катоде – побочная электрохимическая реакция восстановления и

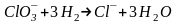 .
.
Для уменьшения потерь вводят добавку K2Cr2O7.
Хлораты
Электролит:
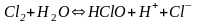
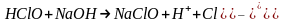
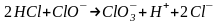
А: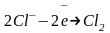
К: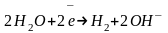
Таким образом, получение хлоратов возможно в результате:
химического окисления
 хлорноватистой
кислатой,
хлорноватистой
кислатой,анодного окисления иона .
Соотношения между скоростями реакций зависит от условий электролиза.
Для
получения хлоратов обычно используют
концентрированные растворы (280г/л)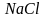 ,
так как уменьшается концентрация
исходного раствора
,
так как уменьшается концентрация
исходного раствора
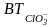 уменьшается.
уменьшается.
Аноды- графит, металлооосидные-ОРТА,Fe3O4,Ti-PbO2,ПТА( Pt несколько мкм ).
С- аноды разрушаются, особенно при i=0,8-1,0 кА/м2 и при увеличение t от 400С до 500С.
Оптимальный износ С-А : 6-8 кг/т ClO-
Для МИА i=1,5-3,5 кА/м2.
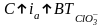
Так как получение хлората протекает не только по ЭХ реакции, но и по химической реакции, процесс характеризуется объемной I (или концентрацией тока).
Объемная плотность тока – это отношение силы тока, проходящей через электролизер к объему электролита (А/л).
Для химической стадии целесообразно увеличить время пребывания раствора в электролизере, т.е. проводить процесс с низким iоб.
Обычно iоб~10А/л и более.
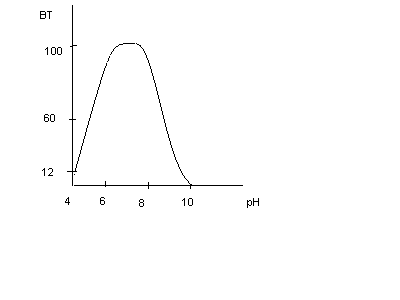
Значение рН: 6,0-6,8.Скорость химической реакции максимальна.
Поддерживают
постоянным введение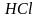 ,
используя буферные свойства бихромата
в области рН:
,
используя буферные свойства бихромата
в области рН:
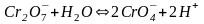
Бихромат калия для уменьшения потерь и вследствие их восстановления на катоде.
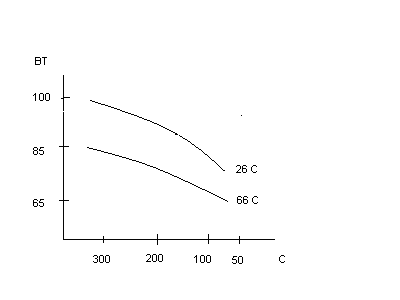
Температура .
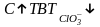 .
.
При
интенсивном перемешивании
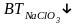
Поэтому для увеличения суммарного ВТ процесс ведут при небольших iоб и интенсивной циркуляции раствора через выносной дозреватель, в котором происходит химический процесс окисления в .В этом случае электролизер служит как бы генератором NaClO3.
На
С-аноде -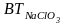 ~83-85%
~83-85%
МИА – Вт 94 – 96%
В настоящее время электролизеры используются совместно с дозревателями
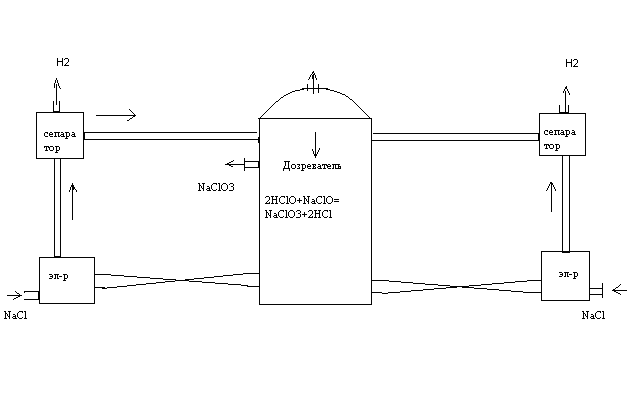
В электролизерах электролиз с образованием NaClO и HClO.Электролит за счет подъемной силы Н2 поднимается по трубам и поступает в сепараторы, где отделяется от жидкости. Далее электролит поступает в дозреватель, где при повышении температуры идет химическая реакция. После накопления NaClO3 до 550-600 г/л раствор отводят.
NaClO3 получают в твердом виде либо выпариванием, либо вымораживание при охлаждении до -2 – (-10)0С.
