
- •1.Уравнение Гиббса.Каким образом величина изменения энергии Гиббса характеризует возможность протекания данного процесса?
- •2.Что представляют собой стандартные значения термодинамических функций?Для каких условий они рассчитываются?
- •3.Какая величина называется «химическим потенциалом»?От каких факторов зависит его значение?
- •4.Что такое «стандартный химический потенциал»?От чего зависит его значение?
- •5. Общее свойство всех термодинамический функций.Закон Гесса
- •6. Зависимость изменения энтальпии от температуры.Уравнение Кирхгофа
- •10.Какая величина называется скоростью гомогенной химической реакции. Привидите математическое выражение!
- •11. Факторы, влияющие на скорость химической реакции:
- •12. Какое соотношение описывает зависимость скорости химической реакции от концентрации реагирующих веществ? Закон действующих масс
- •Закон действующих масс в химической кинетике
- •Закон действующих масс в химической термодинамике
- •13. Какие соотношения описывают зависимость скорости химической реакции от температуры?
- •14.Какие вещества называются катализаторами?Что такое ингибиторы?
- •16. Каков физический смысл константы скорости реакции? От каких факторов зависит значение этой величины?
- •17. Вывод кинетического уравнения реакции I-го порядка.
- •18. Вывод кинетического уравнения реакции II -го порядка.
- •19.В чём заключается сущность графического метода определения порядка реакции?
- •20.Какая величина называется энергией активации?Каков её физический смысл?
- •21.Каков механизм действия катализаторов?Энергетические схемы обычных и каталитических реакций.
- •25.Какое явление называется диффузией? Что такое скорость диффузии? Уравнение Фика.
- •26.Какие системы называются растворами? Классификация растворов по агрегатному состоянию.
- •27.Какой способ выражения концентрации называется массовой долей?
- •28.Какой способ выражения концентрации называется молярной концентрацией?
- •29.Какой способ выражения концентрации называется моляльной концентрацией?
- •30.Какой способ выраженияконцентрации называется моляльной долей?
- •31.Каким образом растворимость газов зависит от давления газа?Закон Генри
- •32. Каким образом растворимость газов зависит от температуры и от наличия в растворе других растворённых веществ?
- •33.Какой общий принцип определяет растворимость жидких и твёрдых веществ в жидкостях?
- •37. Какое уравнение описывает зависимость осмотического давления от концентрации растворённого вещества?
- •38.Какова роль осмоса в процессах жизнедеятельности растительных и животных организмов?
- •39. Каким образом температуры кипения растворов отличаются от температур кипения растворителя? Эбулиоскопическая постоянная
- •40.Каким образом температуры замерзания растворов отличаются от температур замерзания растворителя?Криоскопическая постоянная?
- •41.На какие группы делятся вещества по поведению в процессе растворения?в чём заключаются особенности поведения растворов электролитов и неэлектролитов?
- •42.Какая поправка вносится в законы,описывающие ависимость свойств растворов электролитов от их состава?
- •43. Произведение растворимости труднорастворимых электролитов.
- •44. Электролитическая диссоциация воды. Ионное произведение воды. РН раствора.
- •45. Какие свойства растворов называются коллигативными?
- •49.Какие величины используются для количественной оценки процесса набухания?
- •50.Для каких полимеров характерно явление неограниченного набухания? Кривые неограниченного набухания.
- •51.Для каких полимеров характерно явление ограниченного набухания? Ограниченное набухание линейных полимеров.Кривые ограниченного набухания.
14.Какие вещества называются катализаторами?Что такое ингибиторы?
1.Катализаторы, вещества, изменяющие скорость хим. реакции или вызывающие ее, но не входящие в состав продуктов.
Различают катализаторы гомогенного и гетерогенного катализа. Типичные катализаторы для гомогенного катализа - протонные и апротонные кислоты, основания, некоторые комплексы металлов, для гетерогенного - металлы, оксиды металлов, сульфиды и других. Реакции одного и того же типа могут протекать в условиях как гомогенного, так и гетерогенного катализа. Так, для кислотно-основных реакций типичные катализаторы - растворы кислот и оснований или твердые тела с кислотными (Аl2О3, ТiO2, ТhO2, алюмосиликаты. цеолиты и др.) или основными [CaO, BaO, MgO, Ca(NH2)2 и др.] свойствами (см. Гетерогенный катализ. Гомогенный катализ. Кислотно-основной катализ). Для окислительно-восстановительных реакций наиб. распространенными катализаторами являются переходные металлы (Pt, Pd, Ni, Fe, Co), оксиды (V2O5, MnO2, MoO3, Сr2О3), в т.ч. шпинели. сульфиды (MoS2, WS2, CoS), а также полупроводники. не имеющие в своем составе переходных элементов.
2.ИНГИБИТОРЫ - в-ва, тормозящие хим. р-ции. Ингибирование характерно для каталитич и цепных р-ций, к-рые протекают с участием активных центров или активных частиц. Тормозящее действие обусловлено тем, что ингибитор блокирует активные центры катализатора или реагирует с активными частицами с образованием малоактивных радикалов, не способных продолжать цепь. Ингибитор вводится в систему в концентрации много меньшей, чем концентрации реагирующих в-в (102-105 моль%). Кинетика р-ций с участием ингибиторов принципиально различна для каталитических и цепных р-ций. В каталитич. р-ции число активных центров фиксировано и ингибитор, блокируя часть из них, не расходуется в ходе процесса. Поэтому при введении ингибитора скорость р-ции снижается, а затем процесс протекает длит. время с постоянной скоростью. В нек-рых случаях эта скорость может медленно возрастать из-за расходования ингибитора по к.-л. побочной р-ции. В цепной р-ции активные частицы непрерывно генерируются, что приводит к расходованию ингибитора и постепенному самоускорению р-ции (в случае цепной неразветвленной р-ции обычно восстанавливается исходная скорость). 15.Какая величина называется порядком реакции?Какие значения она может принимать?
ПОРЯДОК РЕАКЦИИ - показатель степени при концентрации этого в-ва в кинетич.. ур-нии р-ции. Согласно действующих масс закону, скорость у простой (одностадийной) р-ции между в-вами А и В типа nАА + nBB : продукты равна:
![]()
где uА-скорость расходования реагента А, СА и Св-концентрации реагентов А и В, k - константа скорости р-ции, nА и nв-порядки реакции по реагентам А и В соотв., п = nА + nв-общий порядок реакции (nА и nв- частные порядки реакции). Для гомог. р-ции порядок реакции по данному в-ву представляет собой стехиометрич. коэф. этого в-ва в ур-нии р-ции. Напр., в р-ции 2NO + С12 : 2NOC1 порядок реакции по NO равен 2, порядок реакции по С12 равен 1, а общий порядок реакции равен 3. Для простых р-ций порядок реакции всегда целое число (1, 2 или 3).
Для сложных р-ций порядки реакции редко совпадают с суммой стехиометрич. коэф., он м. б. числом переменным, дробным и даже отрицательным. Напр., для параллельных р-ций типа
![]() продукты;
продукты;![]() продукты (k1
и k2-
константы
скорости для соответствующих стадий)
суммарная скорость расходования А
составляет uА
= k1СА
+
продукты (k1
и k2-
константы
скорости для соответствующих стадий)
суммарная скорость расходования А
составляет uА
= k1СА
+![]() и
порядок реакции
меняется по мере увеличения СА
от 1 (uA
— k1
СА)
до 2 (uА
=
и
порядок реакции
меняется по мере увеличения СА
от 1 (uA
— k1
СА)
до 2 (uА
=![]() Для
цепной р-ции типа+
Для
цепной р-ции типа+![]()
![]() +
+![]()
![]()
![]() D
в условиях, когда k1CA
D
в условиях, когда k1CA![]()
![]() скорость
расходования А составляет
скорость
расходования А составляет![]() ,
т. к.
,
т. к.
![]() =
(k1
CA/k3)1/2,
то
=
(k1
CA/k3)1/2,
то![]() так
что nА
= 3/2. Для мономолекулярного превращения
А в присут. В, образующего с А неактивный
комплекс (А
так
что nА
= 3/2. Для мономолекулярного превращения
А в присут. В, образующего с А неактивный
комплекс (А![]() продукты; А + В
продукты; А + В![]() D),
скорость р-ции
D),
скорость р-ции
![]() (К-
константа
равновесия). Если равновесие
сдвинуто вправо (CD
(К-
константа
равновесия). Если равновесие
сдвинуто вправо (CD![]() CA),
порядок реакции
по В равен -1.
CA),
порядок реакции
по В равен -1.
Если зависимость скорости расходования исходного реагента или скорости накопления продукта сложной р-ции от соответствующих концентраций не описывается степенной ф-цией, говорить о порядке реакции по данному реагенту (продукту) не имеет смысла. Напр., скорость превращения субстрата S.
![]()
в
присут. фермента
Е составляет(KM-константа
Михаэлиса) и зависит от начальнойконцентраций
фермента
![]() в
первой степени, а зависимость от
концентрации субстрата
Cs
не степенная. Такая р-ция имеет первый
порядок по ферменту,
говорить же о порядке реакции
по субстрату
не имеет смысла.
в
первой степени, а зависимость от
концентрации субстрата
Cs
не степенная. Такая р-ция имеет первый
порядок по ферменту,
говорить же о порядке реакции
по субстрату
не имеет смысла.
Существует
ряд эмпирич. методов определения порядка
реакции
1) Проводят серию опытов с переменной
концентрацией
реагента
А, определяют начальную скорость его
расходования uА
и находят порядок реакции
как отношение: nА
= dln uA/dln
CA.
2) Все реагенты,
кроме А, берут
в избытке, скорость расходования A ut
измеряют в разные моменты времени t,
порядок реакции
находят как отношение: nА
= dln ut/dln
CA.
3) Измеряют время t1/p
превращения А на 1/p-ю часть, когда все
реагенты,
кроме А, взяты в избытке. Это время не
зависит от начальной концентрации![]() в-ва
А, если nА
= 1; оно обратно пропорционально
в-ва
А, если nА
= 1; оно обратно пропорционально
![]() при
nА
= 2 и обратно пропорционально
при
nА
= 2 и обратно пропорционально
![]() при
nА
= 3. Так, для превращения на 50% t1/2
= k-1
ln 2 при nА
= 1; tl/2
= (k
при
nА
= 3. Так, для превращения на 50% t1/2
= k-1
ln 2 при nА
= 1; tl/2
= (k![]() )-1
при nА
= 2 и t1/2
= 3/2k при nА
= 3. Здесь k-константа скорости р-ции, если
)-1
при nА
= 2 и t1/2
= 3/2k при nА
= 3. Здесь k-константа скорости р-ции, если
![]() в
р-ции участвует только один реагент
А; если же А реагирует с В, то k равна
константе
скорости, умноженной на начальную
концентрацию
В. В общем случае для п — 1 t1/p
= k-1ln[p/(p-l)],
a для n.1 t1/р={[p/p-1]n-1-—
1}
в
р-ции участвует только один реагент
А; если же А реагирует с В, то k равна
константе
скорости, умноженной на начальную
концентрацию
В. В общем случае для п — 1 t1/p
= k-1ln[p/(p-l)],
a для n.1 t1/р={[p/p-1]n-1-—
1}![]() ·(п
— 1)k. 4) Следят за расходованием А и
определяют порядок реакции
по кинетич. кривой (см. Кинетическое
уравнение). Если nА
= 1, то А расходуется по экспоненц. закону
и uА
= e-kt.
Если я = 2, то кинетич. кривая описывается
ф-лой:
·(п
— 1)k. 4) Следят за расходованием А и
определяют порядок реакции
по кинетич. кривой (см. Кинетическое
уравнение). Если nА
= 1, то А расходуется по экспоненц. закону
и uА
= e-kt.
Если я = 2, то кинетич. кривая описывается
ф-лой:![]() uА
=
uА
=![]() (1
+ 2k
(1
+ 2k![]() t)-2.
По совпадению эксперим. данных с одной
из этих ф-л определяют nА
.
t)-2.
По совпадению эксперим. данных с одной
из этих ф-л определяют nА
.
Если продукты р-ции влияют на ее протекание, напр. при автокатализе, кинетич. ур-ние становится приближенным. В этих случаях наиб. надежным является 1-й метод определения порядка реакции. Общий порядок реакции можно определить любым из перечисл. методов, проводя р-цию со стехиометрич. смесью реагентов.
Реакции первого порядка. Если скорость реакции зависит от концентрации только одного реагента в первой степени, то выражение для скорости принимает вид

О такой реакции говорят, что она является реакцией первого порядка.
Реакции второго порядка. Когда скорость реакции пропорциональна квадрату концентрации отдельного реагента или концентрациям каждого из двух реагирующих веществ в первой степени, мы имеем дело с реакцией второго порядка. В дифференциальной форме выражения для скорости такой реакции имеют вид
![]()
и
![]()
Реакции третьего порядка. Скорость реакции третьего порядка может зависеть от концентрации одного реагента в третьей степени, либо концентрации одного реагента во второй степени и второго реагента в первой степени, либо от концентрации каждого из трех реагентов в первой степени. Так,
![]()
или
dx/dt = k(a – x)3
Реакции нулевого порядка. Скорость реакций нулевого порядка не зависит от концентраций реагентов и определяется другими лимитирующими факторами, например площадью поверхности катализатора (в реакциях гетерогенного катализа) или поглощением света (в фотохимических реакциях). Уравнение для скорости такой реакции в дифференциальной форме имеет вид
–dC/dt = k
Реакции п-го порядка. В общем случае для реакции порядка п при п > 1 связь между концентрацией и временем для конечного времени наблюдения описывается уравнением
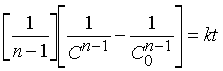
где С – концентрация реагента в момент времени t, C0 – начальная концентрация. График зависимости 1/(Сn – 1) от t представляет собой прямую с наклоном (n–1) k. Размерность k – (моль/л)1 – n/c.
Реакции не всегда имеют целочисленный порядок. Показатели степени при концентрациях в выражении для скорости часто являются дробными. Однако и в этом случае порядок реакции равен сумме показателей степеней. Например, для реакции, скорость которой равна

порядок п = 0,7 + 1,8 = 2,5.
Часто порядок реакции, определяемый экспериментально, не соответствует порядку, который следует из стехиометрического уравнения. Большинство химических реакций включает две или несколько стадий, протекающих одновременно, что приводит к более сложным выражениям для скорости.
