- •1. Особенности строения и биологическая роль природных пептидов. Пептидная связь. Качественные реакции на пептиды. Методы анализ аминокислотных последовательностей
- •Биологически активные пептиды
- •2. Состав нуклеиновых кислот. Пуриновые и пиримидиновые основания. Нуклеозиды и нуклеотиды. Строение и номенклатура. Полинуклеотиды. Первичная и иные структуры рнк и днк.
- •2. Днк. Содержание в организмах, локализация в клетке. Первичная и вторичная структуры. Принцип комплементарности. Третичная структура днк (хроматин). Биологические функции днк.
- •1. Химические свойства аминокислот. Биологически важные химические реакции аминокислот. Пиридоксальфосфат. Альдимин I. Трансаминирование и декарбоксилирование аминокислот в организме.
- •2. Нуклеозидмонофосфаты и полифосфаты. Их функции и значение в метаболизме.
- •1. Форма белковых молекул. Глобулярные и фибриллярные белки. Олигомирные белки. Преимущества четвертичной структуры белков и ферментов.
- •2. Макроэргические соединения. Атф как универсальный источник энергии. Другие макроэргические соединения и их биологическая роль.
2. Днк. Содержание в организмах, локализация в клетке. Первичная и вторичная структуры. Принцип комплементарности. Третичная структура днк (хроматин). Биологические функции днк.
Структура ДНК
ДНК является носителем генетической информации.
Первичная структура ДНК представляет собой последовательность азотистых оснований, содержащих в своем составе углеводный остаток –дезоксирибозу, соединенных фосфодиэфирными связями
Вторичная структура представляет собой двойную спираль, образованную двумя полинуклеотидными цепочками, скрученными в правовращающую спираль вокруг одной и той же оси. Цепи могут быть разделены только путём раскручивания
Они стабилизированы водородными связями комплементарных по отношению друг к другу оснований
Две цепи являются антипараллельными
Одну из двух комплементарных цепей называют кодирующей, а другую – не кодирующей.
Вдоль спирали основания уложены стопкой друг на друга, образуя параллельные плоскости, удерживаемые гидрофобными межплоскостными взаимодействиями оснований.
Комплементарность— пространственная взаимодополняемость молекул или их частей, приводящая к образованию водородных связей.
В нуклеиновых кислотах наблюдается комплементарность последовательностей оснований в противоположных цепях ДНК. Азотистые основания нуклеотидов способны вследствие образования водородных связей формировать парные комплексы аденин—тимин (или урацил в РНК) и гуанин—цитозин при взаимодействии цепей нуклеиновых кислот.
Таким образом, две полинуклеотидные цепи в результате комплементарного взаимодействия пар пуриновых и пиримидиновых оснований (А-Т, Г-Ц) образуют двуспиральную молекулу.
Комплементарность очень важна для репликации ДНК, обеспечивающей передачу генетической информации при делении клетки, и для транскрипции ДНК в РНК при синтезе белков.
Функции ДНК 1. ДНК является носителем генетической информации. Функция обеспечивается фактом существования генетического кода. 2. Воспроизведение и передача генетической информации в поколениях клеток и организмов. Функция обеспечивается процессом репликации. 3. Реализация генетической информации в виде белков, а также любых других соединений, образующихся с помощью белков-ферментов. Функция обеспечивается процессами транскрипции и трансляции.
БИЛЕТ № 4
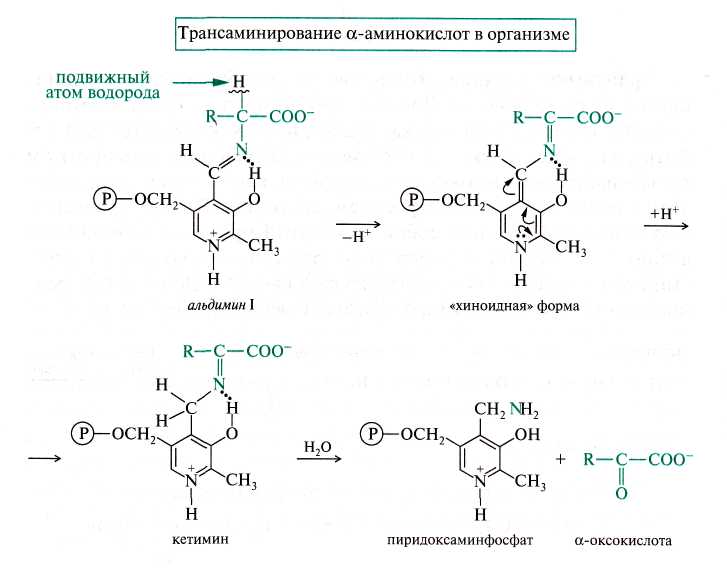
1. Химические свойства аминокислот. Биологически важные химические реакции аминокислот. Пиридоксальфосфат. Альдимин I. Трансаминирование и декарбоксилирование аминокислот в организме.
Химические свойства аминокислот
Кристаллические аминокислоты хорошо растворяются в воде.
В водном растворе α-аминокислоты существуют в виде равновесной смеси цвиттериона, катионной и анионной форм. Значение рН, при котором концентрация цвиттериона максимальна, а минимальные концентрации анионных и катионных форм α-аминокислот равны, называется изоэлектрической точкой.
Наличие в составе молекул α-аминокислот двух различных функциональных групп кислотного и основного характера обуславливает амфотерные свойства. Поэтому α-аминокислоты образуют соли как со щелочами, так и с кислотами.
С катионами тяжелых металлов α-аминокислоты, как бифункциональные соединения, образуют внутрикомплексные соли.
α-Аминокислоты как гетерофункциональные соединения вступают в реакции, характерные для карбоксильной и аминогруппы:
1. Образование эфиров – этерификация. В качестве катализатора выступает – газообразный хлороводород.
2. Образование галогенангидридов.
3. Образование N-ацильных производных.
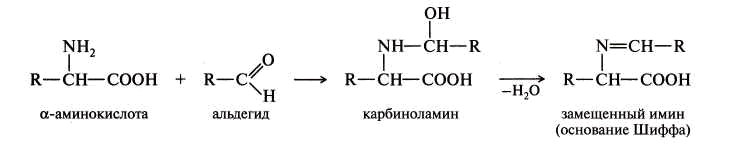
4. Образование оснований Шиффа.
5. Образование ДНФ-производных.

6. Образование ФТГ-производных (реакция Эдмана).
Биологически важные химические реакции с участием α-аминокислот
Химические реакции, протекающие в живых организмах через стадию альдимина I:
трансаминирование,
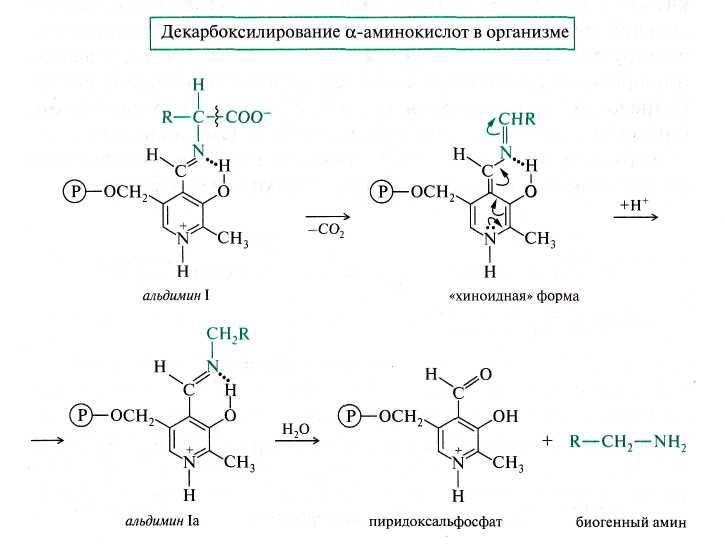
декарбоксилирование,
элиминирование,
рацемизация,
альдольное расщепление
и т.д.