
- •Лекція №1. Вступ
- •Лекція №2. Агрегатні стани речовини. Газоподібний стан речовини
- •Основні положення кінетичної теорії газів
- •Основні закони і рівняння ідеального газу
- •Реальні гази
- •Застосування рідких газів
- •Лекція №3. Рідкий стан речовини
- •Властивості рідин залежать:
- •Значення в’язкості
- •Характеристики рідкого стану речовини
- •Лекція №4. Твердий стан речовини
- •Процеси, що відбуваються з утворенням кристалічної решітки:
- •Лекція №5. Термодинаміка: основні поняття та закони
- •Застосування хімічної термодинаміки для:
- •Залежно від кількості фаз системи класифікують на:
- •Перетворення речовин бувають:
- •Способи передачі енергії системі або від неї:
- •І та іі закони термодинаміки і закон термодинаміки (Майєр, 1842; Гельмгольц, 1847)
- •І закон термодинаміки для ізохорних та ізобарних процесів
- •Спонтанні процеси. Ентропія
- •Іі закон термодинаміки (Клаузіус, 1850; Томсон, 1851)
- •Сутність теплових процесів у харчових виробництвах
- •Теплофізичні закономірності процесів варіння і смаження
- •16 Лютого 2005р. Вступив у дію Кіотський протокол. Основні зобов’язання щодо скорочення викидів у повітря шести парникових газів (со2, сн4, n2o, sf6, hfCs, pfCs) узяли на себе індустріальні країни:
- •Виробництво нових синтетичних холодоагентів (групи нfc) для пкхм.
- •Застосування природних холодоагентів (со2, с3н8, nh3).
- •Удосконалення екологічно чистої холодильної техніки, що базується на низько ефективних принципах одержання холоду.
- •Розробка нових принципів одержання холоду.
- •Виробництво холодильних машин Стірлінга помірного холоду.
- •Лекція №6. Термохімія: основні поняття та закони
- •Калорійність основних складових частин їжі та алкогольних напоїв
- •Закони термохімії
- •Лекція №7. Хімічна кінетика
- •Зміна швидкості реакції в часі
- •Залежність швидкості реакції від концентрації реагентів
- •Вплив температури на швидкість реакції
- •Теорія перехідного стану
- •Початковий стан (Реагенти) → Перехідний стан (Активований комплекс) → Кінцевий стан (Продукти)
- •Вплив каталізатора на швидкість реакції
- •Розвиток ланцюга.
- •Обрив ланцюга.
- •Лекція №8. Каталіз. Ферментативний каталіз
- •К аталіз
- •Каталіз
- •Гомогенний
- •Гетерогенний
- •Ферментативний
- •Загальні властивості:
- •Властивості ферментів
- •Лекція №9. Хімічна рівновага
- •Вплив температури на стан рівноваги
- •Вплив тиску на стан рівноваги
- •Застосування принципу Ле Шательє
- •Застосування принципу Ле Шательє
- •Лекція №10. Розчини. Розчинність газів, рідин і твердих речовин
- •Рідкі розчини
- •Розчинність рідин у рідинах
- •Застосування екстракції
- •Лекція №11. Властивості розбавлених розчинів неелектролітів
- •Роль дифузії
- •Залежність р насиченої пари від температури над чистим розчинником і над розчином
- •Вплив процесу заморожування на властивості харчових продуктів
- •Лекція №12. Властивості розбавлених розчинів електролітів
- •Визначення рНх за допомогою калібрувального графіка:
- •Індикаторний метод
- •Спосіб Міхаеліса
- •Вплив рН середовища на перебіг технологічних і ферментативних процесів
- •Буферні розчини
- •Лекція №13. Основи електрохімії
- •Абсолютна швидкість і рухливість іонів. Закон Кольрауша
- •Фізико-хімічні методи дослідження
- •Водневий електрод. Будова, принципи роботи, призначення
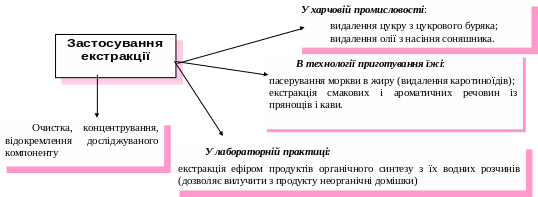
Застосування екстракції
Процес екстракції використовується для вилучення цінних речовин, що входять до складу складного твердого тіла найчастіше поруватої структури, а також при приготуванні багатьох напоїв. Так, приготування чаю і кави – типовий процес екстракції з твердих речовин (водою) компонентів, що обумовлюють смак і запах цих напоїв. При цьому для ефективної екстракції цінних компонентів кави попередньо подрібнюють. Установлено, що число екстрактивних речовин, які переходять у воду, збільшується майже у 1,5рази, якщо розмір часточок розмеленої кави дорівнює 200мкм, порівняно з кавою, часточки якої мають розмір 800мкм.
При приготуванні бульйонів м'ясо занурюють у холодну воду, нагрівають до кипіння і варять на слабкому вогні. При цьому способі у рідину переходить більша кількість екстрактивних речовин, а м'ясо стає більш плотним і м’яким. Для виготовлення других страв м'ясо занурюють у гарячу воду, доводять до кипіння і варять, не допускаючи кипіння, при 80 – 90 С. При такому способі у рідину переходить менша кількість білків та екстрактивних речовин. Одержаний бульйони є менш смачним, проте м'ясо – більш ніжним і смачним. Білки м’яса утворюють ніжніші згустки і утримують більшу кількість вологи. Для більшої ефективності процесу екстракції сировину подрібнюють для збільшення питомої активної поверхні (використання м’ясної відтяжки для освітлення кісткових бульйонів).
Лекція №11. Властивості розбавлених розчинів неелектролітів
Основні питання:
Ідеальні розчини. Колігативні властивості розчинів.
Дифузія.
Осмос.
Тиск пари над розчинами. І закон Рауля.
Замерзання та кипіння розчинів. ІІ закон Рауля.
Розчини, утворення яких з компонентів не супроводжується зміною об’єму системи (∆V=0), тепловими ефектами (∆Н=0), називають ідеальними розчинами .
Причина утворення ідеальних розчинів: зростання ентропії при змішуванні.
До моделі ідеального розчину наближаються безмежно розбавлені розчини (концентрація розчиненої речовини занадто мала, відносно великі відстані між молекулами, тому можна знехтувати силами взаємодії між частинками розчиненої речовини і розчинника).
Властивості ідеальних розчинів не залежать від природи розчиненої речовини, а визначаються лише концентрацією.
Згідно з рекомендацією ІЮПАК, концентрацією розчиненої речовини (не розчину!) називають відношення кількості або маси розчиненої речовини до об’єму розчину; концентрацію виражають у моль на літр або грамах на літр.
Концентрація – це відношення не однотипних величин. Відношення однотипних величин називається часткою, наприклад, відношення маси розчиненої речовини до маси розчину називається масовою часткою розчиненої речовини у розчині.
Властивості розчинів, які не залежать від природи розчиненої речовини, а визначаються кількістю частинок у розчині, називаються колігативні (означає „зв’язані між собою”).
До колігативних властивостей розчинів належать:
осмотичний тиск;
зниження тиску насиченої пари розчинника над розчином;
підвищення температури кипіння розчинів;
зниження температури замерзання розчинів.
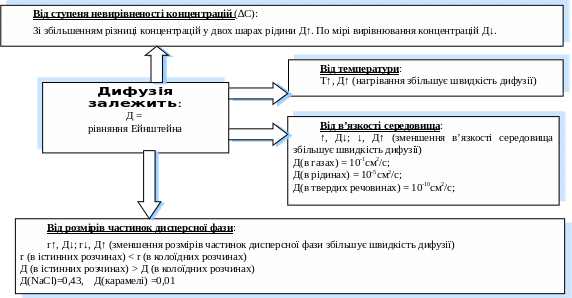
Дифузія – це довільний процес поступового проникнення частинок однієї речовини (під впливом їх теплового руху) в середовище другої речовини, внаслідок чого концентрації речовин у всіх частинах об’єму системи вирівнюються.
Кількісною мірою дифузії у стандартних умовах є коефіцієнт дифузії (Д) – характеризує здатність речовин до дифузії – вимірюється кількістю речовини, що перенесена за одиницею часу через одиницю площі поверхні (м2/с).
Для інтенсифікації процесу розчинення тверду речовину подрібнюють для збільшення площі поверхні контакту з рідиною (збільшення питомої поверхні твердої речовини).
У
технологічних процесах:
дифузія
солі, води, цукру, барвників тощо; під
час варіння, набухання, засолювання,
консервування та інших процесів. Приготування
бульйонів
(збільшення переходу екстрактивних
речовин у розчин) – збільшення швидкості
дифузії: велика
кількість рідини (1:3,5); продукт
занурюють у холодну воду; використання
відтяжки (зменшення розміру частинок,
збільшення поверхні стикання),
подрібнення кісток; солять
у кінці (збільшення ∆С).
В
життєдіяльності організмів: процеси
переносу поживних речовин та продуктів
обміну в живих
організмах.
