
- •Экзаменационный билет № 1
- •Общие представления о теориях строения дэс. Уравнение Пуассона-Больцмана для диффузной части дэс и его решение для случая слабозаряженных поверхностей. Уравнение Гуи-Чепмена.
- •Экзаменационный билет № 2
- •Механизмы образования дэс. Соотношение между электрическим потенциалом и поверхностным натяжением (уравнение Липпмана). Электрокапиллярные кривые и определение параметров дэс.
- •В таблице приведены данные по адсорбции паров воды макропористым адсорбентом при комнатой температуре. Пользуясь уравнением Ленгмюра определите емкость адсорбционного монослоя:
- •Экзаменационный билет № 3
- •Современная теория строения дэс (теория Штерна); роль специфической адсорбции, перезарядка поверхности. Примеры образования дэс. Строение мицеллы.
- •Адгезия и смачивание, определения. Уравнение Дюпре для работы адгезии. Угол смачивания и уравнение Юнга. Уравнение Дюпре-Юнга для работы адгезии. Влияние пав на адгезию и смачивание.
- •Экзаменационный билет № 5
- •Правило фаз Гиббса и дисперсность. Влияние кривизны поверхности (дисперсности) на внутреннее давление тел (вывод и анализ уравнения Лапласа). Капиллярные явления (уравнение Жюрена).
- •Вывод уравнения для скорости осаждения частиц в гравитационном поле. Условия соблюдения закона Стокса. Седиментационный анализ, расчет и назначение кривых распределения частиц по размерам.
- •Экзаменационный билет № 6
- •Экзаменационный билет № 7
- •Седиментационно-диффузионное равновесие (гипсометрический закон). Вывод уравнения. Мера седиментационной устойчивости. Факторы, влияющие на седиментационную устойчивость дисперсных систем.
- •Экзаменационный билет № 8
- •Экзаменационный билет № 9
- •Мономолекулярная адсорбция, форма изотермы адсорбции. Уравнение Генри. Основные положения теории Ленгмюра.
- •Лиофильные дисперсные системы. Классификация и общая характеристика пав. Термодинамика и механизм мицеллообразования. Строение мицелл пав в водных и углеводородных средах. Солюбилизация.
- •Экзаменационный билет № 10
- •Лиофильные дисперсные системы. Истинно растворимые и коллоидные пав, их классификация. Мицеллообразование, строение мицелл, методы определения ккм. Факторы, влияющие на ккм.
- •Экзаменационный билет № 11
- •Гидрозоль AgI получен добавлением 8 мл кi с концентрацией 0,05 моль/л к 10 мл раствора AgNo3 с концентрацией 0,02 моль/л. Напишите формулу мицеллы образовавшегося золя и объясните строение дэс.
- •Экзаменационный билет № 12
- •Экзаменационный билет № 13
- •Потенциальная теория адсорбции Поляни. Адсорбционный потенциал. Характеристическая кривая адсорбции. Температурная инвариантность и афинность характеристических кривых.
- •Экзаменационный билет № 14
- •Экзаменационный билет № 15
- •Экзаменационный билет № 16
- •Экзаменационный билет № 17
- •Ньютоновские жидкости, уравнения Ньютона и Пуазейля. Методы измерения вязкости. Уравнение Эйнштейна для вязкости дисперсных систем, границы применения.
- •Экзаменационный билет № 18
- •Седиментационный анализ. Кривые распределения частиц по размерам, их расчет и назначение, седиментация в центробежном поле.
- •Экзаменационный билет № 19
- •Правило фаз Гиббса и дисперсность. Влияние кривизны поверхности (дисперсности) на внутреннее давление тел (вывод и анализ уравнения Лапласа). Капиллярные явления (уравнение Жюрена).
- •Экзаменационный билет № 20
- •Седиментационно-диффузионное равновесие (гипсометрический закон). Вывод уравнения. Мера седиментационной устойчивости. Факторы, влияющие на седиментационную устойчивость дисперсных систем.
- •Рассчитайте разность уровней воды в двух сообщающихся капиллярах диаметрами 0,1 и 0,3 мм при 20 ºС. Поверхностное натяжение и плотность воды составляют соответственно 72,75 мДж/м2 и 0,998 г/см3.
- •Экзаменационный билет № 21
- •Мономолекулярная адсорбция, форма изотермы адсорбции, уравнение Генри. Основные положения теории Ленгмюра, вывод уравнения и его анализ, линейная форма уравнения Ленгмюра.
- •Строение двойного электрического слоя (дэс) по теории Штерна, перезарядка поверхности. Примеры образования дэс, строение мицеллы.
- •Экзаменационный билет № 22
- •Лиофильные дисперсные системы. Классификация и общая характеристика пав. Термодинамика и механизм мицеллообразования. Строение мицелл пав в водных и углеводородных средах. Солюбилизация.
- •Экзаменационный билет № 23
- •Рассчитайте работу адгезии и коэффициент растекания для системы вода-графит, если известно, что краевой угол равен 90 º, а поверхностное наятжение воды 72 мДж/м2.
- •Экзаменационный билет № 24
- •Лиофильные дисперсные системы. Истинно растворимые и коллоидные пав, их классификация. Мицеллообразование, строение мицелл, методы определения ккм. Факторы, влияющие на ккм.
- •Экзаменационный билет № 25
- •Потенциальная теория адсорбции Поляни. Десорбционный потенциал. Характеристическая кривая адсорбции. Температурная инвариантность и афинность характеристических кривых.
- •Экзаменационный билет № 26
- •Экзаменационный билет № 27
Экзаменационный билет № 6
Влияние дисперсности на термодинамическую реакционную способность. Вывод уравнения капиллярной конденсации Кельвина. Влияние дисперсности на растворимость, константу равновесия химической реакции и температуру фазового перехода.
Термодинамическая реакционная способность характеризует способность вещества переходить в какое-либо иное состояние, например переходить в другую фазу, вступать в химическую реакцию. Она указывает на удаленность данного состояния вешества или системы компонентов от равновесного состояния при определенных условиях. Термодинамическая реакционная способность определяется химическим сродством, которое можно выразить изменением энергии Гиббса или разностью химических потенциалов.
Реакционная способность зависит от степени дисперсности вещества, изменение которой может приводить к сдвигу фазового или химического равновесия.
Соответствующее приращение энергии Гиббса dGд (благодаря изменению дисперсности) можно представить в виде объединенного уравнения первого и второго начал термодинамики:
![]()
Для индивидуального
вещества V=Vм
и при Т=const
имеем:![]()
Подставляя в это
уравнение соотношение Лапласа, получим:![]()
для сферической
кривизны:![]()
Если рассматривается
переход вещества из конденсированной
фазы в газообразную, то энергию Гиббса
можно выразить через давление пара,
приняв его за идеальный. Дополнительное
изменение энергии Гиббса, связанное с
изменением дисперсности, составляет:![]()
Подставляя данное выражение, получим:
![]()
Полученное соотношение называется уравнением Кельвина (уравнение капиллярной конденсации).
Для неэлектролитов его можно записать следующим образом:
![]()
Из этого уравнения видно, что с увеличением дисперсности растворимость растет, или химический потенциал частиц дисперсной системы больше, чем у крупной частицы, на величину 2σV/r.
Степень дисперсности может влиять также на равновесие химической реакции:
![]()
С увеличением дисперсности повышается активность компонентов, а в соответствии с этим изменяется константа химического равновесия в ту или другую сторону, в зависимости от степени дисперсности исходных веществ и продуктов реакции.
С изменением дисперсности веществ изменяется температура фазового перехода.
Количественная взаимосвязь между температурой фазового перехода и дисперсностью вытекает из термодинамических соотношений.
Для фазового
перехода:![]() ,
,![]()
Для сферических
частиц:
![]()
Видно, что с уменьшением размера частиц г температуры плавления и испарения вещества уменьшаются (Hф.п.>0).
Природа броуновского движения. Понятие и определение среднеквадратичного сдвига по выбранному направлению. Взаимосвязь между среднеквадратичным сдвигом и коэффициентом диффузии (ввод уравнения Эйнштейна-Смолуховского).
Основой доказательства теплового молекулярного движения в телах явилось обнаруженное английским ботаником Робертом Броуном в 1827 г. с помощью микроскопа непрерывное движете очень мелких частичек — спор папоротника (цветочной пыльцы), взвешенных в воде. Более крупные частицы находились в состоянии постоянного колебания около положения равновесия. Колебания и перемещения частиц ускорялись с уменьшением их размера и повышением температуры и не были связаны с какими-либо внешними механическими воздействиями.
Теоретически обоснованная интерпретация броуновского движения — участие частиц дисперсной фазы ультрамикрогетерогенных систем в тепловом движении — была дана независимо друг от друга Эйнштейнии (1905 г.) и Смолуховским (1906 г.).
Проведенными исследованиями была окончательно доказана природа броуновского движения. Молекулы среды (жидкости или газа) сталкиваются с частицей дисперсной фазы, в результате чего она получает огромное число ударов со всех сторон.
Э йнштейн
и Смолуховский для количественного
выражения броуновского движения частиц
ввели представление о среднем сдвиге
частицы. Если при наблюдении движения
частицы золя под микроскопом через
определенные равные промежутки времени
отмечать ее местонахождение, то можно
получить ее траекторию движения. Так
как движение происходит в трехмерном
пространстве, то квадрат среднего
расстояния, проходимого частицей за
любой промежуток времени, равен
йнштейн
и Смолуховский для количественного
выражения броуновского движения частиц
ввели представление о среднем сдвиге
частицы. Если при наблюдении движения
частицы золя под микроскопом через
определенные равные промежутки времени
отмечать ее местонахождение, то можно
получить ее траекторию движения. Так
как движение происходит в трехмерном
пространстве, то квадрат среднего
расстояния, проходимого частицей за
любой промежуток времени, равен
![]() .
.
Под микроскопам
наблюдают проекцию смещения частицы
на плоскость за какое-то время, поэтому
![]() .
.
При равновероятных
отклонениях частицы ее направление
будет находиться между направлениями
x
и у, т. е. под углом 45° к каждой координате.
Отсюда
![]() или
или
![]() .
.
Из-за равновероятных отклонений среднеарифметическое значение сдвигов равно нулю. Поэтому используются среднеквадратичные расстояния, проходимые частицей:
![]()
Эйнштейн и Смолуховский, постулируя единство природы броуновского движения и теплового движения, установили количественную связь между средним сдвигом частицы (называемым иногда амплитудой смещения) и коэффициентом диффузии D.
Если броуновское движение является следствием теплового движения молекул среды, то можно говорить о тепловом движении частиц дисперсной фазы. Это означает, что дисперсная фаза, представляющая собой совокупность числа частиц, должна подчиняться тем же статистическим законам молекулярно-кинетической теории, приложимым к газам или растворам.
Д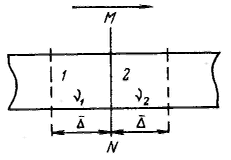 ля
установления связи между средним сдвигом
(смещением) частицы и коэффициентом
диффузии представим себе трубку с
поперечным сечением S,
наполненную золем, концентрация частиц
которого уменьшается слева направо. В
этом же направлении протекает и диффузия
частиц золя (на рисуике отмечено
стрелкой). Выделим по обе стороны от
линии MN
два малых участка 1 и 2, размеры которых
в направлении диффузии равны Δ
— среднему квадратичному сдвигу за
время τ. Обозначим частичную концентрацию
золя в объемах этих участков соответственно
через ν1
и ν2
(ν1>ν2).
Хаотичность теплового движения приводит
к равной вероятности переноса дисперсной
фазы из обоих объемов вправо и влево от
линии MN:
половина частиц переместится вправо,
а другая половина — влево. Количество
дисперсной фазы за время τ
переместится из объема 1 вправо:
ля
установления связи между средним сдвигом
(смещением) частицы и коэффициентом
диффузии представим себе трубку с
поперечным сечением S,
наполненную золем, концентрация частиц
которого уменьшается слева направо. В
этом же направлении протекает и диффузия
частиц золя (на рисуике отмечено
стрелкой). Выделим по обе стороны от
линии MN
два малых участка 1 и 2, размеры которых
в направлении диффузии равны Δ
— среднему квадратичному сдвигу за
время τ. Обозначим частичную концентрацию
золя в объемах этих участков соответственно
через ν1
и ν2
(ν1>ν2).
Хаотичность теплового движения приводит
к равной вероятности переноса дисперсной
фазы из обоих объемов вправо и влево от
линии MN:
половина частиц переместится вправо,
а другая половина — влево. Количество
дисперсной фазы за время τ
переместится из объема 1 вправо:
![]() ,
а из объема 2 влево
(в обратном направлении):
,
а из объема 2 влево
(в обратном направлении):![]() .
.
Так как |Q1|
> |Q2|
(ν1>ν2),
то суммарное количество перенесенного
вещества через плоскость MN
вправо определится соотношением
![]() .
.
Градиент концентрации по расстоянию в направлении диффузии можно выразить так:
![]()
Подставляя, получим:
![]()
Сравнивая это
соотношение с первым законом диффузии
Фика:
![]() ,
окончательно
имеем:
,
окончательно
имеем:
![]()
Это уравнение выражает закон Эйнштейна — Смолуховского, в соответствии с которым квадрат среднего сдвига пропорционален коэффициенту диффузии н времени.
Для отрицательно заряженного гидрозоля Al2S3, порог коагуляции при добавленном КСl равен 49 ммоль/л. Используя закон Дерягина, рассчитайте пороги коагуляции для таких электролитов как Na2SO4, MgCl2 и AlCl3.

