
- •Учебно-методическое пособие для выполнения лабораторно-практических работ по дисциплине: «Ветеринарная вирусология».
- •Раздел I. Общая вирусология
- •Ведение
- •Раздел I. Общая вирусология
- •Тема 1. Правила работы с вируссодержащими материалами. Устройство вирусологической лаборатории
- •Методика проведения занятия и методические указания по теме
- •1.1 Техника безопасности и правила работы с вируссодержащим материалом
- •1.2 Требования к рабочим помещениям и обеспечение условий работы
- •1.3 Хранение вирусов и других материалов, учет и этикетировка их в лаборатории.
- •1.4 Основные методы консервации вирусов
- •Тема 2. Получение, транспортировка и подготовка патологического материала для вирусологических исследований.
- •Методика проведения занятия и методические указания по теме
- •2.1 Получение и обработка патологического материала
- •2.2 Получение патологоанатомического материала
- •2.3 Получение проб для гистологического исследования.
- •2.4 Транспортировка и хранение проб.
- •Тема 3. Индикация вирусов в патологическом материале по обнаружению вирионов и вирусных телец-включений
- •Методика проведения занятия и методические указания по теме
- •Тема 4. Использование лабораторных животных в диагностических исследованиях. Цели использования лабораторных животных в вирусологии
- •Методика проведения занятия и методические указания по теме
- •Тема 5. Использование лабораторных животных в диагностических исследованиях. Биопроба
- •Методика проведения занятия и методические указания по теме
- •Тема 6. Использование лабораторных животных в диагностических исследованиях. Вскрытие лабораторных животных
- •Методика проведения занятия и методические указания по теме
- •Тема 7. Использование в вирусологии куриных эмбрионов. Культивирование вирусов на куриных эмбрионах
- •Тема 8. Использование в вирусологии куриных эмбрионов. Заражение куриных эмбрионов
- •8.1 Методы экспериментального заражения куриных эмбрионов.
- •Тема 9. Использование в вирусологии куриных эмбрионов. Вскрытие куриного эмбриона и получение вируссодержащего материала. Индикация вирусов
- •9.2 Определение гемагглютинирующих свойств вирусов.
- •Тема 10. Использование в вирусологии культур клеток. Типы культур клеток
- •Тема 11. Использование в вирусологии культур клеток. Культивирование вирусов в культуре клеток
- •Тема 12. Использование в вирусологии культур клеток. Заражение культур клеток. Индикация вируса
- •Методика проведения занятия и методические указания по теме.
- •Тема 13. Титрование антител к вирусам в реакции торможения (задержки) гемагглютинации (ртга, рзга)
- •Методика проведения занятия и методические указания по теме.
- •Тема 14. Использование в вирусологии реакции непрямой гемагглютинации
- •Методика проведения занятия и методические указания по теме.
- •Тема 15. Использование в вирусологии реакции диффузной преципитации в агаровом геле
- •Методика проведения занятия и методические указания по теме.
- •15.2 Основные задачи рдп:
- •Тема 16. Титрование вирусов
- •Методика проведения занятия и методические указания по теме.
- •Библиографический список
- •Оглавление:
- •Раздел I. Общая вирусология
Тема 5. Использование лабораторных животных в диагностических исследованиях. Биопроба
Цель занятия: ознакомить студентов с методами фиксации и заражения лабораторных животных.
Оборудование и материалы: набор инструментов в стерилизаторе (ножницы, иглы, шприцы, пинцеты, корнцанги), лабораторные животные, суспензии вирусов эктромелии и осповакцины, ватные спиртовые тампоны краски для мечения, эфир, ксилол, мультимедийное оборудование, плакаты и презентации MS Office Power Point по теме занятия.
Методика проведения занятия и методические указания по теме
Объяснение преподавателя: Для снижения естественной резистентности животных перед заражением их можно облучать рентгеновскими лучами (мышей – 300 Р, морских свинок – 250 – 300, белых крыс – 120, кроликов – 600 Р) или обрабатывать кортизоном (5–10 мг/кг). Все эти приемы ускоряют репродукцию вируса в организме и облегчают его выделение и типирование.
Демонстрация: а) приемов обращения со стерилизованными инструментами, подготовки шприца и его наполнения инфекционным материалом; б) приемов фиксации животных; в) методов экспериментального заражения кроликов и белых мышей.
5.1 Методы экспериментального заражения лабораторных животных. Вируссодержащий материал может быть введен лабораторным животным различными методами. Наиболее часто используются (п/к (в/м), внутрибрюшинное (в/б), внутривенное (в/в), интраназальное (и/н), интрацеребральное (и/ц). Однако в каждом конкретном случае исследователь стоит перед выбором введения материала каким-то одним способом.
Волосы удаляют сульфгидратом кальция, сульфитом стронция или специальным средством по прописи Barium sulforatum – 25,0, Zincum oxydaturn – 12,5, Amylum – 12,5 Депиляторное средство перемешивают с водой до образования кашицы, которую наносят деревянной лопаточкой на нужное место, оставляют на несколько минут и затем тщательно смывают. После этого кожу смазывают вазелином.
Для наркоза мышей, хомяков, хорьков, кроликов и морских свинок используют эфир и хлороформ, для крыс и собак – эфир, для кур предпочитают применять хлороформ
Выбор метода заражения определяется тропизмом вируса. Под тропизмом вируса понимают способность его репродуцироваться в определенных типах клеток организма. Вирусы, репродуцирующиеся в нервных клетках, называются нейротропными (например, вирус бешенства), репродуцирующиеся в клетках кожи – дермотропными (например, вирус оспы), в клетках легких – пневмотропными (вирус гриппа). Вирусы, способные репродуцироваться в нескольких типах клеток, называются политропными (вирус инфекционного ринотрахеита крупного рогатого скота в клетках органов дыхания и размножения), а во всех типах клеток – пантропными (вирус чумы собак).
Зная тропизм вируса, материал вводят в органы, содержащие чувствительные к этому вирусу клетки. Например, вирус гриппа вводят интраназально, вирус оспы – внутрикожно, вирус бешенства – интрацеребрально. Пантропные вирусы лучше разносятся по организму при введении их внутривенно или внутрибрюшинно. Если же исследователь не имеет данных о тропизме находящегося в материале вируса, то заражают животных нескольких групп разными методами.
5.2 Способы фиксации и техника заражения лабораторных животных. Способы фиксации и техника заражения тем или другим методом также различны для животных разных видов. Кроликов удерживают за кожу спины ближе к лопаткам, а другой рукой придерживают за заднюю часть тела. Такая фиксация предотвращает получение царапин. Морских свинок держат одной рукой за грудь, а другой – за задние лапы. Крыс и мышей берут за хвост, дают им возможность уцепиться передними конечностями за металлическую сетку (например, клетки), захватывают двумя пальцами левой руки кожу на затылке и слегка растягивают животное. При этом крыс прочнее и безопаснее фиксировать корнцангами, а для большей надежности голову животного можно удерживать двумя корнцангами за щечные кожные складки. Оба этих корнцанга помощник держит в левой руке, а корнцанг, фиксирующий хвост, – в правой.
Белых мышей без помощника фиксируют, захватывая складку кожи между ушами пинцетом Пеано, который, в свою очередь, укрепляют, набрасывая его кольца на держатели штатива Бунзена или, что еще проще, на стоящую в обычном штативе пробирку. Возможна фиксация мышей и одной рукой.
Перед заражением место введения материала тщательно обрабатывают 3%-ным спиртовым раствором йода.
Смонтировав шприц и укрепив на нем инъекционную иглу, набирают вируссодержащий материал так, чтобы во флакон или пробирку была введена только игла, но не цилиндр шприца.
От попавшего с набираемым в шприц материалом воздуха освобождаются, повернув шприц вертикально вверх иглой, которая предварительно воткнута в толщу стерильного комочка ваты, упакованного в сложенный по типу конверта небольшой лист пергаментной бумаги. Иглу вкалывают в толщу ватика через складки бумаги, где ее не касались руками. Ватики предотвращают потерю капель вируссодержащего материала из шприца, т. е. распространение вируса в окружающей среде. Кроме того, игла, находясь в ватике, до момента инъекции остается стерильной.
Заражение через пищеварительный тракт представляет значительный интерес для выяснения патогенеза болезней, передающихся алиментарным путем (кишечные вирусные инфекции).
В зависимости от поставленной задачи животных заражают per os, в желудок и ректально.
Per os – вируссодержащий материал вводят с пищей, а также с помощью тупой иглы, не прикасаясь к слизистым оболочкам, по нескольку капель в один прием. Через несколько минут процедуру повторяют. В желудок инфекционный материал вводят с помощью зонда или желатиновых капсул, содержащих исследуемую суспензию. Ректально заражают путем введения вирусного материала, суспендированного в физиологическом растворе, имеющем температуру тела. при помощи клизмы. Анальное отверстие заклеивают лейкопластырем, создавая копростаз, что ускоряет проникновение в организм заразного начала.
Подкожное заражение. Кожную складку, захваченную большим и указательным пальцами левой руки, приподнимают и в ее основание параллельно поверхности тела вводят иглу со шприцем. Местом инъекции, как правило, у большинства животных является область спины, бока, плеча, лопатки и реже боковой стенки грудной клетки (собака), коленной складки (морская свинка), шеи (куры).
Внутрикожное заражение. Для заражения этим методом у кроликов на боку или животе выстригают, а затем выбривают шерсть на участке кожи. Подготовленное поле протирают спиртом и физраствором. Иглу шприца скосом наружу вводят под острым углом в толщу поверхностного слоя кожи на несколько миллиметров. Материал инъецируют до приподнимания слоя кожи в виде бугорка.
Мелким лабораторным животным внутрикожно вводят материал в плантарную поверхность задней конечности, которую фиксируют, отводя ее назад и помещая на указательный палец левой руки. Правой рукой иглу со шприцем вводят в кожу в направлении от пальцев к голеностопному суставу.
Для размножения в организме дермотропных вирусов (например, возбудителей оспы) содержащий их материал втирают в скарифицированную кожу. На коже, подготовленной как и для внутрикожного заражения, делают несколько поверхностных царапин иглой или обломленной пастеровской пипеткой до появления капелек лимфы. Затем наносят материал и втирают его шпателем, стеклянной палочкой или остриженной зубной щеткой. Заражение в скарифицированную кожу у крупных животных проводят на боку или животе, у морской свинки – на плантарной поверхности ступни, у мелких животных – в области спины, у петухов – в гребень и сережки, а также в перьевые фолликулы голени сразу же после удаления перьев.
Внутримышечное заражение. Для этого способа заражения чаще всего выбирают мышцы бедра, а у кур – большую мышцу груди. Иглу после дезинфекции места инъекции вводят через кожу и подкожную клетчатку в мышцы, направляя перпендикулярно к поверхности тела. После инъекции материала иглу извлекают, место введения повторно дезинфицируют.
Внутрибрюшинное заражение. Животное при данном способе заражения фиксируют вертикально вниз головой для того, чтобы органы брюшной полости сместились к диафрагме и при введении материала игла не травмировала кишечник (рис. 9). В области паха, а у кур на середине расстояния между верхушкой грудной кости и клоаки короткую иглу вводят сквозь кожу и брюшинную стенку, направляя под углом 45° к продольной оси тела. При этом левой рукой слегка оттягивают лапу животного, создавая натяжение кожи и мышц брюшной стенки со стороны инъекции. Проникновение иглы ощущается по исчезнувшему сопротивлению брюшной стенки.
Внутривенное заражение. Важно контролировать, чтобы в вену из шприца не попали пузырьки воздуха или частицы материала, которые могут вызвать эмболию и гибель животного.
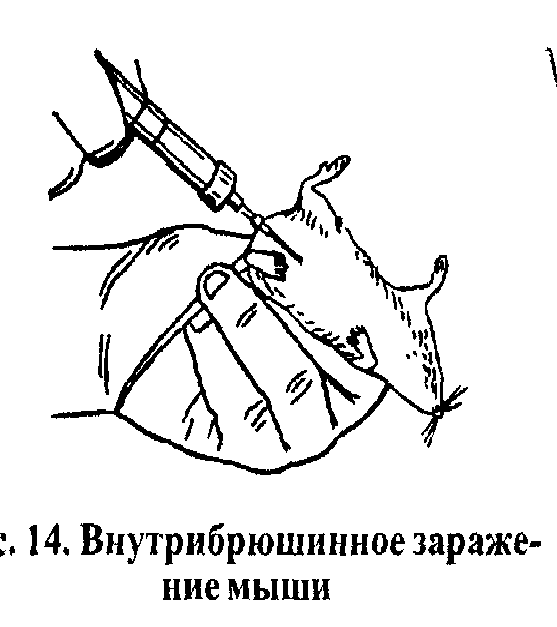
Рисунок 9 Внутрибрюшинное заражение мыши
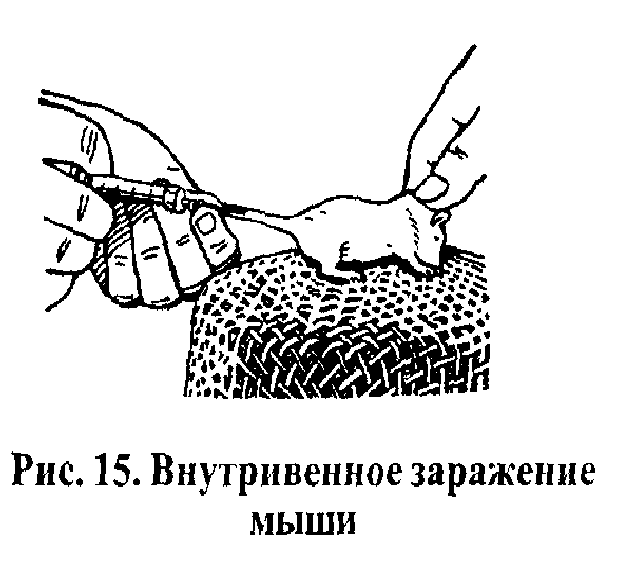
Рисунок 10. Внутривенное заражение мыши
Белых мышей и крыс заражают в боковые вены хвоста, предварительно расширив их, растирая тампоном, смоченным ксилолом или горячей водой. Помощник левой рукой сдавливает хвост у корня, а правой фиксирует животное за кожу затылка (рис.10). Иглу скосом наружу вводят под острым углом в вену нижней трети хвоста, где кожа тоньше, и направляют к корню хвоста. Если игла попала в сосуд, то жидкость легко поступает из шприца, а сосуд на всем протяжении бледнеет.
Освободив вену у корня хвоста, медленно вводят материал. Затем вену передавливают ниже места вкола, иглу извлекают и место инъекции прижимают сухой ватой.
Морским свинкам можно ввести вирус в ток крови, только проникнув иглой в сердце. Для этого определяют место сердечного толчка, в межреберный промежуток слева и на 1 см выше мечевидного отростка вводят иглу без шприца. Если в игле покажется кровь, значит, игла попала в сердце, и тогда, присоединив шприц, инъецируют материал.
Кроликам внутривенно материал вводят в краевую вену уха, предварительно удалив волосы на месте инъекции и пережав сосуд ниже вкола иглы. Игла должна быть направлена по ходу тока крови, т.е. к голове.
Птице вируссодержащий материал вводят в подкрыльцовую вену.
Интраназальное заражение. Большинство лабораторных животных (за исключением кроликов) при закапывании материала в ноздри чихают и разбрызгивают вируссодержащую суспензию. Поэтому перед интраназальным заражением животным делают глубокий эфирный наркоз. Для этого помещают их в банку с крышкой и кусочком смоченной эфиром ваты. Заснувших животных извлекают, фиксируют вверх ноздрями. Материал по каплям вводят в ноздри, и с вдыхаемым воздухом он втягивается внутрь.
Кроликам же вируссодержащую суспензию можно закапывать в ноздри по каплям при запрокинутой на спину голове без наркоза.

Рисунок 11. Интрацеребральное заражение кролика
Интрацеребральное заражение. Кожу головы мышат большим и указательным пальцами левой руки оттягивают к затылку. Иглой шприца с ограничителем прокалывают кожу и череп на глубину 1–2 мм в точке, лежащей в центре квадрата, образованного средней сагиттальной линией и перпендикуляром к ней, проходящим по наружному краю глазниц.
Белых крыс интрацеребрально заражают через трепанационное отверстие, а молодых кроликов и морских свинок – прокалывая кости черепа в надглазничной борозде, где кость довольно тонкая. Иглу используют с ограничителем, обеспечивающим проникновение иглы не более чем на 4–5 мм. Старых животных интрацеребрально заражают через трепанационное отверстие (рис. 11).
Объем заражающей дозы материала значительно варьирует в зависимости от метода внесения и вида животных (табл. 4).
Таблица 4
Максимальные объемы вводимого материала для лабораторных
|
Метод заражения |
Кролики |
Морские свинки |
Белые крысы |
Белые мыши |
|
Внутрикожный |
0,1 |
0,1 |
0,05 |
0,02 |
|
Подкожный |
5,0 |
3,0 |
3,0 |
0,5 |
|
Внутримышечный |
5,0 |
2,0 |
1,0 |
0,3 |
|
Внутрибрюшинный |
10,0 |
5,0 |
2,0 |
1,0 |
|
Внутривенный |
5,0 |
2,0 |
2,0 |
1,0 |
|
Интраназанальный |
1,0 |
0,3 |
0,1 |
0,03 |
|
Интрацеребральный |
0,3 |
0,05 |
0,03 |
0,02 |
5.3 Содержание лабораторных животных после заражения. После заражения животные должны быть помещены в клетки, на которые навешивают этикетки с указанием вируса или номера экспертизы исследуемого материала, количества и номеров зараженных животных, даты заражения. В рабочем журнале записывают название вируса или номер экспертизы исследуемого материала, количество и характеристику зараженных животных, их маркировку, метод введения и дозу вируса.
За животными устанавливают наблюдение, обращая внимание на их внешний вид, подвижность, прием корма и т. п. Следует отметить, что гибель животных в первые дни после заражения может быть связана с травмой или токсическим действием исследуемого материала.
Задания
1. Отработка приемов фиксации и экспериментального заражения лабораторных животных всеми методами.
2. Заражение внутрикожно белых мышей вирусом эктромелии и кроликов вирусом осповакцины.
Самостоятельная работа студентов
Студенты отрабатывают приемы фиксации и экспериментального заражения лабораторных животных всеми методами.
Подведение итогов занятия
Задание к следующему занятию
Контрольные вопросы:
1. С какой целью используют лабораторных животных в вирусологических исследованиях.
2. Требования, предъявляемые к лабораторным животным, уход, содержание.
3. Животные - гнотобиоты. СПФ - животные .
4. Методы заражения лабораторных животных.
