
- •Лабораторная работа №1 «Приготовление катализатора методом пропитки»
- •1.Теоретическая часть
- •1.1 Общие сведения о катализаторах.
- •1.2. Катализаторы на носителях, получаемые методом пропитки
- •2.Экспериментальная часть
- •2.1 Выбираем и подготавливаем исходные реагенты.
- •2.2 Рассчитаем объёмы концентрации рабочих растворов.
- •3. Получение материала с заданными характеристиками ( получение активных композиций).
- •3.1 Ход работы
- •3.2 Выбор режима сушки и активации катализатора.
- •3.3 Под микроскопом
- •Лабораторная работа №2 «Приготовление катализатора методом осаждения»
- •Теоретическая часть
- •Приготовление катализаторов методом осаждения
- •2.Экспериментальная часть
- •2.1 Выбираем и подготавливаем исходные реагенты.
- •2.2 Рассчитаем объёмы концентрации рабочих растворов.
- •3. Получение материала с заданными характеристиками ( получение активных композиций).
- •3.1 Ход работы
- •4.Перерабатываем синтезированный материал в товарный продукт.
- •5. Выбор режима сушки и активации катализатора.
2.Экспериментальная часть
Цель: разработать технологию приготовления катализатора методом осаждения растворимых солей меди. Также рассчитать объемы и концентрации рабочих растворов; выбрать режим осаждения; выбрать режим сушки и активации катализатора; предложить область применения.
-
Приборы и реактивы: диатамитовый порошок, кальцинированная сода,
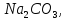 CuHS
CuHS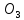 *5
*5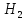 O,
O, *
*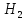 O,
цемент, колба, пипетка, фарфоровая
чашка, водяная баня, мерный цилиндр,
сушильный шкаф, микроскоп, муфельная
печь, термометр, воронка Бюхнера,
лакмусовая бумажка, весы электронные.
O,
цемент, колба, пипетка, фарфоровая
чашка, водяная баня, мерный цилиндр,
сушильный шкаф, микроскоп, муфельная
печь, термометр, воронка Бюхнера,
лакмусовая бумажка, весы электронные.
Дано:
1. В
качестве носителя использовать
диатамитовый порошок. Осаждение
производить кальценированной содой
переводя растворимые соли в нерастворимые
карбонаты.
Количество
носителя 10
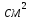 ,
,
-
В составе готового катализатора содержание оксида меди – 10% масс.
Исходное сырьё: 1. Диатамитовый порошок ( ТУ – 10-05031531-378-94)
2.Кальцинированная сода
-
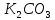 *
*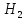 O
O -
Цемент
-
CuHS
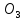 *5
*5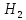 O
O -
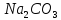
Ход работы состоит из трёх этапов: 1. Выбираем и подготавливаем исходные реагенты. 2. Получаем материал с заданными характеристиками. 3. Перерабатываем синтезированный материал в товарный продукт.
А процесс осаждения включает: 1. Получение осадка. 2. Промывка осадка. 3. Сушка осадка. 4. Прокалка осадка. 5. Активация осадка.
2.1 Выбираем и подготавливаем исходные реагенты.
В
качестве исходных материалов выбираем
диатамитовый порошок. Так как катализатор
нужно получить методом осаждения, то в
качестве осадителя выбираем кальценированную
соду, так как её физическая способность
позволяет перевести растворимые соли
в нерастворимые карбонаты. Физические
свойства носителя:
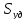 = 30
= 30
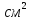 /
г.; рН водн. Вытяжки: 6÷8.
/
г.; рН водн. Вытяжки: 6÷8.
Объёмная
насыпная масса: 400 кг/
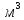 .
.
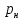 =
400 кг/
=
400 кг/
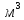 = 0.4 г/
= 0.4 г/
 .
.
2.2 Рассчитаем объёмы концентрации рабочих растворов.
1.
Определяем массу носителя CuHS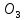 *5
*5 O
через массу меди:
O
через массу меди:
М
(CuHS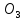 *5
*5 O)
= 63.5+1+32+3*16+5*2+16=234.5 г/моль;
O)
= 63.5+1+32+3*16+5*2+16=234.5 г/моль;
М (Сu) = 63/5 г/моль;
m(Cu)
=
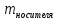 *W
(Cu);
*W
(Cu);
 =
V*
=
V* =
10*0,4 = 4 г.
=
10*0,4 = 4 г.
m(Cu) = 4*0.1 = 0.4 г.
-
 найдём
методом пропорции:
найдём
методом пропорции:
X - 0.4г
234.5 г/моль - 63.5 г/моль
X=
 =
1.64 г.
=
1.64 г.
-
Рассчитаем необходимый объём воды:
Для
этого возьмём 20% раствора CuHS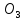 следовательно
следовательно
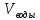 =
=
 =
=
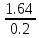 =
8.2 мл.
=
8.2 мл.
3. Получение материала с заданными характеристиками ( получение активных композиций).
3.1 Ход работы
Для
начала рассмотрим диатамитовый порошок
под микроскопом. Носитель имеет зерна
бежевого цвета. Исходя из расчетных
данных берём 8.2 мл. воды и приливаем к
1.64 г
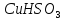 .
Полученную смесь подогреваем на водяной
бане. Затем берём 4 г. Носителя, количество
которого рассчитали выше, и добавляем
его к смеси, которая стоит на водяной
бане. Полученная смесь приобрела
темно-зеленый цвет.
.
Полученную смесь подогреваем на водяной
бане. Затем берём 4 г. Носителя, количество
которого рассчитали выше, и добавляем
его к смеси, которая стоит на водяной
бане. Полученная смесь приобрела
темно-зеленый цвет.
Параллельно на водяную баню ставим смесь соды и воды. Произвольно выбираем массу соды 1.5 г. Теперь произведём расчёт необходимого объёма воды: так как 10% раствор соды, то масса раствора равна 15 г.. Значит объём воды равен:
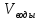 =
=
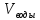 =
=
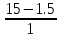 =
13.5 мл.
=
13.5 мл.
Теперь
смешиваем соду и воду и ставим на водяную
баню. При 70°С сода полностью растворилась
в воде. Данную смесь приливаем к раствору
диатамитового порошка и CuHS *5
*5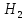 O.
После этого ждём, когда начнется
осаждение. Теперь полученную смесь
отфильтровываем на воронке Бюхнера.
Это мы делаем до тех пор, пока рН осадка
нестанет равен 7. Для получения рН = 7,
нам потребовалось четыре раза
профильтровать на воронке Бюхнера.
Результаты приведены в таблице 1
O.
После этого ждём, когда начнется
осаждение. Теперь полученную смесь
отфильтровываем на воронке Бюхнера.
Это мы делаем до тех пор, пока рН осадка
нестанет равен 7. Для получения рН = 7,
нам потребовалось четыре раза
профильтровать на воронке Бюхнера.
Результаты приведены в таблице 1
Таблица 1
|
Количество фильтрований |
рН |
|
1 |
9 |
|
2 |
8 |
|
3 |
8 |
|
4 |
7 |
Затем наш катализатор ставим на прокалку в муфельную печь и вытаскиваем его спустя 30 мин. Прокалку ведём при 250 °С. Затем взвешиваем наш катализатор вместе с керамической посудой на технических весах. m= 84.8 г. Масса самой керамической посуды = 69.7г. В итоге масса катализатора = 84.8 – 69.7 = 15.1 г.
