
- •Лекція 8
- •1. Теоретичні основи спектроскопічних методів
- •1. Теоретичні основи спектроскопічних методів
- •2. Класифікація спектроскопічних методів
- •3. Короткі відомості про методи атомної спектроскопії
- •3.1. Загальні відомості про атомні спектри
- •3.2. Атомно-емісійна спектроскопія
- •3.3. Атомно-абсорбційна спектроскопія
- •Атомно-абсорбційні спектрометри складаються з атомізатора, джерела випромінювання, монохроматора, приймача випромінювання й детектора.
3. Короткі відомості про методи атомної спектроскопії
3.1. Загальні відомості про атомні спектри
Атом одноразово може поглинути або випустити тільки певну кількість енергії, тобто він може перебувати тільки в певних енергетичних станах. Речовина складається з безлічі атомів, здатних переходити на різні енергетичні рівні, випускаючи або поглинаючи фотони різних частот.
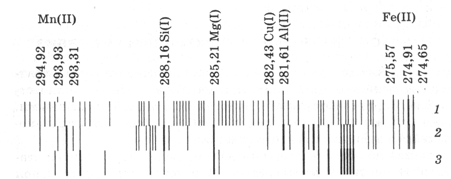
Рис.1. Області спектра заліза (1), магнію (3), алюмінієво-магнієвого сплаву (2)
Сукупність фотонів однакової частоти становить спектральну лінію. Якщо фотони поглинаються, ці лінії утворюють спектр поглинання (абсорбційний спектр), якщо фотони випускаються (піддаються емісії) − виходить емісійний спектр. Емісія − самовільний процес, тому що атом завжди прагнути перейти в стабільний стан з найменьшою енергією. Поглинання − завжди примусовий процес, який збільшує енергію атома.
Абсорбційний спектр одержують, поміщаючи досліджувану речовину в поле електромагнітного випромінювання (наприклад, на шляху світлового потоку).
Для одержання емісійного спектра атоми речовини попередньо переводять у збуджений стан підведенням якого-небудь виду енергії (теплової, хімічної та ін.); далі атоми повертаються в основний стан, випускаючи фотони або теплоту.
Енергія атомних орбіталей сильно відрізняється. Так, для збудження електрона з найближчої до ядра орбіталі потрібно більше 104 кДж/моль (частота рентгенівського випромінювання), а для зхбудження зовнішніх електронів досить 150–600 кДж/моль (випромінювання УФ і видимої області). Із збільшенням відстані від ядра, енергія атомізації різко зменшуються. Найбільш імовірні переходи з першого збудженого рівня на основний, які називаються резонансними.
Енергія атомізації для різних елементів різна. Так, у лужних металів для одержання резонансних ліній потрібно 2 еВ (видима область), у неметалів ця енергія значно більше (5 еВ, ближня УФ область). Чим більше зовнішніх електронів, тим більше спектральних ліній, тому спектри перехідних металів складаються з тисяч ліній, спектри лужних металів мають їх значно менше.
Електронні переходи не рівноймовірні, що зумовлено квантово-механічними причинами. Так, дозволені переходи, коли енергії переходу електрона й енергії фотона, що поглинається, рівні; заборонені переходи більше одного електрона в атомі, зі зміною спина, зі зміною орбітального квантового числа більш ніж на одиницю (можливі s p, p d та ін.) тощо.
Інтенсивність емісійних ліній пропорційна частоті, числу емісійних фотонів і числу дозволених переходів.
Інтенсивність абсорбційних ліній пропорційна частоті й імовірності поглинання фотонів і числу поглинаючих атомів.
3.2. Атомно-емісійна спектроскопія
Загальні відомості
Метод атомно-емісійної спектроскопії (АЕС) заснований на емісії квантів електромагнітного випромінювання збудженими атомами. Загальну схему емісії можна представити так:
А + Е А* А + h.
Енергія атомізації повинна бути менше енергії іонізації атома, інакше в результаті будуть утворюватися іони, а не збуджені атоми. Атомізація вільних атомів відбувається при зіткненнях із частками плазми, дуги або іскри з великою кінетичною енергією. При поглинанні атомами енергії 100–600 кДж/моль–1 зовнішній електрон переходить на одну з збуджених орбіталей і через 10–8 сек вертається на основний або який-небудь інший рівень. При цьому енергія виділяється у вигляді кванта світла h або у вигляді теплоти (безвипромінювальний перехід).
На відміну від молекул, в атомі можливі тільки електронні переходи, різниця енергій яких досить велика, тому емісійний атомний спектр складається з окремих ліній. Речовини, що важко піддаються атомізації (наприклад, N2), частково залишаються у вигляді молекул і утворюють смугасті спектри (мал. 2).
Р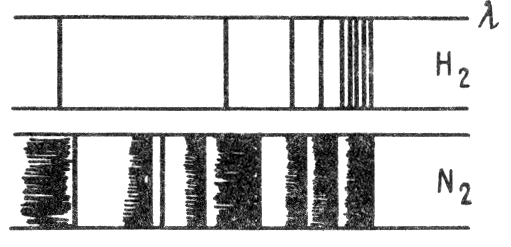 ис.2.
Лінійчатий спектр водню й смугастий
спектр азоту
ис.2.
Лінійчатий спектр водню й смугастий
спектр азоту
Інтенсивність випромінювання І залежить від числа збуджених атомів і ймовірності електронних переходів у них. Найбільш імовірні та інтенсивні резонансні переходи, яким відповідаюь чітки резонансні лінії, тому їх найчастіше використовують в аналітичній хімії. Інтенсивність випущення прямо пропорційна концентрації певних атомів у пробі І = аС, і може бути використана для визначення С. Коефіцієнт а залежить від умов процесу, тому в АЕС вирішальне значення має правильний вибір умов атомізації й виміру сигналу. У реальних умовах ця залежність часто уксладнюється через різноманітні побічні ефекти оптичної й фізико-хімічної природи.
Будова атомно-емісійних спектрометрів
Атомно-емісійні спектрометри складаються з атомізаторів і джерел збудження, монохроматорів, приймача випромінювання та реєструючого пристрою.
Для переводу речовини в газоподібний атомний стан (атомізації) застосовують атоміизатори, для збудження атомів − джерела збудження, які часто конструктивно об'єднані.
Типи атомізаторів наведені в табл. 3.
Таблиця 3. Основні типи атомізаторів в АЕС
|
Тип атомізатора |
Т, С |
Стан проби |
Мінімальна визначувана концентрація, Сmin, % |
Sr (стандартне відхилення) |
|
Полум'я |
1500 –3000 |
Розчин |
10–7÷10–2 |
0,01÷0,05 |
|
Електрична дуга |
3000–7000 |
Тверда |
10–4÷10–2 |
0,1÷0,2 |
|
Електрична іскра |
10000-12000 |
Тверда |
10–3÷10–1 |
0,05÷0,1 |
|
Індуктивно-звۥязана плазма |
6000-10000 |
Тверда |
10–8÷10–2 |
0,01÷0,05 |
Полум'я. Варіант АЕС із атомізациєю у полум'ї називають методом емісійної фотометрії полум'я. В ньому розпилену за допомогою форсунки аналізовану пробу (розчин) подають у полум'я пальника (мал. 3).
Р ис.
3. Схема
полум'яного атомізатора для атомно-емісійної
спектроскопії: 1 - полум'я; 2 - розпилена
проба; 3 - проба
ис.
3. Схема
полум'яного атомізатора для атомно-емісійної
спектроскопії: 1 - полум'я; 2 - розпилена
проба; 3 - проба
Полум'я – низькотемпературне джерело атомізації й збудження. Залежно від природи горючої суміші температура полум'я може становити від 1500 (світильний газ (СО) – повітря) до 3000 °С (С2Н2 − N2O). Такі температури використовуються для визначення легко збуджуваних елементів − лужних (Na, K) і лужно-земельних (Са, Sr, Ba) металів. Для них метод фотометрії полум'я є одним із самих чутливих (межі виявлення до 10–7 % мас). Спектр речовин, збуджених у полум'ї складається, в основному, з резонансних ліній. Важливою перевагою полум'я є висока стабільність і пов'язана з нею добра відтворюваність результатів вимірів (Sr = 0,01÷0,05).
Р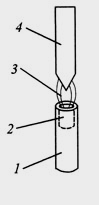 ис.4.
Схема дугового (іскрового)
атомізатора: 1 –
нижній електрод; 2
-поглиблення для проби;
3 – зона
електричного розряду; 4
-верхній електрод
ис.4.
Схема дугового (іскрового)
атомізатора: 1 –
нижній електрод; 2
-поглиблення для проби;
3 – зона
електричного розряду; 4
-верхній електрод
Електрична дуга. В АЕС використовують також дугові розряди постійного і перемінного струму. Дуговий атомізатор складається з пари електродів (найчастіше вугільних), між якими пропускають електричний розряд (мал.4). Нижній електрод має поглиблення, в яке поміщають пробу. Таким чином, дуговий розряд найбільш зручний для аналізу твердих проб. Для аналізу розчинів пробу попередньо випарюють разом з інертним порошкоподібним матеріалом (колектором), а потім поміщають у поглиблення електрода. Якщо аналізована проба − метал (сплав), то вона безпосередньо служить нижнім електродом.
Температура дугового розряду істотно вище, ніж температура полум'я (3000÷7000 °С). Таких температур достатньо для ефективної атомізації й збудження більшості елементів (крім найбільш важко збуджуваних неметалів –галогенів). Для більшості елементів межі виявлення в дуговому розряді на один-два порядка нижче, ніж у полум'ї і в середньому становлять 10–4– 10–2 % мас.
Дугові атомізатори відрізняються невисокою стабільністю роботи, тому відтворюваність результатів невелика (Sr = 0,1÷0,2). Однак для напівкількісних визначень вона достатня. Одна з найбільш важливих областей їх застосування - якісний аналіз.
Електрична іскра. Іскровий атомізатор побудований так само, як і дуговий. Для генерації дугового та іскрового розрядів використовують тіж самі пристрої, а вибір типу розряду здійснюється перемиканням електричної схеми. Іскровий атомізатор теж призначений для аналізу твердих зразків. Ефективна температура атомізації досягає 10000 °С. Цієї температури достатньо для збудження важко збуджуваних елементів (галогенів). Іскровий розряд більш стабильний, ніж дуговий, тому відтворюваність результатів вище (Sr = 0,05÷0,1).
Індуктивно
зв'язана плазма (ІЗП)
− сучасніше
джерело атомізації, що має найкращі
аналітичні показники та метрологічні
характеристики. Атомізатор з ІЗП являє
собою плазмений пальник особливої
конструкції (мал. 5), що складається із
трьох концентричних кварцових трубок.
В них з великою швидкістю подають потоки
чистого аргону. Самий внутрішній потік
служить для вприскування розчину проби,
середній є плазмоутворюючим, а зовнішній
служить для охолодження плазми; витрата
аргону в цьому потоці особливо велика
(10–20 л/хв). Аргонова плазма ініціюється
(підпалюється) іскровим розрядом, а
потім стабілізується за допомогою
високочастотної індуктивної котушки,
що оточує верхню частину пальника. При
цьому виникає сильний кільцевий струм
заряджених часток, що перебувають у
плазмі (іонів Аr+
і вільних електронів). Темп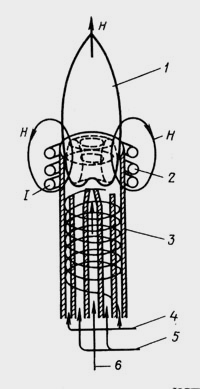 ература
аргонової плазми змінюється по висоті
пальника й становить 6000÷10000 °С.
ература
аргонової плазми змінюється по висоті
пальника й становить 6000÷10000 °С.
Рис.5. Схема атомізатора з ІЗП: 1 – зона спостереження; 2 – індукційна котушка; 3 – кварцовий пальник; 4 – потік охолодного газу; 5 – проміжний потік; 6 – внутрішній потік
Метод ІЗП-АЕС характеризується універсальністю (збуджується більшість елементів), високою чутливістю, доброю відтворюваністю й широким діапазоном визначуваних концентрацій. Основний фактор, що стримує застосування ІЗП в аналітичній практиці − висока вартість пристроїв й матеріалів, що витрачаються (аргону високої чистоти).
Для монохроматизації випромінювання застосовується оптичний вузол (вхідна щілина, конденсорні лінзи, диспергуючі призми), що поміщається між джерелом збудження та реєструючим пристроєм.
В АЕС аналітичним сигналом є випромінювання, що випускається збудженими атомами. Його сприймають візуально (спектроскопи й стилоскопи), реєструють на фотопластинці (спектрографи), перетворять в електричний сигнал за допомогою фотоелементів і фотомножників.
Достоїнствами методу АЕС є висока селективність і багатоелементність (у ряді випадків він дозволяє напівкількісно оцінити зміст близько 80 елементів), що робить його незамінним якісним методом у геології, ґрунтознавстві, біології, медицині, криміналістиці й, природно, при моніторингу об'єктів навколишнього середовища. Його використовують для визначення мікроелементів у ґрунтах і біологічних об'єктах. Емісійна полум'яна спектроскопія – зручний і швидкий метод визначення більше 40 елементів. Це найпоширеніший, чутливий і відтворюваний метод визначення лужних і лужно-земельних металів у водах, біологічних об'єктах, ґрунтах. Діапазон визначуваних вмістів для ІЗП може досягати 4–5 порядків величин концентрацій, для інших методів – 2–3 порядки. Для найбільш стабільних джерел атомізації (полум'я, ІЗП) величини Sr становлять 0,01—0,05, що є високою відтворюваністю для інструментальних методів аналізу.
Основним недоліком методу є невисока точність (погрішність перебуває в межах 10-20 %), що обмежує його застосування в кількісному аналізі.
