
- •Материаловедение
- •1. Атомно-кристаллическое строение материалов
- •1.1 Агрегатные состояния вещества
- •1.2 Аморфное и кристаллическое состояние твёрдых тел
- •1.3 Понятие кристаллической решётки
- •1.4 Структура кристаллов
- •1.5 Поликристаллическое (зернистое) строение материалов
- •1.6 Анизотропия кристаллов
- •1.7 Дефекты кристаллической структуры
- •2. Структура и свойства металлов
- •2.1 Общая характеристика и классификация металлов
- •2.2 Металлическая межатомная связь и модель «электронного газа»
- •2.3 Кристаллическая структура металлов
- •2.4 Полиморфизм металлов
- •3. Формирование микроструктуры металлов
- •3.1 Энергетические причины процесса кристаллизации
- •3.2 Кривые охлаждения металлов
- •3.3 Механизм процесса кристаллизации
- •3.4 Строение слитка металла
- •4. Деформация и механические свойства материалов
- •4.1 Упругая и пластическая деформация материалов
- •4.2 Методы механических испытаний материалов
- •4.3 Испытания материалов на одноосное растяжение. Диаграмма растяжения.
- •4.4 Механизм упругой и пластической деформации.
- •4.5 Наклёп или упрочнение металлов под воздействием
- •4.6 Возврат и рекристаллизация деформированных металлов
- •4.7 Разрушение материалов
3. Формирование микроструктуры металлов
И СПЛАВОВ ПРИ ЗАТВЕРДЕВАНИИ
Процесс перехода вещества из жидкого состояния в твёрдое кристаллическое состояние называют кристаллизацией. Обратный процесс называют плавлением. Рассмотрим подробно процесс кристаллизации металлов.
3.1 Энергетические причины процесса кристаллизации
Любую систему атомов (т.е. вещество) можно характеризовать некоторой термодинамической функцией F, которую называют свободной энергией:
F = U – T×S, (3.1)
где U – полная энергия системы атомов; T – абсолютная температура; S – энтропия системы атомов (энтропия это мера беспорядка).
Предоставленная сама себе система атомов всегда стремится в состояние с наименьшей свободной энергией. Чем меньше свободная энергии системы атомов, тем она более стабильна, более устойчива.
Как видно из формулы свободная энергия системы атомов с повышением температуры уменьшается, причём по-разному для упорядоченной и неупорядоченной системы атомов. Для неупорядоченной системы атомов, т.е. для жидкого состояния, у которого энтропия выше, уменьшение свободной энергии более стремительное, чем в случае упорядоченного, т.е. кристаллического состояния вещества (рис. 3.1.).

Рис 3.1. Зависимость свободной
энергии системы атомов
от температуры
Кр. – упорядоченная система
атомов (кристалл);
Ж. – неупорядоченная система
атомов (жидкость).













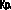

















При некоторой температуре TS наблюдается совпадение свободных энергий жидкого и кристаллического состояний вещества, т.е. пересечение графиков, отражающих изменение свободной энергии системы атомов с температурой. При температурах ниже TS меньше свободная энергия у кристаллического состояния и поэтому при таких температурах системе выгоднее находится в кристаллическом состоянии. При температурах выше TS , напротив, меньше свободная энергия у жидкого состояния, и здесь системе выгоднее быть в жидком состоянии. Таким образом, температура TS отделяет область существования жидкого и кристаллического состояний вещества. В то же время при данной температуре в реальных условиях охлаждения или нагрева не наблюдается перехода вещества из одного агрегатного состояния в другое, поскольку при этой температуре FЖ = FКр и у вещества нет никаких причин для изменения агрегатного состояния.
Температуру TS называют теоретической или иначе равновесной температурой кристаллизации (плавления) вещества. Именно эту температуру для различных веществ обычно указывают в справочниках.
Для начала процесса кристаллизации жидкого расплава необходимо охладить его до температур чуть ниже TS. Тогда FКр окажется меньше FЖ и процесс перехода вещества из жидкого состояния в кристаллическое окажется энергетически выгодным. Другими словами реальный процесс кристаллизации всегда происходит в условиях некоторого переохлаждения расплава. По тем же причинам реальный процесс плавления всегда идёт в условиях некоторого перегрева вещества.
Температуру, при которой наблюдается реальный процесс кристаллизации расплава, называют фактической температурой кристаллизации. Эта температура всегда ниже TS, в то время как фактическая температура плавления всегда выше TS. Степенью переохлаждения расплава (ΔТ) называют разницу между теоретической и фактической температурами кристаллизации. Степенью перегрева называют разницу между фактической и теоретической температурами плавления вещества. Степень переохлаждения расплава тем выше, чем ниже фактическая температура кристаллизации вещества. (На рис. 3.1 T2 T1 , поэтому ΔT2 ΔT1).
