
Лекція №5
Тема: Лікарські засоби неорганічної природи. ІV група періодичної системи. Лікарські засоби карбону та його сполук
План:
-
Загальна характеристика групи.
-
Вугілля активоване.
-
Натрію гідрокарбонат.
-
Порівняльна характеристика гідрокарбонатів і карбонатів.
-
Фактори, що впливають на стабільність натрію гідрокарбонату у водних розчинах.


До групи карбону (ІV група періодичної системи) належать п’ять елементів: карбон, силіций, германій, олово і свинець. Атоми елементів, що входять до цієї групи, мають на зовнішній електронній оболонці 4 електрони, відтак їх максимальна валентність дорівнює 4. Крім того, вони можуть утворювати 2-валентні сполуки, причому, чим вища атомна вага елементу, тим більш тривкі такі сполуки. Одночасно із збільшенням атомної ваги елементи набувають щораз виразніших металічних властивостей. Звичайно карбон і силіций відносять до неметалів, а решту елементів – до металів.
Сполуки германію не найшли застосування у лікарській справі, а сполуки олова в дуже незначній мірі.
Карбон знаходиться у природі як у вільному стані, так і у вигляді численних сполук. Сполуки карбону, так звані «органічні сполуки», ми розглянемо в наступних лекціях. До неорганічних сполук карбону відносять умовно вуглекислоту та її солі. При нагріванні органічних речовин (деревина,кістки, тощо) без доступу повітря одержують різні сорти вугілля, які характеризуються адсорбційною здатністю. Деякі види вугілля знайшли застосування як лікарські засоби.
Силіций – один із найпоширеніших у природі елементів – становить понад 25% доступної нам частини земної оболонки. Найважливішими його сполуками є кремнезем, силікати та алюмосилікати. До алюмосилікатів належить також і глина. Із сполук силіцию в аптечній практиці має скло ( склянки, ампули).
Вугілля активоване
 Carbo
activatis
Carbo
activatis
Вугілля активоване являє собою чорний порошок дуже високого ступеню дисперсності, отже має велику площу поверхні. В зв’язку з цим використовується як адсорбент. За його допомогою вилучають пари розчинників (ефір, бензол), освітлюють рослинні олії, вилучають сивушні масла.
Властивості: нерозчинний у воді і інших розчинниках легкий чорний порошок.
Ідентичність:
-
на порошок діють сірчаною кислотою, газ, що утворюється в результаті реакції, пропускають через вапняну воду, відбувається її помутніння:
C + H2SO4 = CO2 + SO2 + 2H2O
А ктивоване
вугілля, що використовується у медичній
практиці, повинно бути вільним від
наступних домішок:
ктивоване
вугілля, що використовується у медичній
практиці, повинно бути вільним від
наступних домішок:
-
сульфуру - Na2S + 2HCL = 2 NaCL + H2S
-
карбонатів - CaCO3 + 2 HCL = CO2 + H2O + CaCL2
-
цианідів - 2KCN + H2SO4 = K2SO4 + 2HCN
HCN + NaOH = NaCN + H2O
6NaCN + FeSO4 = Na4[Fe(CN)6] + Na2SO4 в присут. HCL
3Na4[Fe(CN)6] + FeCL3 = Fe4[Fe(CN)6]3 + 12NaCL
 Утворюється
берлінська лазурь синього кольору.
Утворюється
берлінська лазурь синього кольору.
-
Смоли - порошок обробляють спиртом. Фільтрат після відстоювання повинен бути чисти і безбарвним.
-
Адсорбційна здатність – до розтертого препарату додають 16 мл 0,15% розчину метиленового синього, збовтують 5 хвилин, відстоюють, фільтрують. Фільтрат повинен бути прозорим і безбарвним.
Застосування : в медичній практиці застосовують при диспепсії, метеоризмі, інтоксикаціях, отруєнні алкалоїдами, солями важких металів. Призначають всередину по 1-2 г на прийом 3-4 рази на день. Випускають в таблетках по 0,5 г.

Натрію гідрокарбонат
Natrii hydrocarbonas
NaHCO3 M.M. 83,99
 Це білий
кристалічний порошок без запаху ,
солоно-лужного смаку. Розчиняється у
віоді у співвідношенні 1:2 з рН розчинів
8,1.
Це білий
кристалічний порошок без запаху ,
солоно-лужного смаку. Розчиняється у
віоді у співвідношенні 1:2 з рН розчинів
8,1.
Препарат отримують методом Сольве:
NH3 + CO2 + H2O = NH4HCO3
NH4HCO3 + NaCL = NH4CL + NaHCO3
Отриманий продукт відфільтровують, прокалюють, при цьому утворюється
Na2CO3 , при цьому звільняються від домішки NH4CL, що є леткою сполукою. Отриманий продукт називається кальцинована сода. Після перекристалізації продукту отримують його гідрат Na2CO3.10 H2O, насичують вуглекислим газом, при цьому утворюється гідрокарбонат натрію. Препарат перекристалізовують з води, знову насичують вуглекислим газом, отримують чистий продукт, що застосовується у медицині.
Ідентичність:
-
натрій- йон: забарвлення полум’я в жовтий колір;
-
До розчину препарату додають 15% розчин K2CO3, нагрівають до кипіння, додають 4 мл розчину калію піроантимонату, знову доводять до кипіння, охолоджують у льодяній воді, при необхідності потирають стінки пробірки скляною паличкою, утворюється густий білий осад.
![]()
-
З метоксифенілоцтовою кислотою утворюється об’ємний білий кристалічний осад, що розчиняється у розчині аміаку.
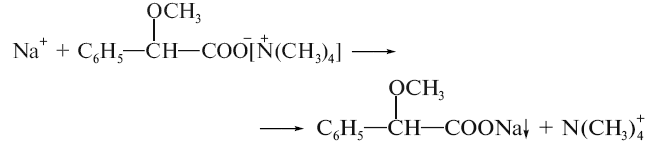
-
гідрокарбонат-йон – з хлороводневою кислотою або з розведеною оцтовою кислотою у водному розчині утворюються бульбашки вуглекислого газу:
NaHCO3 + HCL = NaCL + CO2 + H2O
Кількісне визначення: метод нейтралізації, ацидиметрія, титрований розчин 0,1М хлороводнева кислота, індикатор метиловий оранжевий, що має інтервал переходу забарвлення 3,0 (червоний) – 4,4(жовтий ). Титрування проводять до переходу забарвлення від жовтого до оранжевого. Еквівалент дорівнює молекулярній масі.
Наступною реакцією можна розрізнити гідрокарбонат і карбонат-йони: це взаємодія з насиченим розчином магнію сульфату
4MgSO4 + 4Na2CO3+ H2O = 3MgCO3 .Mg(OH)2. 3H2O + 4Na2SO4 + CO2
Гідрокарбонат утворює осад тільки при кип’ятінні.
Натрію гідрокарбонат має в розчині біль слабку лужну реакцію, ніж, карбонат, отже не має їдкої подразнюючої дії лугу на організм людини. Дія його зводиться до підвищення лужності крові, підтримання лужного резерву організму при його закисленні (ацетонемія). Нейтралізує кислоту шлункового соку, раніше випускались таблетки натрію гідрокарбонату по 0,5 г. Місцево у вигляді полоскань при запальних процесах слизових оболонок верхніх дихальних шляхів. Гідрокарбонат натрію входить до складу різноманітних лужних мінеральних вод.

