
- •Контрольні завдання
- •§ 1. Розділ 1 механіка
- •§ 1. Кінематика матеріальної точки
- •§ 2. Динаміка матеріальної точки. Закони ньютона
- •§ 3. Робота, потужність, енергія
- •§ 4. Сили в механіці і сили інерції.
- •§ 5. Динаміка обертального руху твердого тіла.
- •Умови рівноваги твердого тіла
- •§ 6. Гравітація. Елементи теорії поля.
- •Напруженість гравітаційного поля тіла масою
- •§ 7. Механіка рідин 1 газів
- •§ 8. Елементи спеціальної теорії відносності
- •§ 12, 13. Основи молекулярно-кінетичної теорії речовини. Статистичні розподіли та явища переносу в газах
- •§ 14. Перше начало термодинаміки
- •§ 15. Друге начало термодинаміки
- •§ 16. Реальні гази 1 рідини
- •§ 17. Теплові властивості твердих тіл. Фазові переходи
- •§ 18. Електричне поле
- •§ 19. Електричне поле в речовині
- •§ 20. Постійний електричний струм
- •Правила Кірхгофа для розгалужених кіл
- •§ 21. Електричний струм у металах, вакуумі та газах
- •§ 22. Постійне магнітне поле
- •§ 23. Електромагнітна індукція
- •§ 25. Магнітне поле в речовині
- •1. Вільні коливання в контурах
- •2. Вимушені коливання в контурах
- •Тема 27. Геометрична оптика.
- •§ 28. Інтерференція світла
- •§ 29. Дифракція світла
- •§ 30. Поляризація світла. Розсіяння, поглинання, дисперсія світла
- •§ 33. Хвильові властивості речовини
- •§ 34. Будова атомів і молекул
- •§ 35. Квантові явища в твердих тілах
- •§ 38. Основні характеристики атомного ядра
- •§ 39. Радіоактивність
- •Тема 9. Вільні гармонічні коливання.
- •Тема 10. Згасаючі та вимушені коливання.
- •Тема 11. Хвильові процеси. Акустика.
- •Тема 12. Основи молекулярно-кінетичної теорії'.
- •Тема 13. Статистичні розподіли та явища переносу в газах.
- •Тема 14. Перше начало термодинаміки.
- •Тема 19. Електростатичне поле в речовині.
- •Тема 20. Закони постійного струму.
- •Тема 22. Магнітне поле.
- •Тема 27. Геометрична оптика.
- •Тема 28. Інтерференція світла.
- •Тема 29. Дифракція світла.
- •Тема 31. Теплове випромінювання.
- •Тема 32. Квантова оптика.
- •Тема 33. Елементи квантової механіки.
§ 14. Перше начало термодинаміки
Перше начало термодинаміки
![]() , (1.165)
, (1.165)
де
![]() - елементарна кількість теплоти, що
підводиться до термодинамічної системи;
- елементарна кількість теплоти, що
підводиться до термодинамічної системи;
![]() - зміна внутрішньої енергії системи;
- зміна внутрішньої енергії системи;
![]() - робота, виконувана системою проти
зовнішніх сил при нескінченно малій
зміні об’єму.
- робота, виконувана системою проти
зовнішніх сил при нескінченно малій
зміні об’єму.
Зміна внутрішньої енергії ідеального газу
![]() , (1.166)
, (1.166)
![]() -
зміна температури; - молярна теплоємність
газу при ізохорному процесі;
-
зміна температури; - молярна теплоємність
газу при ізохорному процесі;
![]() , (1.166а)
, (1.166а)
![]() -
кількість ступенів вільності молекул
газу.
-
кількість ступенів вільності молекул
газу.
Молярна теплоємність газу при ізобарному процесі (рівняння Майєра)
![]() . (1.167)
. (1.167)
Молярна і питома теплоємності пов’язані рівнянням
![]() . (1.167а)
. (1.167а)
Робота, виконувана газом при ізобарному процесі,
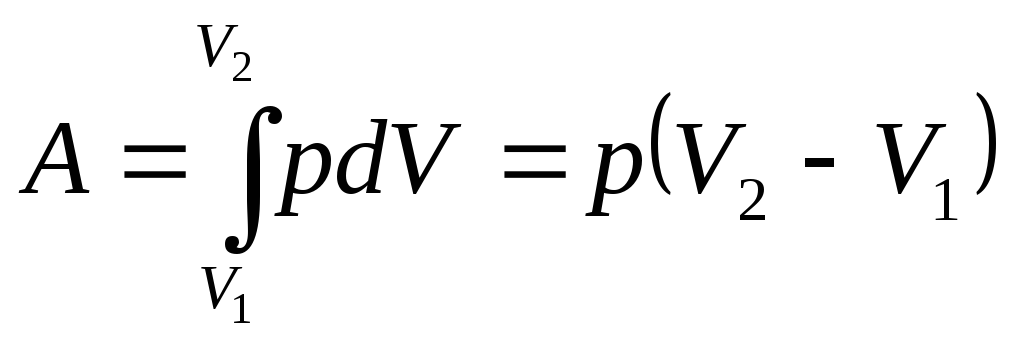 . (1.168)
. (1.168)
Робота при ізотермічному процесі
![]() . (1.169)
. (1.169)
Рівняння адіабатного процесу (рівняння Пуассона)
![]() ,
(1.170)
,
(1.170)
або
![]() , (1.170,а)
, (1.170,а)
або
![]() ,
(1.170,б)
,
(1.170,б)
де
![]() — показник
адіабати.
— показник
адіабати.
Робота при адіабатному процесі
 ,
,
або
 =
=
![]()
![]() . (1.170, в)
. (1.170, в)
Рівняння політропного процесу
![]() , (1.171)
, (1.171)
де
![]() — показник
політропи;
— показник
політропи;
![]() — молярна теплоємність газу при
політропному процесі.
— молярна теплоємність газу при
політропному процесі.
Робота при політропному процесі
 , (1.172)
, (1.172)
або
 . (1.173)
. (1.173)
§ 15. Друге начало термодинаміки
Коефіцієнт корисної дії (ККД) теплової машини
![]() , (1.174)
, (1.174)
де
![]() — кількість теплоти, яку дістає робоче
тіло від нагрівника;
— кількість теплоти, яку дістає робоче
тіло від нагрівника;
![]() — кількість теплоти, яка передається
робочим тілом холодильнику.
— кількість теплоти, яка передається
робочим тілом холодильнику.
ККД ідеального циклу Карно
![]() , (1.175)
, (1.175)
де
![]() — температура нагрівача;
— температура нагрівача;
![]() — температура холодильника.
— температура холодильника.
Холодильний коефіцієнт холодильної машини
![]() , (1.176)
, (1.176)
де
![]() — кількість теплоти, яка відбирається
від охолоджуваного тіла за цикл;
— кількість теплоти, яка відбирається
від охолоджуваного тіла за цикл;
![]() — робота,
виконувана над робочим тілом за цикл;
— робота,
виконувана над робочим тілом за цикл;
![]() — кількість теплоти, яка передається
навколишньому середовищу.
— кількість теплоти, яка передається
навколишньому середовищу.
Холодильний коефіцієнт ідеального оберненого циклу Карно
![]() , (1.177)
, (1.177)
де
![]() — температура середовища, якому
передається теплота;
— температура середовища, якому
передається теплота;
![]() — температура охолоджуваного тіла.
— температура охолоджуваного тіла.
Приріст
ентропії
![]() при переході термодинамічної системи
із стану 1
у стан 2
при переході термодинамічної системи
із стану 1
у стан 2
![]() . (1.178)
. (1.178)
Адіабатний
процес (![]() ).
Для оборотного процесу маємо
).
Для оборотного процесу маємо
![]() ,
звідси
,
звідси
![]() ,
(1.179)
,
(1.179)
тобто оборотні адіабатні процеси є ізоентропійними.
Для оборотного ізотермічного процесу між двома станами 1 і 2 маємо
![]() . (1.180)
. (1.180)
З рівняння (1.165),
оскільки
![]() ,маємо
,маємо
![]() ,
а робота в ізотермічному процесі
дорівнює (1.169), тому вираз (1.180) можна
записати у вигляді:
,
а робота в ізотермічному процесі
дорівнює (1.169), тому вираз (1.180) можна
записати у вигляді:
![]() . (1.181)
. (1.181)
Ізохорний
процес (![]() ).
При сталому об’ємові
).
При сталому об’ємові
![]() ,
тому
,
тому
 .(1.182)
.(1.182)
Ізобарний
процес (![]() ).
При цьому
).
При цьому
![]() і приріст ентропії
і приріст ентропії
 .
(1.183)
.
(1.183)
Ентропія
![]() і термодинамічна ймовірність (статистична
вага)
і термодинамічна ймовірність (статистична
вага)
![]() зв'язані співвідношенням
зв'язані співвідношенням
![]() ,
де
,
де
![]() — стала Больцмана.
— стала Больцмана.
§ 16. Реальні гази 1 рідини
Рівняння Ван-дер-Ваальса для довільної маси пг газу
 , (1.179)
, (1.179)
де
![]() і
і
![]() — сталі
Ван-дер-Ваальса. В цьому рівнянні
— сталі
Ван-дер-Ваальса. В цьому рівнянні
![]() —тиск,
зумовлений
силами
взаємодії молекул,
—тиск,
зумовлений
силами
взаємодії молекул,
![]() —
об'єм, зв'язаний з власним об'ємом
молекул.
—
об'єм, зв'язаний з власним об'ємом
молекул.
Зв'язок
критичних параметрів — молярного
об'єму, тиску і температури газу — із
сталими
![]() і
і
![]() Ван-дер-Ваальса
Ван-дер-Ваальса
![]() . (1.180)
. (1.180)
Стала
Ван-дер-Ваальса
![]() ,
де
,
де
![]() —
радіус молекули газу,
—
радіус молекули газу,
![]() —
стала
Авогадро.
—
стала
Авогадро.
Зв'язок між критичними параметрами моля речовини
![]() . (1.181)
. (1.181)
Рівняння Ван-дер-Ваальса у зведених величинах для одного моля газу
![]() , (1.182)
, (1.182)
де
![]() .
.
Зміна температури при дроселюванні реального газу в об'єм з невеликим тис
ком
 , (1.183)
, (1.183)
де
![]() — початковий об'єм і початкова температура
газу.
— початковий об'єм і початкова температура
газу.
Відносна вологість повітря
![]() ,
або
,
або
![]() , (1.184)
, (1.184)
де
![]() і
і
![]() — відповідно парціальний тиск і густина
водяної пари, що знаходиться в повітрі
при даній температурі (абсолютна
вологість);
— відповідно парціальний тиск і густина
водяної пари, що знаходиться в повітрі
при даній температурі (абсолютна
вологість);
![]() і
і
![]() —парціальний
тиск і густина насиченої водяної пари
при тій самій температурі.
—парціальний
тиск і густина насиченої водяної пари
при тій самій температурі.
Рівняння Клапейрона - Клаузіуса
![]() , (1.185)
, (1.185)
де
![]() і
і
![]() — питомі об'єми речовини в двох станах;
— питомі об'єми речовини в двох станах;
![]() і
і
![]() — температура
і питома теплота переходу речовини із
стану 1
в 2.
— температура
і питома теплота переходу речовини із
стану 1
в 2.
Коефіцієнт поверхневого натягу
![]() , (1.186)
, (1.186)
де
![]() — сила
поверхневого натягу;
— сила
поверхневого натягу;
![]() —
довжина ділянки контуру, що обмежує
вільну поверхню;
—
довжина ділянки контуру, що обмежує
вільну поверхню;
![]() —
зміна вільної енергії поверхневого
шару рідини;
—
зміна вільної енергії поверхневого
шару рідини;
![]() — зміна площі цього шару.
— зміна площі цього шару.
Надлишковий тиск, зумовлений кривизною поверхні рідини (формула Лапласа),
 , (1.187)
, (1.187)
де
![]() і
і
![]() — радіуси кривизни двох взаємно
перпендикулярних перерізів поверхні
рідини.
— радіуси кривизни двох взаємно
перпендикулярних перерізів поверхні
рідини.
Висота підняття рідини в капілярних трубках та між паралельними площинами
![]() ,
, ![]() (1.188)
(1.188)
де
![]() -
крайовий кут змочування;
-
крайовий кут змочування;
![]() -
густина рідини;
-
густина рідини;
![]() -
радіус капілярної трубки;
-
радіус капілярної трубки;
![]() - відстань між пластинами..
- відстань між пластинами..
Відносна зміна об'єму рідини при нагріванні
![]() , (1.189)
, (1.189)
де
![]() — температурний коефіцієнт об'ємного
розширення.
— температурний коефіцієнт об'ємного
розширення.
Відносна зміна об'єму рідини при зміні тиску
![]() , (1.190)
, (1.190)
де
![]() — коефіцієнт стисливості.
— коефіцієнт стисливості.
Осмотичний тиск розчину (1.формула Вант-Гоффа)
![]() , (1.191)
, (1.191)
де
![]() — кількість молів розчиненої речовини
в одиниці об'єму розчинника.
— кількість молів розчиненої речовини
в одиниці об'єму розчинника.
Тиск насиченої пари над вгнутою сферичною поверхнею рідини менше, а над опуклою – більше, за тиск над плоскою поверхнею, на величину, яка дорівнює
![]() , (1.191)
, (1.191)
де
![]() - радіус сфери,
- радіус сфери,
![]() і
і
![]() - густина насиченої пари і рідини.
- густина насиченої пари і рідини.
