
- •Общие методические указания
- •Требования к знаниям и умениям по дисциплине.
- •Распределение часов учебного плана по формам обучения и видам занятий
- •1.1. Вывод химической формулы вещества по его количественному составу
- •1.2. Расчеты по химическим уравнениям
- •1 Моль hCl – 1 моль nh4Cl
- •0,2 Моль hCl – х моль nh4Cl
- •2. Моль. Закон Авогадро. Мольный объем
- •1 Моль занимает объем 22,4 л
- •3. Классы неорганических соединений
- •4. Составление уравнений окислительно-восстановительных реакций по методу электронного баланса
- •5. Направление окислительно-восстановительных процессов
- •6. Гальванические элементы
- •7. Коррозия
- •8. Электрохимические процессы при электролизе
- •9. Комбинированные задачи
- •Варианты контрольных работ
3. Классы неорганических соединений
Неорганические соединения могут классифицироваться как по составу, так и по свойствам (функциональным признакам). По составу они, прежде всего, подразделяются на двухэлементные (бинарные), и многоэлементные соединения.
К бинарным соединениям относятся, например, соединения элементов с кислородом (оксиды), галогенами (галиды – фториды, хлориды, бромиды, иодиды), серой (сульфиды), азотом (нитриды), фосфором (фосфиды), углеродом (карбиды), соединения металлов с водородом (гидриды). Названия бинарных соединений образуются из латинского корня названия более электроотрицательного элемента с окончанием «ид» и русского названия менее электроотрицательного элемента в родительном падеже. Так, Al2O3 – оксид алюминия (но OF2 – фторид кислорода, так как фтор – более электроотрицательный элемент, чем кислород).
Исключением из указанных правил являются водородные соединения неметаллов, проявляющие свойства кислот; их названия образуются по правилам, принятым для кислот.
По функциональным признакам неорганические соединения подразделяются на классы в зависимости от характерных функций, выполняемых ими в химических реакциях. Так, оксиды подразделяются на несолеобразующие (безразличные) и солеобразующие. Последние, в свою очередь, делятся на основные, кислотные и амфотерные.
Существуют соединения элементов с кислородом, которые по составу относятся к классу оксидов, но по своему строению и свойствам принадлежат к классу солей. Это так называемые пероксиды, или перекиси.
Важный класс неорганических соединений, выделяемый по функциональным признакам, составляют кислоты. С позиций теории электролитической диссоциации к кислотам относятся вещества, способные диссоциировать в растворе с образованием ионов водорода.
Еще один важный класс неорганических соединений, характеризующийся общими свойствами, образуют основания. Согласно теории электролитической диссоциации к ним относятся вещества, способные диссоциировать в растворе с образованием гидроксид-ионов, т.е. основные гидроксиды.
Соли можно рассматривать как продукты полного или частичного замещения атомов водорода в молекуле кислоты атомами металла или как продукты полного или частичного замещения гидроксогрупп в молекуле основного гидроксида кислотными остатками. При полном замещении атомов водорода в молекуле кислоты образуются средние (нормальные) соли, при неполном – кислые соли (гидросоли). Кислые соли образуются многоосновными кислотами.
При частичном замещении гидроксогрупп в молекуле основного гидроксида кислотными остатками образуются основные соли (гидроксосоли). Основные соли могут быть образованы только многокислотными гидроксида.
Пример. Осуществите превращения согласно схеме:
Ca→Са3Р2 →РН3→Р2О5→Са(Н2РО4)2→Na3PO4→Ca3(PO4)2
Решение:
1. 3Са0+2Р0
![]() Са3+2Р
Са3+2Р![]() .
.
2. Са3Р2 + 6Н2О → 3Са(ОН)2↓ + 2РН3↑.
3. 2Р–3Н![]() + 4О
+ 4О![]()
![]() Р
Р![]() О
О![]() +3Н
+3Н![]() О–2.
О–2.
4. Р2О5 + Н2О + Са(ОН)2 →Са(Н2РО4)2;
Р2О5 +
Н2О+2ОН–→2Н2РО![]() .
.
5. 3Са(Н2РО4)2+12NaOH→Са3(РО4)2↓ + 4Na3PO4 + 12H2O;
3Са2+ + 6Н2РО![]() + 12ОН– → Са3(РО4)2↓
+ 4РО
+ 12ОН– → Са3(РО4)2↓
+ 4РО![]() + 12Н2О.
+ 12Н2О.
6. 2Na3РO4 + 3CaCl2 → Ca(PO4)2↓ + 6NaCl.
3Cа2+
+ 2PO![]() → Ca3(PO4)2↓
→ Ca3(PO4)2↓
Вместо СаСl2 можно использовать любую другую растворимую соль кальция или Са(ОН)2.
Задачи
61. Осуществите превращения согласно схеме:
HNO3 → NH4NO3 → NH3 → NH4NO2 → N2 →NO2
62. Осуществите превращения согласно схеме:
Fe → Fe2(SO4)3 → Fe → Fe(OH)2 → Fe(OH)3 → FeCl3 → FeCl2
63. Осуществите превращения согласно схеме:
Cu(OH)2 → Cu(NO3)2 → (CuOH)Cl → CuCl2 → (CuOH)NO3
64. Осуществите превращения согласно схеме:
S → ZnS → H2S → SO2 → H2SO4 → Na2SO4 → NaCl
65. Осуществите превращения согласно схеме:
Ca → Ca3P2 → PH3 → P2O5 → Ca(H2PO4)2 → Na3PO4 →Ca3(PO4)2
66. Осуществите превращения согласно схеме:
Na2CO3 → NaHCO3 → CaCO3 → KHCO3 → KCl → KOH → KH
67. Осуществите превращения согласно схеме:
KNO2 → KNO3 → HNO3 → Cu(NO3)2 → NO2 →KNO3 → K2SO4
68. Осуществите превращения согласно схеме:
Ag → AgNO3 → O2 → SO3 →H2SO4 → Ag2SO4
69. Осуществите превращения согласно схеме:
FeS → SO2 → NaHSO3 → Na2SO4 → NaNO3 → SO2 → Ca(HSO3)2
70. Осуществите превращения согласно схеме:
Si → Ca2Si → SiH4 → CaSiO3 → CaO
71 Осуществите превращения согласно схеме:
Fe → FeSO4 → Fe2(SO4)3 → Fe(NO3)3 → Fe(OH)3 →Fe(NO3)3 →Fe2O3 →Fe
72. Осуществите превращения согласно схеме:
Mg → MgO → MgCl2 → Mg(NO3)2 → MgO → Mg(OH)2
73. Осуществите превращения согласно схеме:
N2 → NH3 → NO → NO2 → HNO3 → NaNO3 → NaNO2
74. Осуществите превращения согласно схеме:
Al → Al(NO3)3 → Al(OH)3 → AlCl3 → Al2(SO4)3 → Al(OH)3 → Al2O3
75. Осуществите превращения согласно схеме:
KMnO4 → O2 → Fe3O4 →Fe → FeS → H2S → S
76. Осуществите превращения согласно схеме:
Zn →
Na2ZnO2
→ Zn(OH)2
→ K2![]() → ZnCl2 → Zn
→ ZnCl2 → Zn
77. Осуществите превращения согласно схеме:
C → CO → CO2 → CO → NaHCO3 → Na2CO3 → CaCO3
78. Напишите уравнения реакций, с помощью которых можно осуществить следующие превращения:
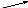 Са3(РО4)2
Са3(РО4)2
![]() СаНРО4
СаНРО4
![]() Са(Н2РО4)2
Са(Н2РО4)2
а)
Р
![]() Р2О5
Р2О5
![]() Н3РО4
Н3РО4
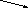
Са(Н2РО4)2
![]() СаНРО4
СаНРО4
![]() Са3(РО4)2
Са3(РО4)2
79. Напишите уравнения реакций разложения следующих аммонийных солей: NH4NO2, NH4NO3, (NH4)2CO3, (NH4)2SO4, NH4Cl.
80. При окислении фосфора было израсходовано 16 г кислорода. Полученный фосфорный ангидрид растворили в 50 см3 25%-ного раствора едкого натра (плотность 1,28 г/см3). Какая соль при этом образовалась и какова ее массовая доля в растворе?
81. Составьте уравнения реакций, с помощью которых можно осуществить следующие превращения:
а) SiO2
![]() Si
Si
![]() Mg2Si
Mg2Si
![]() SiH4
SiH4
![]() Na2SiO3
Na2SiO3
![]() H2SiO3;
H2SiO3;
б) SiCl4
![]() Si
Si
![]() K2SiO3
K2SiO3
![]() H2SiO3
H2SiO3
![]() SiO2
SiO2
![]() стекло;
стекло;
в) Si
![]() SiO2
SiO2
![]() СaSiO3
СaSiO3
![]() H2SiO3
H2SiO3
![]()
![]()
![]() SiC
SiC
Si
![]() SiF4.
SiF4.
82. В трех пробирках имеются растворы силиката натрия, карбоната натрия и сульфида калия. С помощью какого одного реактива можно определить каждый из указанных растворов? Приведите уравнения соответствующих реакций.
83. Приведите примеры реакций, в которых:
а) сернистый газ играет роль кислотного оксида;
б) сернистый газ играет роль окислителя;
в) сернистый газ проявляет восстановительные свойства.
84. Напишите уравнения практически осуществимых реакций:
а. Fe+HCl= е. Fe(OH)3+KCl=
б. Fe2O3+HNO3= ж. FeSO4+Ba(NO3)2=
в. Fe2O3+H2O= з. Fe(OH)2+H2SO4=
г. FeCl2+Cl2= и. FeSO4+NaCl=
д. FeSO4+Cu= k. Fe2O3+Al=
85. Как осуществить следующие превращения:
H2SO3![]() SO2
SO2
![]() S
S
![]() H2S
H2S
![]() SO2
SO2
![]() SO3
SO3
![]() H2SO4
H2SO4![]() BaSO4
BaSO4



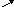
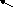



H2SO4
![]() ZnSO4
ZnSO4
![]() ZnS Na2S
ZnS Na2S
![]() Na2SO4
Na2SO4
