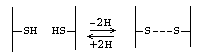- •Биологическое окисление. Понятие о метаболизме.
- •История развития учения о биоокислении.
- •Современная теория биоокисления
- •Митохондриальное окисление (МтО).
- •Главная (полная) цепь
- •Укороченная (сокращенная) цепь
- •Главная дыхательная цепь
- •Митохондриального окисления
- •Синтез атф.
- •Никотинамидные дегидрогеназы (надг)
- •Комплекс I
- •Комплекс III.
- •Комплекс IV.
- •Основные процессы, для которых используется энергия атф:
- •Синтез атф.
- •Специфические ингибиторы тканевого дыхания
- •Вещества-разобщители процессов окисления и фосфорилирования
- •Теория сопряжения окисления и фосфорилирования питера митчелла.
- •Автономная саморегуляция системы митохондриального окисления
- •Варианты дыхательной цепи.
- •1. Полная дыхательная цепь
- •2. Сокращенная (укороченная) дыхательная цепь
- •3. Максимально сокращенная (максимально укороченная) дыхательная цепь.
- •Окислительное декарбоксилирование пировиноградной
- •Окислительное декарбоксилирование пирувата
- •Цикл трикарбоновых кислот
- •Итоговое уравнение цтк
- •Биологическое значение цтк
- •Автономная саморегуляция цтк
- •Энергетический заряд клетки (эзк)
- •Челночные механизмы переноса водорода
- •Биохимия крови.
- •Функции крови.
- •Альбумины
- •Функции альбуминов
- •Глобулины
- •Функции 1-глобулинов
- •Биохимия мышечной ткани
- •1. Специальные реакции субстратного фосфорилирования
- •2. Гликолиз, гликогенолиз.
- •3. Окислительное фосфорилирование.
- •Биохимия почек.
- •1. Ультрафильтрация
- •2. Реабсорбция
- •3. Секреция
- •1. Водно-солевой гомеостаз.
- •2. Участие почек в регуляции кислотно-щелочного равновесия
- •2) Аммониогенез
- •3) Глюконеогенез
- •Биохимия костной ткани, тканей зуба, биохимия слюны.
- •Органический матрикс кости.
- •Дентин.
- •Пульпа.
- •Биохимия нервной ткани
- •2) Пептиды
- •Биохимия питания биохимические основы питания человека.
- •Окислительное декарбоксилирование пирувата
- •Внемитохондриальное окисление
- •I. Окисление оксидазного типа.
- •II. Окисление оксигеназного типа
- •Примеры реакций оксигеназного типа окисления
- •Антиоксидантная система.
- •1. Ферментативная
- •В) пероксидаза.
- •2. Неферментативные компоненты антиоксидантной системы
- •Метаболизм белков Особая роль белков в питании
- •Переваривание и всасывание белков в желудочно-kишечном тракте
- •Механизмы, защищающие белки от действия протеиназ:
- •Ингибиторы сериновых протеиназ.
- •Ингибиторы тиоловых протеиназ
- •Высокоспецифичные протеиназы
- •Катаболизм аминокислот.
- •3. Гистидиндекарбоксилаза
- •Обмен сложных белков обмен нуклеопротеинов
- •Обмен нуклеиновых кислот
- •Различия в катаболизме пуриновых и пиримидиновых азотистых оснований.
- •Функции мочевой кислоты:
- •Синтез нуклеиновых кислот синтез мононуклеотидов
- •Синтез пиримидиновых мононуклеотидов.
- •Синтез нуклеиновых кислот из мононуклеотидов
- •Строение и обмен хромопротеинов
- •Параметаболизм
- •Некоторые параметаболические процессы
- •Строение и свойства белков.
- •Основные различия в строении белковых молекул
- •II. Биологическая классификация.
- •Типы связей между аминокислотами в молекуле белка
- •Слабые типы связей
- •Пространственная организация белковой молекулы
- •Первичная структура
- •Вторичная структура
- •Третичная структура
- •Четвертичная структура
- •Методы определения первичной структуры белка
- •1)Деградация по Эдмону
- •2) Секвенирование днк
- •3) Рентгеноструктурный анализ
- •Электронная микроскопия
- •Конфигурация и конформация белковой молекулы
- •Лиганды
- •Нативность белковой молекулы
- •Денатурация белка
- •Факторы, вызывающие денатурацию белков
- •Физические факторы
- •Химические факторы
- •Обратимость денатурации
- •Белки стресса
- •Физико-химические свойства белков. Растворимость белков в воде.
- •Факторы стабилизации белка в растворе.
- •Свойства воды гидратной оболочки
- •Способы осаждения белков
- •Осаждение нативных белков
- •Осаждение денатурированных белков
- •Строение и свойства ферментов
- •Общие свойства катализаторов
- •Особенности ферментов как биологических катализаторов
- •Строение ферментов
- •I класс - оксидоредуктазы.
- •Кинетика ферментативного катализа
- •Характеристика конкурентных ингибиторов
- •Автономная саморегуляция ферментативных процессов
- •2. Субстрат - аллостерический активатор своего фермента.
- •3. Продукт реакции - аллостерический активатор своего фермента.
- •4. Один субстрат - два фермента и два продукта.
- •5. Один субстрат, два фермента и один продукт
- •Фруктоземия.
- •Химия и обмен липидов.
- •Липопротеины
- •Пищевой жир.
- •Липогенез.
- •Гормональная регуляция синтеза жира
- •Катаболизм жира
- •Пути метаболизма глицерина
- •Распад глицерина по пути к углеводам
- •Пути использования жирных кислот.
- •Катаболизм жирных кислот
- •Реакции синтеза кетоновых тел
- •Утилизация кетоновых тел
- •Биохимия фосфолипидов, гликолипидов и стероидов. Биологические мембраны. Биологические мембраны
- •Фосфолипиды.
- •Роль мембранных белков.
- •Роль углеводных компонентов мембран
- •Функции липоидов
- •Катаболизм липоидов.
- •Строение и обмен хромопротеинов
- •Цикл трикарбоновых кислот
- •Итоговое уравнение цтк
- •Биологическое значение цтк
- •Автономная саморегуляция цтк
- •Энергетический заряд клетки (эзк)
- •Челночные механизмы переноса водорода
II. Биологическая классификация.
а) Незаменимые аминокислоты, их еще называют "эссенциальные". Они не могут синтезироваться в организме человека и должны обязательно поступать с пищей. Их 8 и еще 2 аминокислоты относятся к частично незаменимым.
Незаменимые: метионин, треонин, лизин, лейцин, изолейцин, валин, триптофан, фенилаланин.
Частично незаменимые: аргинин, гистидин.
а) Заменимые (могут синтезироваться в организме человека). Их 10: глутаминовая кислота, глутамин, пролин, аланин, аспарагиновая кислота, аспарагин, тирозин, цистеин, серин и глицин.
III. Химическая классификация - в соответствии с химической структурой радикала аминокислоты (алифатические, ароматические).
Белки синтезируются на рибосомах, не из свободных аминокислот, а из их соединений с транспортными РНК (т-РНК).
Этот комплекс называется «аминоацил-т-РНК».
Типы связей между аминокислотами в молекуле белка
2 группы:
1. КОВАЛЕНТНЫЕ СВЯЗИ - обычные прочные химические связи.
а) пептидная связь
б) дисульфидная связь
2. НЕКОВАЛЕНТНЫЕ (СЛАБЫЕ) ТИПЫ СВЯЗЕЙ - физико-химические взаимодействия родственных структур. В десятки раз слабее обычной химической связи. Очень чувствительны к физико-химическим условиям среды. Они неспецифичны, то есть соединяются друг с другом не строго определенные химические группировки, а самые разнообразные химические группы, но отвечающие определенным требованиям.
а) Водородная связь
б) Ионная связь
в) Гидрофобное взаимодействие
ПЕПТИДНАЯ СВЯЗЬ.
Формируется за счет COOH-группы одной аминокислоты и NH2-группы соседней аминокислоты. В названии пептида окончания названий всех аминокислот, кроме последней, находящейся на «С»-конце молекулы меняются на «ил»
Тетрапептид: валил-аспарагил-лизил-серин


ПЕПТИДНАЯ СВЯЗЬ формируется ТОЛЬКО ЗА СЧЕТ АЛЬФА-АМИНОГРУППЫ И СОСЕДНЕЙ COOH-ГРУППЫ ОБЩЕГО ДЛЯ ВСЕХ АМИНОКИСЛОТ ФРАГМЕНТА МОЛЕКУЛЫ!!! Если карбоксильные и аминогруппы входят в состав радикала, то они никогда(!) не участвуют в формировании пептидной связи в молекуле белка.
Любой белок - это длинная неразветвленная полипептидная цепь, содержащая десятки, сотни, а иногда более тысячи аминокислотных остатков. Но какой бы длины ни была полипептидная цепь, всегда в основе ее - стержень молекулы, абсолютно одинаковый у всех белков. Каждая полипептидная цепь имеет N-конец, на котором находится свободная концевая аминогруппа и С-конец, образованный концевой свободной карбоксильной группой. На этом стержне сидят как боковые веточки радикалы аминокислот. Числом, соотношением и чередованием этих радикалов один белок отличается от другого. Сама пептидная связь является частично двойной в силу лактим-лактамной таутомерии. Поэтому вокруг нее невозможно вращение, а сама она по прочности в полтора раза превосходит обычную ковалентную связь. На рисунке видно, что из каждых трех ковалентных связей в стержне молекулы пептида или белка две являются простыми и допускают вращение, поэтому стержень (вся полипептидная цепь) может изгибаться в пространстве.
Хотя пептидная связь довольно прочная, ее сравнительно легко можно разрушить химическим путем – кипячением белка в крепком растворе кислоты или щелочи в течении 1-3 суток.
К ковалентным связям в молекуле белка помимо пептидной, относится также ДИСУЛЬФИДНАЯ СВЯЗЬ.
Цистеин - аминокислота, которая в радикале имеет SH-группу, за счет которой и образуются дисульфидные связи.