
- •Биологическое окисление. Понятие о метаболизме.
- •История развития учения о биоокислении.
- •Современная теория биоокисления
- •Митохондриальное окисление (МтО).
- •Главная (полная) цепь
- •Укороченная (сокращенная) цепь
- •Главная дыхательная цепь
- •Митохондриального окисления
- •Синтез атф.
- •Никотинамидные дегидрогеназы (надг)
- •Комплекс I
- •Комплекс III.
- •Комплекс IV.
- •Основные процессы, для которых используется энергия атф:
- •Синтез атф.
- •Специфические ингибиторы тканевого дыхания
- •Вещества-разобщители процессов окисления и фосфорилирования
- •Теория сопряжения окисления и фосфорилирования питера митчелла.
- •Автономная саморегуляция системы митохондриального окисления
- •Варианты дыхательной цепи.
- •1. Полная дыхательная цепь
- •2. Сокращенная (укороченная) дыхательная цепь
- •3. Максимально сокращенная (максимально укороченная) дыхательная цепь.
- •Окислительное декарбоксилирование пировиноградной
- •Окислительное декарбоксилирование пирувата
- •Цикл трикарбоновых кислот
- •Итоговое уравнение цтк
- •Биологическое значение цтк
- •Автономная саморегуляция цтк
- •Энергетический заряд клетки (эзк)
- •Челночные механизмы переноса водорода
- •Биохимия крови.
- •Функции крови.
- •Альбумины
- •Функции альбуминов
- •Глобулины
- •Функции 1-глобулинов
- •Биохимия мышечной ткани
- •1. Специальные реакции субстратного фосфорилирования
- •2. Гликолиз, гликогенолиз.
- •3. Окислительное фосфорилирование.
- •Биохимия почек.
- •1. Ультрафильтрация
- •2. Реабсорбция
- •3. Секреция
- •1. Водно-солевой гомеостаз.
- •2. Участие почек в регуляции кислотно-щелочного равновесия
- •2) Аммониогенез
- •3) Глюконеогенез
- •Биохимия костной ткани, тканей зуба, биохимия слюны.
- •Органический матрикс кости.
- •Дентин.
- •Пульпа.
- •Биохимия нервной ткани
- •2) Пептиды
- •Биохимия питания биохимические основы питания человека.
- •Окислительное декарбоксилирование пирувата
- •Внемитохондриальное окисление
- •I. Окисление оксидазного типа.
- •II. Окисление оксигеназного типа
- •Примеры реакций оксигеназного типа окисления
- •Антиоксидантная система.
- •1. Ферментативная
- •В) пероксидаза.
- •2. Неферментативные компоненты антиоксидантной системы
- •Метаболизм белков Особая роль белков в питании
- •Переваривание и всасывание белков в желудочно-kишечном тракте
- •Механизмы, защищающие белки от действия протеиназ:
- •Ингибиторы сериновых протеиназ.
- •Ингибиторы тиоловых протеиназ
- •Высокоспецифичные протеиназы
- •Катаболизм аминокислот.
- •3. Гистидиндекарбоксилаза
- •Обмен сложных белков обмен нуклеопротеинов
- •Обмен нуклеиновых кислот
- •Различия в катаболизме пуриновых и пиримидиновых азотистых оснований.
- •Функции мочевой кислоты:
- •Синтез нуклеиновых кислот синтез мононуклеотидов
- •Синтез пиримидиновых мононуклеотидов.
- •Синтез нуклеиновых кислот из мононуклеотидов
- •Строение и обмен хромопротеинов
- •Параметаболизм
- •Некоторые параметаболические процессы
- •Строение и свойства белков.
- •Основные различия в строении белковых молекул
- •II. Биологическая классификация.
- •Типы связей между аминокислотами в молекуле белка
- •Слабые типы связей
- •Пространственная организация белковой молекулы
- •Первичная структура
- •Вторичная структура
- •Третичная структура
- •Четвертичная структура
- •Методы определения первичной структуры белка
- •1)Деградация по Эдмону
- •2) Секвенирование днк
- •3) Рентгеноструктурный анализ
- •Электронная микроскопия
- •Конфигурация и конформация белковой молекулы
- •Лиганды
- •Нативность белковой молекулы
- •Денатурация белка
- •Факторы, вызывающие денатурацию белков
- •Физические факторы
- •Химические факторы
- •Обратимость денатурации
- •Белки стресса
- •Физико-химические свойства белков. Растворимость белков в воде.
- •Факторы стабилизации белка в растворе.
- •Свойства воды гидратной оболочки
- •Способы осаждения белков
- •Осаждение нативных белков
- •Осаждение денатурированных белков
- •Строение и свойства ферментов
- •Общие свойства катализаторов
- •Особенности ферментов как биологических катализаторов
- •Строение ферментов
- •I класс - оксидоредуктазы.
- •Кинетика ферментативного катализа
- •Характеристика конкурентных ингибиторов
- •Автономная саморегуляция ферментативных процессов
- •2. Субстрат - аллостерический активатор своего фермента.
- •3. Продукт реакции - аллостерический активатор своего фермента.
- •4. Один субстрат - два фермента и два продукта.
- •5. Один субстрат, два фермента и один продукт
- •Фруктоземия.
- •Химия и обмен липидов.
- •Липопротеины
- •Пищевой жир.
- •Липогенез.
- •Гормональная регуляция синтеза жира
- •Катаболизм жира
- •Пути метаболизма глицерина
- •Распад глицерина по пути к углеводам
- •Пути использования жирных кислот.
- •Катаболизм жирных кислот
- •Реакции синтеза кетоновых тел
- •Утилизация кетоновых тел
- •Биохимия фосфолипидов, гликолипидов и стероидов. Биологические мембраны. Биологические мембраны
- •Фосфолипиды.
- •Роль мембранных белков.
- •Роль углеводных компонентов мембран
- •Функции липоидов
- •Катаболизм липоидов.
- •Строение и обмен хромопротеинов
- •Цикл трикарбоновых кислот
- •Итоговое уравнение цтк
- •Биологическое значение цтк
- •Автономная саморегуляция цтк
- •Энергетический заряд клетки (эзк)
- •Челночные механизмы переноса водорода
Различия в катаболизме пуриновых и пиримидиновых азотистых оснований.
Пиримидиновые азотистые основания подвергаются тотальному разрушению до СО2, Н2О и NH3.
Пуриновые азотистые основания сохраняют циклическую структуру пурина. Конечный продукт: мочевая кислота - вещество пуриновой природы.
Аминогруппа азотистых оснований очень легко могут отщепляться гидролитическим путем. Аминогруппа может отщепляться, когда азотистое основание еще находится в составе нуклеозида, мононуклеотида и даже в составе нуклеиновой кислоты. Но поскольку в организме урацил не входит в состав ДНК, то дезаминирование цитозина и превращение его в урацил воспринимается клеткой как ошибка и исправляется.

Тимин распадается подобно урацилу, но сохраняется CH3-группа, и вместо -аланина образуется -аминоизобутират (-метил--аланин). Поскольку тимин встречается только в ДНК, то по уровню -аминоизобутирата в моче судят об интенсивности распада ДНК.
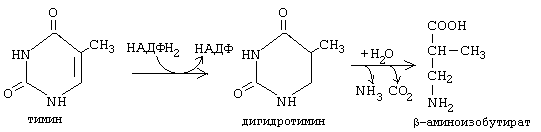
-аминоизобутират выводится из организма и определение его количества в моче может использоваться для оценки катаболизма ДНК.
КАТАБОЛИЗМ ПУРИНОВЫХ АЗОТИСТЫХ ОСНОВАНИЙ
Распад начинается с отщепления аминогруппы (ее отщепление также возможно в составе ДНК).

Фермент аденозиндезаминаза иногда образуется в дефектной мутантной форме, что приводит к врожденному иммунодефициту, так как нуклеотиды являются регуляторами функций лейкоцитов. При СПИДе активность этого фермента также значительно снижена.
Образовавшийся инозин подвергается фосфоролизу, и далее гипоксантин подвергается двукратному окислению путем отнятия водорода с одновременным присоединением воды. Эти две одинаковые реакции катализирует один и тот же фермент – ксантиноксидаза. Ксантиноксидаза может существовать в двух формах:
-
D-форма – дегидрогеназная
-
O-форма – оксидазная
Формы отличаются друг от друга по способности передавать 2 атома водорода. D-форма передает водород на главную дыхательную цепь митохондриального окисления, а O-форма – сразу на кислород с образованием H2O2. D-форма может переходить в О-форму путем ограниченного протеолиза при отщеплении небольшого участка молекулы.
Генетический дефект ксантиноксидазы проявляется ксантинурией и образованием ксантиновых камней в тканях. В этом случае источник ксантина – гуанин, подвергающийся гидролитическому дезаминированию.
Кроме, как у человека, мочевая кислота является конечным продуктом катаболизма пуринов у приматов, птиц, змей и ящериц.
Для других животных пуриновое кольцо подвергается распаду, за исключением долматской собаки.
Мочевая кислота является одним из нормальных компонентов мочи. За сутки в организме образуется около 1 грамма мочевой кислоты. Мочевая кислота выводится из организма с мочой - это обычный ее компонент, но в почках организма человека происходит ее интенсивная реабсорбция. Концентрация мочевой кислоты в крови поддерживается на постоянном уровне 0.12-0.30 ммоль/л.
В организме мочевая кислота существует, как правило, в лактимной форме.
