
- •Оглавление
- •Предисловие
- •ОБЩАЯ ЧАСТЬ
- •Введение
- •Глава 1. Земная кора и особенности ее состава
- •Глава 2. Конституция и свойства минералов
- •2.1. Общие сведения
- •2.2. Химический состав и формулы минералов
- •2.3. Физические свойства минералов
- •Морфологические особенности кристаллов минералов
- •Прозрачность
- •Цвет минералов
- •Цвет черты
- •Блеск и показатель преломления
- •Спайность и излом
- •Твердость
- •Хрупкость, ковкость, упругость
- •Удельный вес
- •Магнитность
- •Радиоактивность
- •Прочие свойства минералов
- •Глава 4. Образование минералов в природе
- •4.1. Общие положения
- •4.2. Геологические процессы минералообразования
- •Эндогенные процессы минералообразования
- •Экзогенные процессы минералообразования
- •Региональный метаморфизм и связанные с ним процессы минералообразования
- •ОПИСАТЕЛЬНАЯ ЧАСТЬ
- •Классификация и номенклатура минералов
- •Класс 1. Простые сернистые и им подобные соединения
- •Класс 2. Сульфосоли
- •Класс 1. Фториды
- •Класс 2. Хлориды, бромиды и иодиды
- •Класс 1. Простые и сложные окислы
- •Класс 1. Нитраты
- •Класс 2. Карбонаты
- •Класс 3. Сульфаты
- •Класс 4. Хроматы
- •Класс 5. Молибдаты и вольфраматы
- •Класс 6. Фосфаты, арсенаты и ванадаты
- •Класс 7. Бораты
- •Класс 8. Силикаты и алюмосиликаты
- •Подкласс Б. Силикаты с изолированными группами тетраэдров SiO4 в кристаллических структурах
- •ЗАКЛЮЧИТЕЛЬНАЯ ЧАСТЬ
- •Глава 1. Минеральный состав земной коры
- •Главнейшая литература по минералогии
- •1. Учебники, учебные и справочные пособия
- •2. Периодические издания
- •3. Сборники и монографии
- •Список наиболее важных минералов по главнейшим металлам (элементам)
Глава 2. Конституция и свойства минералов |
53 |
(SnO2) в теснейшем прорастании друг с другом, но при сохранении реликтового (т. е. прежнего) пластинчато зернистого строения агре гата, характерного для тиллита. Очевидно, в связи с увеличившейся в какой то момент концентрацией кислорода в данной среде олово, об ладая большим сродством с кислородом, обособилось из первоначаль но гомогенной минеральной массы в виде окисла, а свинец перешел в форму самостоятельного сернистого соединения.
Минералы, находящиеся в метамиктном состоянии, как метастабиль ные фазы, имеют некоторый запас потенциальной энергии по сравнению с устойчивой модификацией. Эта энергия связана со смещением атомов из равновесных положений, произошедшим при столкновении с оскол ками деления; при низких температурах амплитуды тепловых движений атомов не достаточны для их возвращения в положения, которые были характерны для структуры до начала метамиктного распада. Нагревание метамиктных минералов чаще всего позволяет вывести их из метастабиль ного состояния с восстановлением первоначального кристаллического состояния. Нередко восстановление структуры происходит за столь ко роткое время, что бурно выделяющийся избыток энергии, отвечающий теплоте плавления, приводит к почти мгновенному самопроизвольному разогреву минерала до высокой температуры, сопровождаемому растрес киванием и интенсивным свечением (так называемая рекалесценция).
2.2. ХИМИЧЕСКИЙ СОСТАВ И ФОРМУЛЫ МИНЕРАЛОВ
Выше мы уже упоминали о том, что подавляющее большинство встре чающихся в природе минералов представлено химическими соединени ями. Среди последних различают: а) соединения постоянного состава
(дальтониды) и б) соединения переменного состава.
Соединения постоянного состава. Все химические соединения по стоянного состава, как известно, строго подчиняются закону кратных от ношений (закон Дальтона) и закону валентных паев, связывающему от ношения компонентов данного соединения с отношениями их в других типах соединений. Эти законы находятся в полном соответствии с Пери одической системой элементов Д. И. Менделеева, законами кристалло химии и учением о симметрии в кристаллических средах.
Характерно, что эти соединения отличаются целым рядом особых физических свойств, отчетливо выступающих на физико химических диаграммах плавкости, растворимости, электропроводности, твердости, удельного веса, показателей преломления и пр.
Необходимо отметить, что реальные минералы в отношении своего химизма практически никогда не могут рассматриваться в качестве соеди нений постоянного состава, поскольку содержат то или иное изменяюще еся от индивида к индивиду количество примесей (минеральные индивиды
54 |
Общая часть |
также можно считать химически однородными лишь в первом приближе нии). Причина такого положения дел заключается, во первых, в одном из качеств природных минералообразующих систем, которое определяется законом В. И. Вернадского о «всюдности химических элементов». Второй причиной является чрезвычайная энергетическая выгодность наличия при месей в кристаллической структуре по сравнению с чистым веществом. Дело в том, что добавление малого количества примеси (не механической, а в атомной форме) вызывает резкое повышение так называемой конфигу' рационной энтропии соединения по сравнению с нулевым значением этого параметра для чистого вещества, что оказывает стабилизирующее воздей ствие на кристаллическую структуру, тем большее, чем выше температура. Всякое введение посторонних частиц в структуру, конечно, стремится де стабилизировать ее, вызывая в ней напряжения, но для малых количеств примеси энтропийный положительный эффект всегда превышает потери, затрачиваемые на «содержание» примеси. Поэтому ни одно природное со единение без особых причин не может «отказаться» от присутствия хотя бы небольших порций посторонних атомов в структуре, тем более, когда состав минералообразующей системы обеспечивает широкий выбор наи более подходящих примесных атомов.
Лишь отдельные индивиды минералов, формирующиеся в специфи ческих условиях природной дистилляции, приближаются к соединениям постоянного состава. Тем не менее в качестве идеализации многие минера лы полезно условно рассматривать как соединения постоянного состава. Такое абстрагирование от реального состава позволяет использовать по нятие минерального вида и характеризовать индивиды минералов, относя щиеся к определенному минеральному виду, единообразными и относи тельно простыми химическими формулами, отражающими устойчивые особенности их, вообще говоря, непостоянного состава.
К числу бинарных химических соединений относятся: простые окси ды (Cu2O, MgO, Fe2O3, SiO2 и др.), сульфиды (NiS, FeS2, Sb2S3 и др.), гало гениды (NaCl, AgBr, CaF2 и др.) и т. д. Соединения, состоящие из атомов трех элементов, называются тернарными; таковы различные кислород ные соли (Са[CO3], Ca[SO4], Y[PO4], Mg2[SiO4] и др.). Существуют, ко нечно, и соединения более сложного состава.
Химический состав химических соединений может изображаться дво яким способом: 1) в виде эмпирических формул; 2) в виде конституцион ных или структурных формул.
Эмпирическими формулами выражают состав минералов либо в виде символов элементов, входящих в соединение, начиная с наиболее низко валентных катионов и заканчивая наиболее низковалентными анионами (например, Ba[SO4], Na3[AlF6], Na[AlSi3O8] и т. д.), либо в виде ряда прос тейших составляющих соединений (BaO . SO3, 3NaF . AlF3, Na2О . Al2O3.
. 6SiO2 и т. д.). Последний вид формул хотя и не отвечает современным
Глава 2. Конституция и свойства минералов |
55 |
представлениям о природе химических соединений, однако имеет то пре имущество, что позволяет легче запомнить состав минералов и в удоб ной форме записывать уравнения реакций с их участием.
Существенные поправки в начертание формул более сложных соеди нений вносят данные кристаллохимии, основывающиеся на рентгено структурном изучении минералов. Так как большинство неорганических кристаллических веществ характеризуется ионными связями структур ных единиц, то в сложных формулах химических соединений важно от ражать эти структурные элементы (катионы и анионные комплексы), устанавливаемые в различных типах кристаллических структур. Анион ные комплексы обычно отделяются от катионов квадратными скобками, гидроксильная группа — круглыми, например, Са[СО3], Ba[SO4], Na[AlSi3O8], Mg3[Si4O10](OH)2 и т. п. Нередко в подобных формулах до полнительно отражается топология анионных комплексов, для чего пос ле скобок располагаются в виде верхних индексов несколько знаков ∞; их количество соответствует числу измерений, в которых простирается анионная группировка. Так, наличие цепочечного (одномерного) крем некислородного радикала в структуре минерала группы пироксенов — ди опсида — передается в его формуле следующим образом: CaMg [Si2O6]∞. Присутствие слоевых (двумерных) радикалов в структуре талька отра жается в его формуле так: Mg3[Si4O10]∞∞ (OH)2.
Во многих случаях по таким кристаллохимическим формулам мы можем заранее догадываться о тех или иных физических свойствах со единения. Известно, например, что оптические свойства (в частности, двупреломление) часто зависят от формы анионного комплекса и его ориентировки. Наличие в кристаллической структуре параллельно ори ентированных анионов плоской формы [СO3]2– или [Si2O5]2– обуслов ливает высокое двупреломление (сильно выраженную оптическую ани зотропию при отрицательном оптическом знаке). Если же анион представлен группой изометрической формы [SO4]2– или каркасом [AlSi3O8]1–, развитым в пространстве более или менее равномерно, то такие минералы обычно обладают низким двупреломлением. Форма комплексных анионов нередко отражается и на облике кристаллов: слю ды, характеризующиеся непрерывно вытянутыми в двух направлениях анионными листами, зачастую характеризуются пластинчатыми фор мами кристаллов, а пироксены, в которых анионы представлены непре рывно вытянутыми в одном направлении цепочками, обладают призма тическим обликом кристаллов и т. д.
Помимо бинарных и тернарных химических соединений, в природе распространены и более сложные соединения, например, двойные соли. Двойными солями называются такие соединения постоянного состава, которые состоят как бы из двух простых солей, присутствующих в крат ных отношениях. В большинстве случаев эти соли являются двойными
56 |
Общая часть |
по катионам, реже — по анионам или одновременно по катионам и анио нам. В качестве примеров могут быть приведены следующие: CaMg[CO3]2, K3Na[SO4]2 и т. д.
При сравнении формул двойных солей выясняется, что входящие
вих состав катионы, благодаря значительной разнице их ионных радиу сов, не могут изоморфно замещать друг друга: Са2+(1,04 Е) и Mg2+(0,74 Е), К1+(1,33 Е) и Na1+(0,98 Е) и т. д. Поэтому неудивительно, что от составля ющих их простых солей двойные соли отличаются некоторыми особен ностями кристаллических структур и физическими свойствами.
Соединения переменного состава (твердые растворы, смешанные кристаллы, изоморфные смеси). Кроме химических соединений посто янного состава, получаемых обычно в лабораториях с использованием чистых исходных компонентов, существует огромное множество таких соединений, состав которых не является постоянным, а колеблется то в узких, то в более широких пределах, причем эти колебания состава не могут быть объяснены наличием каких либо механических примесей по сторонних веществ. Наоборот, колеблющийся состав соединений с кри сталлохимической точки зрения находит объяснение в растворимости составных компонентов в данном соединении. Такие химические обра зования получили название соединений переменного состава.
Среди минералов соединения переменного состава составляют боль шинство. Существование веществ (фаз) переменного состава кажется вполне естественным, если речь идет о жидких растворах, состав кото рых определяется соотношением количеств растворенного вещества и растворителя. Таким образом, состав раствора колеблется в пределах от чистого растворителя до насыщенного раствора; он может быть любым из непрерывного множества возможных составов в пределах, зависящих от температуры и давления. Способность кристаллических веществ раз личного состава образовывать непрерывно меняющиеся по составу со единения одинаковой кристаллической структуры основана на изомор' физме, т. е. свойстве атомов различных элементов заменять друг друга
втвердых химических соединениях.
Понятие изоморфизма приложимо как к атомам различных элемен тов, способным выполнять в структуре кристаллов одинаковую кристал лохимическую функцию, статистически размещаясь в позициях одного типа, так и к кристаллам чистых веществ, которые могут образовывать промежуточные произвольные по составу соединения — твердые раство' ры — благодаря изоморфизму составляющих их атомов. Изоморфизм, подобно морфотропии, не должен восприниматься как процесс или об менная реакция, хотя соединение переменного состава и удобно описы вать как продукт реакции замещения или растворения в твердом состоя нии. На самом деле твердые растворы в природе в подавляющем большинстве случаев сразу образуются с максимальным допустимым при
Глава 2. Конституция и свойства минералов |
57 |
данных условиях количеством изоморфных примесей, так что дальней шие процессы могут протекать лишь в сторону распада раствора и избав ления от примесей на фоне падения температуры. Исключение составля ют минералы, находящиеся в условиях нарастающей температуры при прогрессивном метаморфизме.
Область возможных составов твердых растворов, допустимых при фикси рованных значениях термодинамических параметров, вместе с составами чи стых компонентов образует так называемый изоморфный ряд. Со стороны крайних членов изоморфных рядов, представляющих чистые компоненты, область допустимых составов всегда имеет непрерывный характер, в облас тях же промежуточных составов может наблюдаться область несмесимости; в таких случаях говорят о существовании разрыва смесимости в ряду твер дых растворов. При отсутствии области несмесимости изоморфизм называ ется совершенным, в противном случае речь идет об ограниченной смесимо сти и изоморфизм этого типа называется несовершенным.
Вфизической химии давно уже было установлено, что степень смеси мости компонентов зависит от внешних факторов, главным образом от температуры: в условиях высоких температур изоморфное замещение компонентов происходит в гораздо более широких пределах, чем при низ ких температурах. Следовательно, при повышении температуры изомор физм в некоторых рядах может из несовершенного сделаться совершен ным. Тем не менее некоторые компоненты имеют настолько низкую смесимость в твердом состоянии, что повышение температуры не может сделать крайне ограниченный, несовершенный изоморфизм в таких сис темах совершенным — один или оба чистых компонента плавятся или раз лагаются гораздо раньше, чем исчезнет разрыв смесимости.
Вминералогии на зависимость изоморфизма от термодинамических условий впервые обратил внимание В. И. Вернадский в 1910 г. Он указал на существование более широких изоморфных рядов химических элемен тов для области глубинных магматических образований (высокие P и T) по сравнению с областью метаморфических пород в литосфере (высокое P
исредняя T) и с областью выветривания (низкие P и T).
Внастоящее время представления об изоморфизме на основе достиже ний кристаллохимии сильно расширились. Явление изоморфизма имеет несколько взаимосвязанных аспектов, определяющих его многообразие.
Во первых, можно рассматривать изоморфизм в отношении структур ного состояния крайних членов изоморфного ряда. Как предполагалось во время, следовавшее непосредственно после открытия явления изомор физма, для осуществления изоморфной смесимости в широких пределах необходима изоструктурность чистых компонентов, т. е. крайние члены изоморфных рядов должны обладать близкими структурами — относить ся к одному структурному типу. Такое требование и отображено в самом термине изоморфизм, означающем по гречески — равенство формы.
58 |
Общая часть |
Позже выяснилось, что изоморфная смесимость может наблюдаться и между веществами с различными структурными типами. Подобное яв ление получило название — изодиморфизм. Примером системы с изоди морфизмом является непрерывный ряд от кубического Ir до гексагональ ного Os. Смена структурного типа твердого раствора, которую можно рассматривать в качестве морфотропного перехода, осуществляется «скач
ком» при составе приблизительно (Ir0,75Os0,25).
Дальнейшие различия в характере изоморфных замещений могут быть обнаружены при анализе общего числа атомов (или других структурных единиц) в крайних членах изоморфного ряда и в твердом растворе.
Наиболее простым и интуитивно ясным является замещение типа «атом на атом» или «молекула на молекулу» («радикал на радикал» в слу чае изоморфизма по анионной части). Такое замещение происходит с со хранением общего числа атомов (молекул) в системе, а так как при изо морфизме должна сохраняться электронейтральность, то это требует равенства валентностей, точнее, зарядов замещающих друг друга струк турных единиц. Изовалентный изоморфизм, характеризующийся заменой в кристаллической структуре ионов одинаковой валентности, широко проявляется при условии, если свойства и размеры взаимно замещающих ионов близки друг к другу (разность ионных радиусов не превышает 15 % от меньшего радиуса, согласно правилу Гольдшмидта). Таковы, например, двухвалентные катионы (в скобках указаны размеры ионных радиусов): Mg2+(0,74), Fe2+(0,80), Ni2+(0,74), Zn2+(0,83), Mn2+(0,91) и др.; трехвалент ные катионы: Fe3+(0,64), Cr3+(0,64), Al3+(0,57) и др. То же самое относится и к анионам, участвующим в строении кристаллических веществ: S2–(1,82), Se2–(l,93) и др. Из простейших соединений, характеризующихся совер шенным изоморфизмом, приведем следующие ряды: MgCO3 — FeCO3, CuS — CuSe и др.
Гетеровалентный изоморфизм отличается тем, что в кристаллических структурах происходит замена одного иона примерно равновеликим ионом иной валентности, однако при условии компенсации зарядов в какой либо другой паре ионов, участвующих в кристаллическом строе нии данного вещества, но существенно отличающихся по своим разме рам от предыдущих. Таков, например, известный изоморфизм в ряду пла гиоклазов: Na[AlSi3O8] — Ca[Al2Si2O8]. Здесь Na1+(0,98) заменяется большим по валентности Са2+(1,04) при одновременной замене одного иона Si4+(0,39) на меньший по валентности Аl3+(0,57). Гетеровалентный изоморфизм в плагиоклазах может быть описан следующей схемой: Ca2+Al3+ → Na+Si4+. В некоторых рутилах (TiO2) наблюдается одновре менное присутствие примеси Nb5+ или Ta5+ с Fe3+ (ильменорутил или стрюверит соответственно); гетеровалентное замещение происходит в них по следующей схеме: Me5+Fe3+ → 2Ti4+. Таким образом, общий элект ростатический баланс соединения сохраняется. Описанные случаи гете
Глава 2. Конституция и свойства минералов |
59 |
ровалентного изоморфизма также относятся к изоморфизму с сохране нием числа атомов в системе.
При гетеровалентном изоморфизме кроме компенсации заряда реша ющую роль играют все же размеры заменяющих друг друга структурных единиц — катионов или анионов (они должны быть более или менее рав новеликими).
Однако число структурных единиц при замещении не обязательно должно сохраняться. Например, в слюдах на месте трех двухвалентных катионов Mg (в шестерной координации) могут располагаться два трех валентных катиона Al (3Mg замещаются на 2Al). Третье место остается вакантным. В схемы подобных замещений вводится символ незанятой позиции, называемой вакансией — ?. Для описанного замещения в слю дах схема изоморфизма такова: ?2Al3+ → 3Mg2+.
Если рассматривать слюды с подобными изоморфными замещениями в направлении от магнезиальных членов ряда к глиноземистым, мы уви дим, что общее число атомов уменьшается. Такой изоморфизм называется изоморфизмом вычитания, или дефектным изоморфизмом. С другой сто роны, можно рассматривать слюды этого ряда и в обратном направлении, тогда речь будет идти об изоморфизме заполнения (или внедрения), так как в этом случае мы будем переходить к структурам со все большей степе нью заполнения вакансий катионами Mg2+. Ясно, что изоморфизм с учас тием вакансий приобретает характер вычитания или заполнения в зависи мости от способа рассмотрения изоморфного ряда. Определенность здесь может возникнуть, лишь если один из крайних членов подобного твердого раствора вообще не существует в чистом виде. В таком случае мы вынуж дены говорить о дефектной (или заполненной) структуре как о некоторой химической модификации, отклоняющейся по составу от стехиометриче ского состава чистого крайнего члена в направлении недостижимого (ги потетического) соединения. Для большинства же систем с изоморфной сме симостью любого типа, в которых оба крайних члена существуют, особенно при совершенном изоморфизме, допустимо в схемах изоморфных замеще ний применять двустороннюю стрелку вместо односторонней.
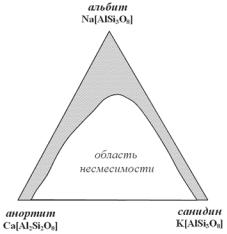
Из вышесказанного ясно, что системы с изоморфными замещениями могут быть и более чем двухкомпонентными. В случае таких систем речь уже идет не о рядах, а о полях и целых областях изоморфной смесимости, как это характерно, например, для полевых шпатов (рис. 8) при высоких температурах, когда смешению подвергаются плагиоклазы и калиевые по левые шпаты.
Как мы знаем, ионные радиусы в вертикальных группах Периодиче ской системы элементов возрастают с увеличением порядкового номера и уменьшаются в горизонтальном направлении с увеличением номера груп пы (т. е. с увеличением валентности). На этом основании А. Е. Ферсманом выведен закон диагональных рядов изоморфных ионов в Периодической
60 |
Общая часть |
Рис. 8. Поле составов твердых растворов высокотемпературных полевых шпатов (выделено крапом)
системе элементов, справедливый для левой ее части. Намечаются следу ющие гетеровалентные ряды изоморфизма ионов (в скобках показаны ион ные радиусы в ангстремах):
Li1+(0,68) — Mg2+(0,74) — Sc3+(0,83) — Zr4+(0,82);
Na1+(0,98) — Са2+(1,04) — Y3+(0,97);
K1+(1,33) — Sr2+(1,20);
Rbl+(l,49) — Ba2+(1,38);
Al3+(0,57) — Ti4+(0,64) — Nb5+(0,66).
Действительно, в природных соединениях мы нередко наблюдаем, что литиевые минералы, например, содержат изоморфные примеси магния, магниевые минералы — примеси скандия, натриевые — примеси кальция, кальциевые — примеси иттрия и т. д.
Кроме того, в комплексных анионах ион [SiO4]4– может заменяться ионами [АlO4]5–, [РО4]3– и [SO4]2–, имеющими одинаковые или близкие размеры. На приведенных примерах мы не раз будем останавливаться при описании минералов.
Исследования А. Е. Ферсмана и В. М. Гольдшмидта показали, что вли яние размерных характеристик атомов на возможность и пределы изо морфных замещений оказывается несимметричным в отношении
/
больших и меньших ионов и связано также с их зарядами (валентнос тью). Это выражено правилом полярности изоморфизма: высокозарядные малые ионы легче (в большем количестве) входят в структуру, чем ионы большего радиуса и с меньшим зарядом.
В настоящее время, во многом благодаря исследованиям акад. В. С. Уру сова, можно считать установленными основные закономерности изоморфиз
Глава 2. Конституция и свойства минералов |
61 |
ма, многие из которых получили объяснение в рамках энергетической кри сталлохимии. Так, выяснено, что весьма существенным фактором изомор фных замещений является близость электронных характеристик замеща ющих друг друга атомов, наиболее просто выражаемая через такие их параметры, как электроотрицательность. Помимо размерного фактора, учи тываемого правилом Гольдшмидта об отличии в радиусах ионов не более 15 %, для обеспечения изоморфной смесимости требуется и близость ве личин их электроотрицательности. Кроме того, для сложных по составу соединений, в которых влияние геометрических параметров замещающих друг друга атомов, благодаря малости доли занимаемого ими общего объе ма в структуре, слабо сказывается на параметрах решетки, требования не более 15 % различия радиусов могут быть существенно смягчены. Установ лен также характер влияния повышенного давления на изоморфизм: пре делы изоморфной смесимости в целом сужаются, однако энергетически выгодным может являться вхождение катиона в структуру минерала, если оно приведет к увеличению координационного числа атомов примеси. Этот эффект иллюстрируется высокой глиноземистостью пироксенов и амфи болов глубоко метаморфизованных пород за счет повышенных содержа ний четырехкоординированного алюминия.
Среди природных соединений переменного состава с генетической и кристаллохимической точки зрения важно различать два типа: 1) ис тинные твердые растворы; 2) микронеоднородные минералы (в том чис ле твердые псевдорастворы, многие из которых представляют собой про дукты распада твердых растворов).
Истинные твердые растворы, или, как их иначе называют, изоморф ные смеси, представляют собой совершенно однородные по кристалли ческой структуре смеси в любых пропорциях двух или нескольких ве ществ, не образующих химических соединений промежуточного состава. Примерами могут служить твердые растворы золота и серебра, оливины, закаленные плагиоклазы вулканического происхождения и т. д.
Физические и химические свойства твердых растворов являются ад дитивными (от лат. addo — прибавляю), т. е. постепенно и закономерно изменяющимися при увеличении содержания второго компонента. Та ковы, например, изменения температуры плавления, удельного веса, по казателей преломления, отражательной способности, электропроводно сти и т. д. Изменения всех этих свойств на диаграммах выражаются в виде практически прямых линий (для удельных весов и параметров решетки) или плавно изгибающихся кривых (температур плавления, оптических свойств и др.). Эти кривые для изоморфных рядов настолько характер ны, что по совокупности изученных свойств какого либо минерального вида переменного состава по ним можно определить состав конкретного индивида, измерив значения его свойств и не прибегая к химическому анализу. Например, нетрудно определить таким путем по специальным
62 |
Общая часть |
диаграммам состав оливина, изучив его оптические свойства в шлифах под микроскопом.
В химических формулах твердых растворов изоморфные атомы или ионы ставят в круглые скобки, отделяя друг от друга запятыми и распо лагая в убывающем порядке содержания: (Au,Ag), (Zn,Fe)S, (Zn,Fe)CO3, (Fe,Mn)WO4 и т. д. Если в двойной соли один из компонентов содержит изоморфные примеси, то формула изображается в следующем виде: Ca(Mg,Fe)[CO3]2.
Приведенные выше формулы твердых растворов, выражающие химизм минералов переменного состава в обобщенном виде, содержат информацию о соотношении изоморфных атомов лишь в порядковой форме (больше — меньше). Химический состав конкретных минеральных индивидов, оцени ваемый по результатам их химического анализа, выражается в так называе мых эмпирических формулах, например, состав одного из клинопироксенов Хибинского массива описывается следующей эмпирической формулой:
(Na0,88Ca0,10K0,02)1,00(Fe3+0,88Mg0,05Al0,03Fe2+0,02Ti4+0,02)1,00 [(Si1,95Al0,05)2,00O6].
Микронеоднородными минералами считаются такие минеральные ин дивиды, неоднородность которых устанавливается лишь при микроско пических исследованиях. Внешне кристаллы подобных минералов могут казаться однородными, однако при микроскопических, а иногда — лишь при электронно микроскопических исследованиях такие минералы об наруживают неоднородное строение. Неоднородности могут быть пред ставлены как минеральными включениями различного масштаба, так и многофазными включениями, представляющими фрагменты минерало образующей среды (расплавные, газово жидкие включения).
Во многих случаях неоднородность минералов является первичной, формируясь непосредственно в процессе их образования в результате за хвата посторонних минеральных частиц и отдельных порций минерало образующей среды через поверхность растущего кристалла. В целом ряде случаев минеральные микровключения занимают ориентированное по ложение относительно кристалла хозяина. Иногда такие включения воз никают при захвате ориентированно наросших (эпитаксических) микро индивидов других минералов (например, тончайшие пластины ильменита или слюды, ориентированные параллельно граням базопинакоида крис таллов корунда). Если ориентированно наросшие минералы впоследствии оказываются заключенными внутри кристалла хозяина, образующиеся вростки называются эндотаксическими. Нередко микроиндивиды посто роннего минерала, имеющие закономерную ориентировку относительно кристалла хозяина, росли одновременно с ним (топотаксия).
Интересный пример неоднородности представляют синтаксические срастания структурно родственных минералов, образующих отдельные блоки, представленные в различных объемных отношениях. Подобное явление на ультрамикроскопическом уровне наблюдается в минералах,
Глава 2. Конституция и свойства минералов |
63 |
представленных монокристаллами, в строении которых участвуют раз личные по составу и строению, но хорошо сочетающиеся между собой регулярно расположенные структурные блоки, присутствующие в крат ных отношениях. Минералы, построенные таким образом, называются полисомами и образуют дискретные ряды — полисоматические серии, например, минералы серии бастнезит паризит. Если полисоматические структуры сложены плоскими блоками (подобно политипам — слоями, но различными по составу), возникают так называемые смешаннослой ные образования, к которым, как показали электронно микроскопические исследования, относятся многие глинистые минералы, ранее считавшие ся однородными.
Всевозможные примеси и дефекты в кристаллах минералов, обладая сами по себе микроскопическими размерами, могут неравномерно рас пределяться в минералах, делая их неоднородными и для невооруженно го взгляда. Как изоморфные, так и механические примеси нередко в раз личных количествах захватываются растущим кристаллом на различных этапах его роста, что приводит к зональному распределению окраски; по добные зоны могут наблюдаться и макроскопически, формируя ритмич но полосчатую зональность. Если примеси неодинаковым образом посту пают в минеральный индивид через различные элементы огранения растущего кристалла (вершины, ребра, различные грани), распределение примесей может иметь секториальный характер.
Весьма распространены в реальных минеральных индивидах и слу чаи вторичной неоднородности, по большей части возникающей в про цессе низкотемпературной эволюции минералов, представлявших при своем возникновении истинные твердые растворы. Так как большинство минеральных индивидов после своего образования претерпевают охлаж дение, пределы изоморфной смесимости сужаются, и твердый раствор начинает испытывать превращения, сводящиеся часто к распаду (экссо люции) с выделением избыточных компонентов в виде новых минераль ных фаз. Например, в экспериментально изученной системе NaCl — KСl эти соединения при высоких температурах образуют непрерывный ряд твердых растворов. Однако при постепенном охлаждении до комнатной температуры в закристаллизовавшейся массе возникают мельчайшие за кономерно сросшиеся тельца NaCl и KСl. Количественные их соотноше ния зависят от исходного состава твердого раствора.
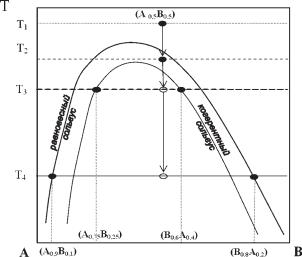
Теоретический состав минеральных фаз, которые должны образовать ся при распаде твердого раствора, определяется на диаграмме «состав — температура» (рис. 9) положением кривой равновесного сольвуса (бино дали). В большинстве случаев образующиеся фазы зарождаются при более низких температурах, чем те, которые задаются равновесным сольву сом. Зарождение индивидов новой фазы в твердом теле требует дополни тельной энергии на преодоление упругих деформаций при согласовании
64 |
Общая часть |
Рис. 9. Эволюция охлаждающегося твердого раствора состава (A0,5B0,5) на субсолидус ной диаграмме «состав — температура» двухкомпонентной системы A–B. При темпера туре T = T1 твердый раствор стабилен. После пересечения кривой равновесного сольвуса твердый раствор находится в метастабильном состоянии (T = T2). Далее зародившиеся при пересечении когерентного сольвуса микровростки, обогащенные компонентом A, достигают при T = T3 состава (A0,75B0,25) и находятся в преобладающей по объему матри це состава (B0,6A0,4). При дальнейшем охлаждении когерентность нарушается и при
T = T3 фазы в срастании характеризуются составами (A0,9B0,1) и (B0,8A0,2) с небольшим преобладанием последней
поверхностей выделяющейся фазы и кристалла матрицы, что достигает ся переохлаждением по сравнению с температурой теоретического «на сыщения»; реальный состав выделяющейся фазы и кристалла матрицы определяется линией когерентного сольвуса. При длительном глубоком переохлаждении структура распада делается более грубой и когерентность может нарушиться, после чего состав сосуществующих фаз достигает ве личин, задаваемых равновесным сольвусом (см. рис. 9).
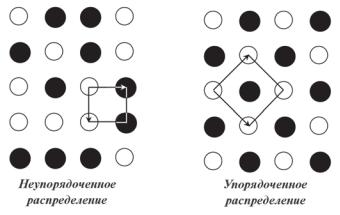
Кроме распадового «сценария» поведения твердого раствора, на фоне снижения температуры возможны процессы упорядочения структуры, при которых изоморфные атомы разных элементов, имевшие в структуре твер дого раствора статистическое (случайное) распределение в позициях од ного типа, начинают перераспределяться в этих позициях, избегая сосед ства с себе подобными. Перераспределение изоморфных атомов, осуществляемое путем диффузии на малые расстояния, приводит к об разованию закономерных конфигураций, так что ранее симметрически эквивалентные позиции, занимавшиеся ионами разных элементов в слу чайном порядке, становятся неравноценными и как бы расщепляются на два или более типов (рис. 10). Процессы упорядочения представляют со бой весьма специфичные непрерывные полиморфные переходы (обычно второго рода), практически всегда приводящие к понижению симметрии
Глава 2. Конституция и свойства минералов |
65 |
Рис. 10. Неупорядоченное (статистическое) и упорядоченное распределение атомов двух сортов. При упорядочении элементарная ячейка изменяет ориентацию
иувеличивает площадь вдвое
икратному увеличению элементарной ячейки (появляется сверхструк тура). В некоторых случаях процессы распада и упорядочения совмеща ются. Так, например, твердые растворы высокотемпературных щелочных полевых шпатов при постепенном охлаждении испытывают распад с вы делением натрового компонента в виде пертитовых вростков альбита, тогда как обогащенная калием матрица, испытывая упорядочение Si и Al по тетраэдрическим позициям, постепенно превращается из моноклин ного ортоклаза в триклинный микроклин.
Выделение новообразованных минеральных фаз из твердых растворов может начинаться с появления чрезвычайно мелкодисперсных, обычно — ориентированных включений, в результате чего образуются твердые ана логи коллоидных растворов — кристаллозоли (черный железистый сфале рит, пигментированный мельчайшими частицами пирротина). В дальней шем новообразования испытывают тенденцию к укрупнению, они растут, подобно обычным кристаллам, выпадающим из пересыщенных жидких растворов, с той лишь разницей, что транспортировка компонентов к ним осуществляется на несколько порядков медленнее, так как диффузия в твер дом теле затруднена.
Процессы зарождения и укрупнения новообразованных фаз, хорошо протекающие при постепенном падении температуры (в эндогенной об становке), могут быть приостановлены или существенно замедлены глу боким и резким охлаждением (например, при вулканизме), которое за медляет процессы диффузии и роста вновь образующихся фаз, так что твердый раствор очень долго потом сохраняется в метастабильном состо янии (например, санидины и анортоклазы из вулканических пород).
Микроиндивиды новообразованных минералов могут в ряде случаев не только не достигнуть крупных размеров, но и, напротив, уменьшиться
66 |
Общая часть |
или вовсе раствориться заново; более того, похожая участь иногда постигает и первичные включения. Подобные явления «рассасывания» механических примесейвозможны,есликристаллминерала хозяинаподвергнетсядлитель ному нагреву, например, в условиях прогрессивного метаморфизма.
Следует отметить и вариант возникновения неоднородностей в мине ралах в процессе внешне обусловленных химических реакций, в частно сти, как результат разложения химического соединения в связи с измене ниями в окружающей среде (например, в оловосодержащем сфалерите — (Zn,Sn)S — в окислительной обстановке возникают мельчайшие включе ния оксида олова — SnO2). Особенно часто включения посторонних мине ралов, как остатков от замещения (реликтов), наблюдаются в кристаллах, образующихся метасоматическим путем в метаморфических породах.
Вполне понятно, что данные химического анализа таких минералов не будут точно укладываться в химические формулы со стехиометриче скими отношениями компонентов. С другой стороны, неоднородности в минералах несут с собой бесценную информацию об условиях формиро вания и последующих изменений минерала, представляя собой одно из важнейших проявлений типоморфизма.
Водные соединения. Предварительно необходимо сделать следующее важное замечание. К числу водных соединений следует относить только такие, которые в своем составе содержат электрически нейтральные мо лекулы воды. Раньше под видом водных соединений рассматривали так же минералы, содержащие гидроксильные анионы [ОН]1–. Однако меж ду молекулой Н2О и отрицательно заряженным ионом [ОН]1– существует, естественно, принципиальная разница, весьма существенно сказывающа яся на физических и химических свойствах минералов. Гидроксил как ион способен заменять в соединениях такие анионы, как F1–, Cl1– и проч но удерживается в кристаллических структурах. Молекула Н2О этим свойством не обладает и, будучи слабо связана в структуре, легко удаля ется при нагревании. То, что гидроксил при прокаливании минералов, его содержащих, покидая кристаллическую решетку, способен превращать ся в пары воды, отнюдь не может служить основанием для отождествле ния его с молекулой Н2O. Поэтому весьма важно в химических формулах минералов раздельно указывать присутствие в них гидроксила и воды. С этой точки зрения, например, малахит — Cu2[CO3][ОН]2 — является не водным, а основным безводным карбонатом меди, хотя при химическом анализе гидроксил определяется в виде Н2О. То же относится к минера лам, представляющим собой кислые соли, в которых в числе катионов находится водород или катион Н3О+ (оксоний).
В зависимости от того, каким способом удерживается вода в минера лах, различают: 1) кристаллизационную, или связанную, воду, входящую в кристаллические структуры минералов; 2) свободную воду, не участву ющую в строении самого кристаллического вещества.
Глава 2. Конституция и свойства минералов |
67 |
Связанная вода в кристаллической структуре участвует в виде молекул Н2О, занимающих в ней строго определенные места. Количество молекул воды находится в простых отношениях к другим компонентам соединения. В качестве примеров можно привести следующие: Na2CO3 . 10H2O (сода), Ca[SО4] . 2H2O (гипс), Ni3[AsO4]2 . 8H2O (аннабергит), Аl2[РО4](ОН)3 . 5Н2О (вавеллит) и др. Это так называемые кристаллогидраты, которые, по Вер неру, должны рассматриваться как «комплексные соединения», т. е. та кие, в которых молекулы воды как структурные единицы располагаются в определенной координации вокруг каких либо ионов, создавая таким путем своего рода комплексные ионы.
Так, в кристаллической структуре соединения Ni[SО4] . 6H2O рентге нометрическими исследованиями установлено, что шесть дипольных молекул Н2О непосредственно окружают катион Ni2+, ориентируясь, оче видно, определенным образом по отношению к катиону (двумя протона ми Н1+ к периферии комплексного иона). Так как молекула Н2О сама по себе электрически нейтральна, то гидратированный катион [Ni(H2O)6]2+ сохраняет заряд Ni2+. Поэтому химическую формулу соединения правиль нее писать так: [Ni(H2O)6][SO4].
На вопросе о причине гидратации ионов в кристаллических структу рах мы остановимся позднее (во введении к кислородным солям). Здесь можно лишь указать, что необходимость гидратации ионов кристаллохи мически строго оправдывается; для образования устойчивых кристалли ческих структур из таких крупных по размерам анионов, как [SO4]2–, при сутствующие в растворе катионы Ni2+ слишком малы, в силу чего и возникает стремление к увеличению их объема без изменения заряда. Само собой разумеется, что образование кристаллогидратов может про исходить лишь в средах, богатых водой, и при низких температурах.
При нагревании кристаллогидраты легко обезвоживаются, если не сразу целиком, то скачкообразно, периодически теряя часть молекул воды. При этом перестройка структуры происходит с сохранением рациональ ных отношений числа молекул Н2О и основного соединения. Например, халькантит Сu[SО4] . 5Н2О при искусственном обезвоживании образует вначале Cu[SО4] . 3H2O, затем Cu[SО4] . H2O и, наконец, Cu[SО4]. При этом скачкообразно меняются и такие физические свойства, как показа тели преломления, удельный вес и др. Из разных соединений вода удаля ется при различных температурах: некоторые из них теряют ее при ком натной температуре (многоводные сульфаты меди и железа), другие — при более высоких и даже при температурах выше 100 °С.
Свободная вода, присутствующая в минеральных массах, характери зуется тем, что не принимает прямого участия в строении кристалличе ского вещества минералов. При нагревании она выделяется постепенно. Различают три вида свободной воды: а) цеолитную; б) коллоидную; в) гигроскопическую.
Цеолитная вода получила свое название от общего названия особой группы минералов — цеолитов, в которых наиболее ярко проявлены
