
- •Оглавление
- •Предисловие
- •ОБЩАЯ ЧАСТЬ
- •Введение
- •Глава 1. Земная кора и особенности ее состава
- •Глава 2. Конституция и свойства минералов
- •2.1. Общие сведения
- •2.2. Химический состав и формулы минералов
- •2.3. Физические свойства минералов
- •Морфологические особенности кристаллов минералов
- •Прозрачность
- •Цвет минералов
- •Цвет черты
- •Блеск и показатель преломления
- •Спайность и излом
- •Твердость
- •Хрупкость, ковкость, упругость
- •Удельный вес
- •Магнитность
- •Радиоактивность
- •Прочие свойства минералов
- •Глава 4. Образование минералов в природе
- •4.1. Общие положения
- •4.2. Геологические процессы минералообразования
- •Эндогенные процессы минералообразования
- •Экзогенные процессы минералообразования
- •Региональный метаморфизм и связанные с ним процессы минералообразования
- •ОПИСАТЕЛЬНАЯ ЧАСТЬ
- •Классификация и номенклатура минералов
- •Класс 1. Простые сернистые и им подобные соединения
- •Класс 2. Сульфосоли
- •Класс 1. Фториды
- •Класс 2. Хлориды, бромиды и иодиды
- •Класс 1. Простые и сложные окислы
- •Класс 1. Нитраты
- •Класс 2. Карбонаты
- •Класс 3. Сульфаты
- •Класс 4. Хроматы
- •Класс 5. Молибдаты и вольфраматы
- •Класс 6. Фосфаты, арсенаты и ванадаты
- •Класс 7. Бораты
- •Класс 8. Силикаты и алюмосиликаты
- •Подкласс Б. Силикаты с изолированными группами тетраэдров SiO4 в кристаллических структурах
- •ЗАКЛЮЧИТЕЛЬНАЯ ЧАСТЬ
- •Глава 1. Минеральный состав земной коры
- •Главнейшая литература по минералогии
- •1. Учебники, учебные и справочные пособия
- •2. Периодические издания
- •3. Сборники и монографии
- •Список наиболее важных минералов по главнейшим металлам (элементам)
258 |
Описательная часть |
изучении их в полированных шлифах под микроскопом, с помощью хи мических анализов, а также рентгенометрических исследований.
П. п. тр. плавятся в магнитный шарик, издавая сильный чесночный запах мышьяка. Разности, богатые кобальтом, разлагаясь в HNO3, при нагревании окрашивают раствор в розовый цвет, а никелевые разности — в желто зеленый цвет.
Происхождение и месторождения. Все эти минералы встречаются
впарагенезисе с другими арсенидами кобальта и никеля исключительно
вгидротермальных месторождениях (типа Шнееберг и др.).
При выветривании за счет скуттерудита и шмальтина образуется эрит рин (Co3[AsO4]2 . 8H2O) в виде примазок розового цвета, а за счет никель скуттерудита и хлоантита — ярко зеленый аннабертит(Ni3[AsO4]2 .
. 8H2O).
Скуттерудит вместе с другими минералами кобальта был встречен
вНижне'Сеймчанском месторождении (Колымский край). В месторож дении Ховуаксы в Туве скуттерудит весьма распросранен, он образует как отдельные кристаллы и вкрапленники в доломитовых жилах, так и участ вует в строении ритмично зональных полиминеральных агрегатов поч ковидно сферолитового строения в тесной ассоциации с раммельсберги том, никелином и др. арсенидами и сульфоарсенидами.
Является обычным минералом в мышьяково кобальтовом месторожде нии Ак'Джилга в Алайском хребте (Южная Киргизия) в ассоциации с глау кодотом, кобальтином, арсенопиритом, пирротином и другими минералами
вкварцевых жилах. Среди месторождений дальнего зарубежья стран следу ет отметить Скуттеруд (Норвегия), где впервые был установлен скуттеру дит в ассоциации с кобальтином и титанитом в оруденелых гнейсах; затем Кобальт в Онтарио (Канада), где, кроме скуттерудита и никельскуттеруди та, встречались также хлоантит и смальтин в ассоциации с другими минера лами кобальта, никеля и серебра; месторождения Рудных гор — Яхимов (Че хия), Шнееберг, Аннаберг (Саксония), Бу'Аззер (Марокко) и др.
Практическое значение. Вместе с другими арсенидами и сульфоар сенидами никеля и кобальта эти минералы встречаются иногда в значи тельных количествах, и в таких случаях представляют несомненный про мышленный интерес.
КЛАСС 2. СУЛЬФОСОЛИ
К этому классу относятся сложные сернистые соединения, по хими ческой конституции похожие на соли. Их называют сульфосолями. По добно оксосолям, в них различают сульфооснования и сульфоангидриды или катионы и комплексные анионы.
Несмотря на большое разнообразие относящихся сюда минералов, в их составе участвует очень небольшое число компонентов.
Раздел II. Сульфиды, сульфосоли и им подобные соединения |
259 |
Роль сульфоангидридов в подавляющем большинстве сульфосолей играют As2S3, Sb2S3 и Bi2S3. Соответственно этому мы имеем и названия соединений: сульфоарсениты, сульфоантимониты и сульфовисмутиты.
Весьма показательно, что в сульфосолях всех этих трех типов в осно вания входят одни и те же металлы, большей частью Cu, Ag и Рb, т. е. наибольшим распространением в природе пользуются сульфосоли меди, серебра и свинца. Исключительно редко встречаются самостоятельные сульфосоли Tl, Hg и Fe, а в виде изоморфных примесей в существенных количествах наблюдаются лишь Zn и Mn.
В очень небольшом количестве устанавливаются также сульфована даты, сульфоарсенаты и сульфоантимонаты меди, т. е. такие сульфосоли, в которых роль сульфоангидридов играют V2S5, As2S5 и Sb2S5 (пятивалент ные ионы).
Все разнообразие сульфосолей обусловливается главным образом тем, что в качественно одинаковых типах соединений устанавливаются раз личные соотношения сульфооснований с сульфоангидридами. Так, на пример, для сульфоантимонитов серебра известны следующие соедине
ния: 12Ag2S . Sb2S3, 9Ag2S . Sb2S3, 5Ag2S . Sb2S3, 3Ag2S . Sb2Ss, Ag2S . Sb2S3 и Ag2S . 6Sb2S3 или, соответственно: Ag24Sb2S15, Ag9SbS6, Ag5SbS4, Ag3SbS3, AgSbS2 и Ag2Sb12S19. Все это совершенно определенные соединения, встре
чающиеся в кристаллах и имеющие разные кристаллические структуры. Основные черты химизм сульфосолей подвержены изменениям
взависимости от атомного веса полуметалла, участвующего в их со ставе. Если сульфоарсениды обычно обладают относительно постоян ным составом, то для сульфоантимонитов, а особенно для сульфовис мутитов характерны непостоянство состава с замещением части серы селеном, свинца — висмутом и наоборот, что ведет к заметной несте хиометричности таких соединений.
Кристаллические структуры сульфосолей, подобно кислородным со лям в сравнении с окислами, должны отличаться от простых сернистых соединений тем, что в сульфосолях в качестве структурных единиц должны участвовать, казалось бы, лишь компактные анионные группы,
например [SbS4]5–, [SbS3]3– и т. д. В наиболее простых кубических и три гональных кристаллических структурах сульфосолей действительно ус тановлены такие анионные группы, не вполне, впрочем, изолированные, а включенные в большинстве случаев в плотнейшую анионную упаков ку, в той или иной степени искаженную или прореженную. Отклонению от обычной для сульфидов правильной координации служит распрост раненная форма сульфоанионов — тупых тригональных пирамид или «зон
тиков» (подобнокомплексныманионам[SO3]2– всульфитах)[AsS3]3–,[SbS3]3– и [BiS3]3–, где As, Sb и Bi трехвалентны. Такие группы имеются, например,
вструктурах прустита (Ag3[AsS3]), пираргирита (Ag3[SbS3]), тетраэдрита (Cu3[SbS3]) и др. Такие зонтичные сульфоанионы обладают явной полярностью,
260 |
Описательная часть |
имея в качестве одной из четырех вершин атом полуметалла. Вопрос о том, почему в описываемых сульфоанионах с неполновалентными полу металлами As3+, Sb3+ и Bi3+ не реализуется плоскотреугольная координа ционная группировка серы, подобно тому, как это осуществляется в кар бонат ионе [CO3]2 , требует для ясного ответа рассмотрения электронной конфигурации полуметаллов.
Ковалентная полярная связь атомов в молекулах сульфидов As3+, Sb3+ и Bi3+ требует максимального взаимного удаления трех отрицательно за ряженных связывающих электронных пар, направленных к атомным ос товам S2 . От связывающих пар отталкивается и не участвующая в хими ческой связи неподеленная электронная пара, принадлежащая каждому из катионов полуметалла, т. к. они не полновалентны (сравните As5+ и As3+, различающиеся как раз на два электрона). Неподеленная пара занимает значительный объем, она и образует недостающую четвертую вершину в координационном тетраэдре, образовавшемся вокруг атома полуметалла при участии трех анионов S2 , дающих только три вершины. Не принимая во внимание неподеленную пару, мы описываем координацию полуме талла как пирамидальную, или «зонтичную».
Размещение неподеленных электронных пар осуществляется неред ко за счет пропуска анионов S2 в плотнейших упаковках, наследуемых сульфосолями от структур родоначальных сульофоснований. Сразу от метим, что неподеленные пары, сцепленные с атомами полуметаллов, способны к образованию между собой слабых вандерваальсовских связей, чем способствуют соединению отдельных молекул в таких сульфидах по луметаллов, как аурипигмент, антимонит и висмутин. Поэтому неподелен ные электронные пары, выталкиваясь из толщи молекул жестко локализо ванными связывающими парами, сами склонны к некоторой конденсации в промежутках между молекулами в структурах аурипигмента, антимони та и висмутина. При отсутствии неподеленных электронных пар (т. е. в слу чае полновалентных ионов элементов V группы Периодической системы) формируются высокосимметричные тетраэдрические анионные группы [VS4]3–, [AsS4]3–, [SbS4]3– , где V, As и Sb пятивалентны.
В отличие от кислородных комплексных анионов, комплексные суль фоанионы характеризуются нередко меньшей компактностью, что связа но, очевидно, с более слабой поляризующей способностью катионов As3+, Sb3+, Bi3+, V5+, As5+ и др. Отдельные координационные группировки полу металлов (особенно Sb и Bi) с серой не всегда остаются в изолированном виде, но могут конденсироваться с образованием сложных построек раз личной формы и строения — полианионов. Так, структуры многих вис мутовых и сурьмяных сульфосолей содержат комплексные анионы в виде протяженных в одном или в двух измерениях фрагментов, как бы выре занных из структур антимонита и висмутина. Катионные части структур также нередко отвечают фрагментам структур простых сульфидов, выс
Раздел II. Сульфиды, сульфосоли и им подобные соединения |
261 |
тупающих в качестве сульфооснований. Анионные и катионные фрагмен ты соединяются между собой достаточно прочными связями в относи тельно компактные блоки. Структурная группировка сульфосолей мо жет быть произведена по топологии анионных и катионных мотивов в структуре, с различением координационных, слоистых и ленточно цепо чечных сульфосолей.
Структурные типы различных сульфосолей формируются в резуль тате довольно сложного компромисса, устанавливающегося между кон курирующими тенденциями, ведущими к переносу в результирующий мотив черт, присущих родоначальным структурам сульфооснований и сульфоангидридов, в зависимости от количественного преобладания того или другого. В результате формируются устойчивые структурные блоки, состоящие из фрагментов структуры сульфооснований, «одетых» снару жи в слои анионных радикалов, близких по строению к структурам суль фоангидридов.
При этом в сульфосоли переходят из молекулярных структур сульфоан гидридов и неподеленные электронные пары, стремящиеся нередко к кон денсации в виде лент или слоев, требующих объема. При этом связь между электронейтральными блоками становится достаточно слабой. Поэтому мотивы взаимного расположения структурных блоков в таких сульфосолях напоминают узор паркета, что в какой то мере согласуется с правилами акад. А. И. Китайгородского о взаимной укладке молекул в органических крис таллах: выступами одних к промежуткам между другими.
Физические свойства сульфосолей отличаются от свойств сульфидов металлов некоторыми особенностями. По сравнению с простыми сернисты ми соединениями они в общей массе обладают меньшей твердостью (осо бенно сульфосоли низших сингоний, к которым принадлежат большинство минералов), гораздо более легкой разлагаемостью кислотами, относительно низкой отражательной способностью. Все эти свойства, несомненно, связа ны с особенностями конституции этих соединений. Так, при переходе от суль фидов металлов — минералов с высоким средним атомным номером, повы шающим степень металличности связи, к сульфосолям — соединениям с участием ковалентных сульфоангидридов, средний атомный номер пони жается и металлические свойства (непрозрачность и высокая отражатель ная способность, ковкость и проводимость) могут проявляться в меньшей степени. Так, некоторые мышьяковые и сурьмяные сульфосоли Ag имеют алмазный блеск и просвечивают красным цветом. Твердость же падает по причине возрастания доли слабых связей и разрыхления структуры неподе ленными парами, а конденсация последних вдоль определенных направле ний приводит к появлению отчетливой спайности.
При классификации сульфосолей наиболее рациональным является разделение их на большие группы по металлам, участвующим в сульфо основаниях, и уже внутри таких групп можно проводить систематику по
262 |
Описательная часть |
составу сульфоангидридов. При такой установке классификацию суль фосолей можно свести к следующему.
A.Сульфосоли меди, т. е. соединения типа nCu2S . X2S3, где X = As3+, Sb3+и Bi3+, и типа ЗСu2S . Х2S5, где X = V5+, As5+ и Sb6+. Таким образом, сюда войдут сульфоарсениты, сульфоантимониты и сульфовисмутиты меди, а также сульфованадаты, сульфоарсенаты и сульфоантимонаты меди.
Б. Сульфосоли серебра: nAg2S . X2S3, где X = As3+, Sb3+ и Bi3+ — сульфо арсениты, сульфоантимониты и сульфовисмутиты серебра.
B.Сульфосоли свинца. nPbS . X2S3, где X = As3+, Sb3+ и Bi3+ — сульфоар сениты, сульфоантимониты и сульфовисмутиты свинца.
Также существует, разумеется, множество поликатионных сульфосо лей, например двойных, которые здесь приходится рассматривать услов но отнесенными к какому либо из вышеперечисленных разделов по од ному из металлов, принятому за главный.
1. Группа тетраэдрита (блеклые руды)
Относящиеся сюда минералы представлены обширной изоморфной группой так называемых блеклых руд с общей химической с приближен ной формулой A3ХS3 или 3A2S . Х233, где A = Сu+, в меньшей степени Ag+, Cu2+, Zn2+, Fe2+, Hg2+, a X = As3+ и Sb3+, иногда Te5+ (в голдфилдите) и редко Bi3+ (в очень незначительных количествах). Сера изредка может в сущест венных количествах замещаться селеном (в хаките и жиродите).
Более точной формулой, согласно рентгенометрическим данным, долж на быть: A+10A2+2Х4S13. С этим вполне согласуется некоторый избыток серы, устанавливаемый при точных химических анализах блеклых руд. Нако нец, отметим, что из 12 позиций, отведенных для металлических катионов, две должны быть заполнены двухвалентными катионами. В этих двух по зициях происходят изовалентные изоморфные замещения, не зависящие от изоморфизма в сульфоанионе (исключая замещение Te4+>X3+, требу ющее сопряженного изоморфизма в катионной группе для поддержания электронейтральности). Доминирование какого либо из двухвалентных элементов в этих позициях приводит к необходимости выделения соот ветствующего минерального вида, что в сочетании с изоморфизмом полу металлов в сульфоанионе приводит к значительному разнообразию.
Так как медь обладает валентностью один или два, то все позиции ка тионов могут быть заняты одним этим элементом; так в большинстве слу чаев и происходит. В зависимости oт того, какой из сульфоангидридов преобладает в таких соединениях, различают следующие два наиболее распространенных минеральных вида: теннантит (Cu12As4S13) и тетра' эдрит (Cu12Sb4S13). Наибольшим распространением в породе пользуют ся так называемые смешанные блеклые руды состава Cu12(As, Sb)4S13.
Кристаллическая структура блеклых руд довольно сложная, но мо жет в общих чертах быть выведена на основании кубической плотней
Раздел II. Сульфиды, сульфосоли и им подобные соединения |
263 |
шей упаковки с расположением катионов в половине тетраэдрических пустот одной ориентации, что делает общий мотив структуры и облик кристаллов близкими к таковым у сфалерита.
Параметр кубической ячейки блеклых руд приблизительно вдвое боль ше параметра ячейки сфалерита. Содержимое элементарной ячейки блек лой руды, как показали рентгенография и измерения плотности, соответ ствует двум ее формулам A+10A2+2Х4S13. Структура сфалерита ZnS (см. рис. 94а), после выбора кубической ячейки вдвое большей по ребру, содержит в восемь раз больше атомов: 32 катиона Zn2+ и 32 аниона S2 . Заменив третью часть металлических катионов Zn2+ катионами полуметалла X3+, а прочие катионы одновалентными A+, получим состав A+24X3+8S2 32. Теперь для обес печения зонтичной тройной координации полуметаллов [X3+S2 3] вместо типичной для Zn в сфалерите четверной (тетраэдрической, см. рис. 94в), удалим восемь анионов S2 . Дефекты, образовавшиеся в плотнейшей упа ковке, сосредоточим по четыре, в вершинах двух отдельных пустых тетра эдров, обладающих противоположной по отношению к заполненным тет раэдрам ориентацией (такие тетраэдры соответствуют пустым октантам сфалеритовой ячейки на рис. 94а). Место удаленных анионов S2 занимают неподеленные электронные пары, привнесенные полуметаллом X3+, они несколько стабилизируют нарушенную упаковку.
На этом этапе не только координация полуметаллов понижена до трех, но и половина всех ионов А+, прилегающих к двум пустым пока тетраэдрам, составленным неподеленными парами вместо S2 , лишена полноценного ок ружения, их координация по анионам S2 равна всего двум. Оставшаяся по ловина катионов А+ обладает по прежнему четверной координацией (как у сфалерита). Общий состав элементарной ячейки блеклой руды теперь мо
жет быть выражен, как A+24X3+8S2 24 или A+24[X3+S2 3]3 8.
Для окончательной стабилизации дефектной плотнейшей упаковки вве дем по одному дополнительному аниону S2 в центр каждого из двух пустых тетраэдров обратной ориентации, вокруг которых сосредоточены заменяю щие серу неподеленные пары. Это повысит координацию половины ато мов A+ от двух до трех. Но после введения 2S2 для соблюдения электроней тральности необходимо повысить заряд катионной части на четыре единицы, для чего четыре катиона А+ из числа трехкоординированных заменяются на катионы А2+. Теперь содержимое ячейки будет A+20A2+4[X3+S2 3]3 8S2, или иначе, — A+20A2+4X3+4S2 26. Легко видеть, что это удвоенная точная формула блеклых руд, приведенная в начале описания группы. Итак, структуру блек лой руды можно, подобно структурам сфалерита или халькопирита, счи тать координационной, чем определяются многие ее свойства, от изомет ричного облика кристаллов до отсутствия спайности.
Все минеральные виды, относящиеся к данной группе, имеют много общего в физических свойствах, поэтому ниже мы дадим совместное описание лишь двух главных представителей группы.

264 |
Описательная часть |
ТЕННАНТИТ — Cu+10Cu2+2As4S13. Название по фамилии химика Тен нанта.
ТЕТРАЭДРИТ — Cu+10Cu2+2Sb4S13. Название дано по форме встреча ющихся кристаллов, обычной вообще для блеклых руд разного состава.
Химический состав. В составе различных блеклых руд наблюдаются следующие колебания в содержании отдельных элементов (в %):
Cu ... 22–53; |
Hg ... 0–17,0; |
As ... 0–20,0; |
Ag ... 0–18; |
Ni ... 0–3,5; |
Sb ... 0–29,2; |
Zn ... 0–9; |
Co ... 0–4,2; |
Bi 0–4,5 (13,07); |
Fe ... 0–13; |
Mn ... 0–1,5; |
S ... 20,6–29,1. |
При замещении атомов одновалентной меди серебром на основе тет
раэдрита можно получить фрайбергит — (Ag+,Cu) |
12 |
Sb |
S |
13 |
; а при изомор |
|
4 |
|
|
||
физме Zn2+→ Cu2+ или Hg2+ → Cu2+ — зандбергерит или швацит соответ |
|||||
ственно. |
|
|
|
|
– |
Сингония кубическая; гексатетраэдрический в. с. 3L2 |
|
|
|||
L36P. Пр. гр. I43m |
|||||
|
|
4 |
|
|
|
(T 3d). a0 = 10,196 (для теннантита) и 10,400 (для тетраэдрита). В изомор фной серии теннантит — тетраэдрит размер элементарной ячейки увели чивается по мере замещения мышьяка сурьмой и меди серебром. Крисj таллическая структура см. выше, в описании группы.
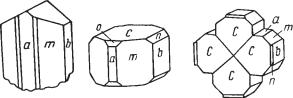
Встречающиеся в пустотах кристаллы имеют тетраэдрический облик
–
(рис. 129) с комбинацией форм: {111}, {111}, {110}, {112}, {100} и др. Обыч но встречается в сплошных массах или в виде вкраплений неправильной формы зерен. Часты двойники по (111), реже по (100).
Цвет стально серый до железно черного (богатых Fe разностей). Для богатой ртутью блеклой руды — швацита, характерна побежалость в си них тонах. Черта имеет тот же цвет, иногда с буроватым и даже вишнево красным оттенком (для теннантита). Непрозрачен. Блеск металлический, тусклый до полуметаллического.
Твердость 3–4. Обладает хрупкостью. Спайность практически отсут ствует. Уд. вес 4,4–5,4. Мышьяковистые разности по сравнению с сурь мянистыми обладают меньшими удельными весами. Прочие свойства. Обладает слабой электропроводностью.
Рис. 129. Кристаллы тетраэдрита
Раздел II. Сульфиды, сульфосоли и им подобные соединения |
265 |
Диагностические признаки. Характерными особенностями являют ся следующие: блеклый тон в изломе и явно проявляющаяся хрупкость (при царапании ножом черта «пылится» и не оставляет блестящего сле да, как это наблюдается у халькозина и аргентита, похожих по некоторым признакам на блеклые руды). По цвету и хрупкости похожи также на бур нонит (CuPb[SbS3]), обладающий меньшей твердостью и несколько бо лее сильным блеском.
П. п. тр. на угле блеклые руды легко плавятся в серый королек с выде лением As2O3 и Sb2O3. Королек дает реакцию на медь и часто на железо. В HNO3 разлагаются с выделением S и Sb2O3. Отношение к реагентам ме няется в зависимости от состава.
Происхождение и месторождения. Блеклые руды, особенно тетраэдрит, принадлежат к числу сравнительно распространенных минералов среди раз личных типов гидротермальных месторождений меди. В подчиненных ко личествах они присутствуют в самых разнообразных по составу рудах. Па рагенетически чаще всего связаны с халькопиритом, реже сфалеритом, галенитом, пиритом, арсенопиритом, бурнонитом и другими минералами.
При выветривании месторождений легко разлагаются, давая различ ные продукты изменений: ковеллин, малахит, азурит, лимонит; за счет мышьяка образуется скородит (Fe[AsO4] . 2H2O); за счет сурьмы — ее окислы и гидроокислы.
Блеклые руды на территории России широко распространены. Они встречаются во всех медных и свинцово цинковых месторождениях, од нако редко образуют крупные скопления. Наибольший интерес по богат ству блеклыми рудами представляют месторождения, известные под названием Благодатные рудники (к северо востоку от Екатеринбурга). С блеклыми рудами этих месторождений связано наибольшее обогаще ние золотом. В составе их участвуют сурьма и мышьяк. Они ассоцииру ют главным образом с пиритом, халькопиритом и отчасти с галенитом. Хорошо образованные кристаллы тетраэдрита встречаются в друзовых пустотах в Березовском золоторудном месторождении. Кристаллы тен нантита встречались в полых трещинах во многих колчеданных залежах Среднего Урала. Блеклые руды составляют заметную часть вольфрамо носных высокотемпературных кварцевых жил Джидинского месторожде ния (Бурятия). Фрайбергит отмечен в рудах Лермонтовского месторож дения (Приморье).
Тетраэдрит известен также в сульфидных жилах Нагольного кряжа (Украина) и Джезказгана (Казахстан).
Практическое значение. Крупные самостоятельные месторождения блеклых руд не встречаются. В промышленных месторождениях они вме сте с другими медьсодержащими сернистыми соединениями являются источником меди. При плавке медных руд, содержащих теннантит, в от ходящих газах улетучивается вредная примесь — мышьяк в виде As2O3.
266 |
Описательная часть |
To же самое происходит, конечно, за счет арсенопирита, энаргита и дру гих мышьяксодержащих соединений, встречающихся в рудах в виде при месей. На крупных производствах этот «газовый мышьяк» в целях обезв реживания продуктов возгона улавливается, и таким путем могут попутно получаться значительные количества этого вида сырья.
2. Группа энаргита
Эта группа представлена соединениями типа Cu3XS4 (2Cu3XS4 = = 3Cu+2S+X2S5), где Х = V, As и Sb, пятивалентные. К этой группе принад лежат несколько минеральных видов, относящихся к структурным ти пам, родственным сфалериту и халькопириту, в их числе кубический суль' ванит Cu3[VS4] и тетрагональные люцонит Cu3[AsS4] и фаматинит Cu3[SbS4], образующие изоморфный ряд. Мы рассмотрим лишь энаргит, диморфный с высокотемпературным люцонитом.
ЭНАРГИТ — Cu+3[As5+S2 4]. «Энаргис» по гречески — явственный (по видимому, имелась в виду ясно выраженная спайность минерала).
Химический состав. Сu — 48,3 %, As — 19,1 %, S — 32,6 %. Примеси: Sb (до 6,5 %), Fe (до 5,7 %), в ничтожных количествах Pb, Zn и Ag (воз можно, за счет включений посторонних минералов).
Сингония ромбическая; ромбо пирамидальный в. с. L22P. Пр. гр. Pnm21(C 72v). a0 = 6,46; b0 = 7,43; с0 = 6,18. Кристаллическая структура по хожа на структуру вюртцита, отличается упорядоченным размещением атомов металла и полуметалла по тетраэдрическим пустотам плотнейшей упаковки S2 и рассматривается как координационная псевдогексагональ ная. Одинаковая тетраэдрическая координация катионов металла и по луметалла позволяет считать энаргит и другие соединения его группы не столько сульфосолями, сколько двойными сульфидами (металла и полу металла), так как здесь атом полуметалла не участвует в формировании комплексной анионной группировки, а исполняет одинаковую с метал лом кристаллохимическую роль.
Встречающиеся кристаллы большей частью имеют столбчатый с вер тикальной штриховкой, реже таблитчатый облик; образованы комбина циями следующих форм: {110}, {001}, {100}, {010} и др. Обычно встреча ются в зернистых сплошных массах и в виде вкраплений.
Цвет энаргита стально серый до железно черного. Черта серовато черная. Непрозрачен. Блеск полуметаллический, сильный.
Твердость 3,5. Хрупок. Спайность совершенная по {110}, довольно ясная также по {010}. Уд. вес — 4,4–4,5. Прочие свойства. Обладает сла бой электропроводностью.
Диагностические признаки. По внешним признакам больше всего похож на черный сфалерит, от которого отличается по спайности, совер шенной лишь в одном направлении, и более сильному блеску.
П.п. тр. на угле плавится, давая налет As2O3, а с содой — королек меди.
ВHNO3 растворяется с выделением всплывающей серы.
Раздел II. Сульфиды, сульфосоли и им подобные соединения |
267 |
Происхождение и месторождения. Встречается иногда в значительных массах в гидротермальных месторождениях меди в ассоциации с блеклыми рудами, халькопиритом, галенитом, пиритом и другими минералами.
Нередко устанавливаются псевдоморфозы теннантита по энаргиту, называвшиеся «зеленым энаргитом». Сравнивая химические формулы этих минералов, легко видеть, что при этом процессе, совершающемся в эндогенных условиях, происходит лишь превращение As2S5 в As2S3.
Взоне окисления месторождений легко разлагается, образуя малахит, азурит, оливенит (арсенат меди) и другие вторичные минералы.
Вместорождениях России энаргит встречается в виде незначитель ной примеси в рудах месторождений преимущественно колчеданной фор мации (Средний Урал), а также в гидротермальных жилах оловорудного месторождения Хапчеранга (Читинская обл.). Отмечен в полиметалли ческом месторождении Невское (Магаданская область) в парагенезисе
ссульфоселенидами и сульфосолями свинца и серебра. Из иностранных месторождений, в которых энаргит представлял крупные промышленные скопления, отметим следующие: Бьютт, Монтана (США), Чукикамата (Чили), Цумеб (Намибия) и др.
Практическое значение. В тех случаях, когда встречается в больших количествах, является рудой на медь и мышьяк.
3. Группа бурнонита
Сюда относятся двойные сульфосоли меди и свинца типа CuPbXS3— бурнонит и айкинит.
БУРНОНИТ — CuPbSbS3. Синоним: бертонит.
Химический состав. Сu — 13,0 %, Рb — 42,5 %, Sb — 24,7 %, S — 19,8 % Примеси: Fe (до 5 %), Ag (до 3 %), следы Zn и Mn.
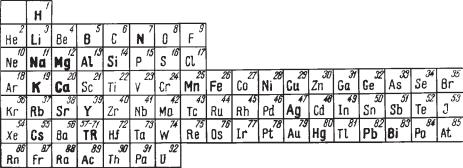
Сингония ромбическая; ромбо дипирамидальный в. с. 3L23PC. Пр. гр. Pnm21(C 72v). а0 = 8,19; b0 = 8,67; с0 = 7,74. Хорошо образованные кристаллы наблюдаются только в пустотах и часто имеют псевдотетрагональный или толстотаблитчатый облик (рис. 130) с развитыми гранями форм {001}, {010}, {100}, {011}, {110} и др. Двойники по (110) часты. Нередко образует повторяющиеся крестообразные или колесоподобные кратные двойни ки (в старой русской литературе по минералогии бурнонит назывался «колесной рудой»). Обычно встречается в неправильных зернах или
Рис. 130. Кристаллы и двойник бурнонита: a {100}, n {011}, m {110}, b {010}, c {001}, o {101}
268 |
Описательная часть |
в сплошных массах. Кристаллическая структура: сходна со структурой антимонита: Сu сосредоточена в тетраэдрах анионной упаковки, место атомов Sb антимонита занято Pb и Sb через один.
Цвет бурнонита стально серый до свинцово серого, нередко с томпа ково бурой побежалостью (на гранях кристаллов). Черта серая. Непро зрачен. Блеск металлический.
Твердость 2,5–3. Хрупок. Спайность несовершенная по {010}. Уд. вес 5,7–5,9. Прочие свойства. Электричество не проводит.
Диагностические признаки. По внешним признакам несколько по хож на блеклые руды, но обладает более сильным блеском.
П. п. тр. на угле с содой легко плавится в черный шарик, который по удалении всего свинца (при осторожном сильном нагревании в сплаве борной кислоты) с трудом дает королек меди. Черный шарик при силь ном нагревании с KJ дает желто зеленый налет PJ2. В HNO3 растворяется с выделением S и Sb2O3.
Происхождение и месторождения. Встречается в гидротермальных мес торождениях свинцово сурьмяных руд. Обычно тесно ассоциирует с тетраэд ритом и галенитом, выделяясь иногда в виде кайм на границах между ними.
Взоне окисления месторождений легко разлагается; за счет его могут образоваться малахит, церуссит (PbCO3) и окислы сурьмы.
ВРоссии бурнонит в заметных количествах встречается в Дарасунском золоторудном месторождении (Восточное Забайкалье) в рудах, состоящих из блеклой руды, галенита и др. Известен также с галенитом и буланжери том в рудах Нежданинского месторождения в Верхоянье (Якутия).
Отмечен в кварцевых жилах Нагольного кряжа (Украина) в ассоциа ции с галенитом, блеклыми рудами, буланжеритом, джемсонитом и др. Среди иностранных месторождений в более значительных массах встре чался в Пршибраме (Чехия), Клаусталле и Андреасберге в Гарце (Герма ния) и во многих месторождениях США, Мексики, Перу, Чили и др.
Практическое значение. В случае крупных скоплений представляет промышленный интерес как руда свинца и меди.
АЙКИНИТ — CuPbBiS3. Впервые был открыт на Урале в начале XIX в. Синоним: патринит.
Химический состав. Сu — 11,0 %, Рb — 36,0 %, Bi — 36,2 %, S — 16,8 %. Примеси: Те и Аu (последнее в виде включений).
Сингония ромбическая; ромбо дипирамидальный в. с. 3L23PC. Пр. гр.
Рптa(D162h). а0 = 11,364; b0 = 11,832; с0 = 8,05. Часто наблюдается в игольча тых и шестоватых кристаллах, вросших в кварц, иногда в сплошных мас сах. На гранях нередко заметна вертикальная штриховка.
Цвет айкинита свинцово серый до стально серого, нередко с бурова той или коричневатой побежалостью. Черта серовато черная, блестящая. Непрозрачен. Блеск металлический.
Твердость 2–2,5. Хрупок. Спайность несовершенная по {010}. Уд. вес 6,1–6,7.
Раздел II. Сульфиды, сульфосоли и им подобные соединения |
269 |
Диагностические признаки. Характерна игольчатая или шестоватая фор ма кристаллов, но без химических реакций на Bi, Pb и Сu узнать его трудно.
П. п. тр. легко плавится, дымится, покрывает уголь белым и желтым налетом. Оставляет металлический королек, который в сплаве борной кислоты с трудом дает королек меди. Реакция на Bi с KJ. В HNO3 раство ряется, выделяя PbSO4 и серу.
Происхождение и месторождения. Минерал редкий. Встречается в кварцевых жилах гидротермального происхождения в ассоциации с пири том, халькопиритом, блеклыми рудами, галенитом, арсенопиритом, самород ным золотом, иногда шеелитом, вольфрамитом и другими минералами.
Большой известностью пользуются шестоватые и игольчатые крис таллы айкинита в прозрачных или полупрозрачных кристаллах кварца в Березовском золоторудном месторождении (к северо востоку от Екате ринбурга). В парагенезисе с ним нередко наблюдаются галенит, блеклые руды, пирит, халькопирит и часто самородное золото. Отмечен с вольф рамитом, пиритом, сфалеритом, родохрозитом и триплитом в кварцевых жилах Джиды (Бурятия).
В зоне окисления неустойчив. В результате разрушения по айкиниту образуются землистые желтые или зеленовато желтые массы так назы ваемых висмутовой и свинцовой охр.
Практическое значение. Сам по себе представляет лишь минерало гический интерес. В Березовском месторождении нахождение его в жи лах служит хорошим признаком их золотоносности.
4. Группа прустита
К данной группе относятся сульфоарсениты и сульфоантимониты серебра типа Ag3XS3, где X = As и Sb.
Из них более распространены в природе изоструктурные прустит и пи раргирит. Несмотря на то что оба минерала имеют аналогичные химические формулы и кристаллизуются в одном виде симметрии, все же, судя по данным химических анализов, они не образуют непрерывного ряда изоморфных сме сей. Лишь при высоких температурах, как показывают экспериментальные исследования, оба эти соединения неограниченно смешивают друг с другом.
Здесь же кратко опишем редкие сульфосоли серебра — стефанит и полибазит.
ПРУСТИТ — Ag3AsS3. Назван по фамилии химика Пруста, впервые установившего, что существуют раздельно мышьяковая и сурьмяная «красные серебряные руды».
Химический состав. Ag — 65,4 %, As — 15,2 %, S — 19,4 %. По имею щимся анализам, содержание Ag колеблется в пределах 63,4–67,6 %, As — 12,3–20,2 % и S — 13,1–20,2 %.
Сингония тригональная; дитригонально пирамидальный в. с. L33Р. Пр. гр. R3с (C 63v). a0 = 10,77; с0 = 8,67. Кристаллическая структура характери

270 Описательная часть
зуется тем, что группы AsS3 занимают каждый угол ромбоэдрической ячейки и центр. Каждая такая группа представлена низкой пирамидой с вершиной As. Вершины всех пирамид направлены вдоль тройной оси, при этом пирамиды, не будучи связаны непосредственно между собой, обра зуют вертикальные колонки, соединенные между собой катионами сереб ра. Последние, в свою очередь, образуют вертикальные спиральные це почки, чередуясь через один с анионами S2 , благодаря чему серебро имеет координацию 2+2 по причине смещения его из центра S24 тетраэдра в на
правлении одного из ребер. В целом структуру можно охарактеризо |
||
|
вать как островную субцепочечную. Облик криj |
|
|
сталлов. Нередко встречается в кристаллах |
|
|
псевдоскаленоэдрического облика с острыми |
|
|
псевдоромбоэдрическими гранями (рис. 131). |
|
|
Главнейшие формы: гексагональная призма |
|
|
{1120} и дитригональные пирамиды {2131}, |
|
|
{1124} и др. На гранях призмы характерна ко |
|
|
сая штриховка. Чаще наблюдается в виде вкрап |
|
|
ленных зерен, иногда в сплошных массах. Цвет |
|
Рис. 131. Кристаллы |
прустита ярко красный (подобен цвету кинова |
|
ри). Черта ярко красная, зеленеющая при рас |
||
прустита: a {1020}, |
||
v {2131}, r {1011}, e {0112}, |
тирании. Полупрозрачен. Блеск сильный ал |
|
p {1562}, u {1014} |
мазный. Для Li света: Nm = 3,088, Np = 2,792. |
|
|
Твердость 2–2,5. Хрупок. Спайность отчетли |
|
вая по {1011}. Излом раковистый. Уд. вес 5,57–5,64. Прочие свойства. Элек тричества не проводит.
Диагностические признаки. По внешним признакам очень трудно отличим от пираргирита. Как правило, несколько светлее, чем пирарги рит. Кристаллы менее богаты гранями, чем кристаллы пираргирита. Глав ное отличие между ними все же в содержаниях As и Sb.
Из других минералов по цвету и блеску на прустит похожи: миар гирит (AgSbS2), киноварь, куприт (Сu2О) и цинкит (ZnO). Миарги рит, если встречается не в кристаллах, от прустита можно отличить по меньшей прозрачности, а от пираргирита — только по соотношению S : Sb, которое можно установить в результате химического анализа. Киноварь легко отличается по поведению п. п. тр. (улетучивается пол ностью). Для куприта характерны октаэдрические кристаллы, буро вато красная черта, а также парагенезис с самородной медью и други ми минералами меди. Цинкит обладает оранжево желтой чертой и повышенной твердостью (4–4,5).
П.п. тр. легко плавится, издает запах мышьяка и образует налет As2О3
иSb2O3 (в случае присутствия сурьмы). Королек при добавлении соды в восстановительном пламени дает серебро. В HNO3 растворяется с выде лением S и As2O3 (для пираргирита Sb2O3).

Раздел II. Сульфиды, сульфосоли и им подобные соединения |
271 |
Происхождение и месторождения. Распространен в гидротермальных
жилах свинцово цинково серебряных руд (так называемой благородной кварцево кальцитовой формации). Встречается среди минералов, образу ющихся в последних стадиях гидротермальных процессов, иногда совмест но с пираргиритом. В парагенезисе с этими минералами очень часто встре чается галенит, иногда самородное серебро, а также различные по составу сульфоарсениты и сульфоантимониты свинца, серебра и меди. В некото рых месторождениях они ассоциируют с арсенидами никеля и кобальта.
В зоне окисления прустит и пираргирит разлагаются, иногда с образова нием самородного серебра и аргентита. Обычно же серебро в виде неустой чивого Ag2SO4 способно мигрировать, особенно в присутствии свободной серной кислоты и сульфата окиси железа. В ряде случаев устанавливается обогащение серебром нижних горизонтов зоны окисления месторождений.
Среди свинцово цинковых месторождений России прустит, так же как
ипираргирит, наблюдается сравнительно редко, главным образом в мик роскопических выделениях, устанавливаемых в полированных шлифах. Наиболее часто они встречаются в ряде свинцово цинково серебряных месторождений Западного Верхоянья (Якутия) — в Безымянском, Верх' не'Эндыбальском, Березинском и др.
Из иностранных месторождений наиболее богаты ими месторожде ния Мексики (Цакатекас, Гуанахуато и др.), Чили, Перу, Боливии и др.
Практическое значение. Прустит и пираргирит принадлежат к числу наи болееширокораспространенныхсеребросодержащихминераловипотомуиме ют значение как источники серебра. При плавке галенитовых концентратов, получаемых из свинцово цинковых руд, серебро получается попутно.
ПИРАРГИРИТ — Ag3SbS3. Название происходит от греч. пирос — огонь и аргирос — серебро. Синонимы: темно красная серебряная руда, серебряная обманка (рис. 132).
Физические свойства этого минерала во многом аналогичны описан ным выше для прустита. Отметим отличительные особенности. Цвет в от раженном свете темно красный до железно черного; на углах кристаллов
ив обломках пираргирит просвечивает. Черта темная
вишнево красная. Уд. вес 5,77–5,86 (больше, чем прус тита). Прочие диагностические признаки указаны выше (см. прустит).
В природе встречается в тех же условиях, что и пру стит, но преимущественно с содержащими сурьму ми нералами.
СТЕФАНИТ — Ag5SbS4 или 5Ag2S . Sb2S3. Содер жание Ag — 68,5 %. Сингония ромбическая; ромбо пи рамидальный в. с. L2PC. a0 = 7,72; b0=12,34; с0 = 8,50. Пр. гр. Сmс21 (C122v). Встречается в короткопризматических кристаллах и сплошных массах.
Рис. 132. Кристалл пираргирита:
o {0001}, r {1011}, m {1010}, y {3251}
272 |
Описательная часть |
Цвет серовато черный. Черта черная. Блеск металлический. Тверj дость 2–2,5. Хрупкий. Спайность по {010} средняя. Уд. вес 6,2–6,3.
П.п. тр. на угле плавится с растрескиванием, образуя налет Sb2O3.
Ссодой дает королек серебра. Разлагается разбавленной HNO3 с выделе
нием S и Sb2S3.
Вместе с другими минералами серебра, обычно в очень небольших количествах, встречается в жилах гидротермального происхождения. Описан в месторождениях Саксонии и Гарца (Германия), в ряде место рождений Мексики и в других местах.
ПОЛИБАЗИТ — (Ag,Cu)16Sb2S11 или 8(Ag,Cu)2S . Sb2S3. Содержание Ag — 62,1–74,9 %, Сu — 3–10 %. Сингония моноклинная; призматиче
ский в. с. L2PC. a0 = 26,17; b0=15,11; с0 = 23,89, β = 90°. Пр. гр. С2/m (C32h). Наблюдается в пластинчатых или короткопризматических кристаллах
псевдотригонального или псевдогексагонального облика.
Цвет серовато черный. Черта черная с красноватым оттенком. Блеск металлический. Твердость 2–3. Спайность по {001}. Уд. вес 6,27–6,33.
П. п. тр. на угле очень легко плавится в металлический шарик с выде лением дыма и налета Sb2S3. При сплавлении с фосфорнокислой солью дает зеленовато синий перл (медь).
Вместе с другими сульфосолями серебра встречается в низкотемпе ратурных гидротермальных жилах в ряде районов: Яхимов и Пршибрам
(Чехия), Банска'Штьявница (Словакия), Цакатекас, Гуанахуато и Ду' ранго (Мексика) и других местах.
5. Сульфосоли свинца
Относящиеся сюда соединения представлены главным образом суль фоарсенитами, сульфоантимонитами и сульфовисмутитами свинца. Все эти соединения ведут себя обособленно от сульфосолей меди и серебра, иногда лишь образуя с ними двойные соединения.
Мы рассмотрим лишь два минерала — буланжерит и джемсонит. БУЛАНЖЕРИТ — Pb5Sb4S11 или 5PbS . 2Sb2S3.
Химический состав. Рb — 55,4 %, Sb — 25,7 %, S — 18,9 %. Содержа ние Рb колеблется в пределах 54—58 %; часть его бывает связана с меха нической примесью галенита. Иногда содержит медь до 1 %.
Сингония моноклинная; призматический в. с. L2PC. Пр. гр. P21/a (С 52h). Кристаллы крайне редки. Обычно встречается в тонкозернистых или спу танно волокнистых агрегатах.
Цвет буланжерита свинцово серый до железно черного. Черта серова то черная с коричневатым оттенком. Непрозрачен. Блеск металлический.
Твердость 2,5–3. Хрупок. Спайность по {100} средняя. Уд. вес 6,23. Диагностические признаки. Обычно бывают характерны тонковолокни
стые агрегаты и коричневатый оттенок черты. Без данных химического ана лиза и рентгеновских исследований невозможно с уверенностью отличить от ряда других, более редко встречающихся сульфоантимонитов свинца.
Раздел II. Сульфиды, сульфосоли и им подобные соединения |
273 |
П.п. тр. легко плавится. С содой на угле дает королек свинца и плотный
белый налет Sb2O3 вблизи пробы. Растворяется в HNO3 и горячей НСl.
Происхождение и месторождения. Встречается в гидротермальных
месторождениях свинцово цинковых руд в сопровождении сульфоанти монитов свинца и меди, галенита, сфалерита, пирита, арсенопирита и др.
Отмечался в ряде месторождений Нерчинского района в Восточном Забайкалье: Алгачинском (в значительных количествах), Кличкинском, Дарасунском и др. В альпийских хрусталеносных жилах Приполярного Урала отмечен в виде игольчатых вростков в кварце. Встречается в На' гольном кряже (Украина) в ассоциации со сфалеритом, галенитом, бур нонитом, блеклой рудой и другими минералами.
В зоне окисления легко разрушается, образуя церуссит Pb[CO3] и гид роокислы сурьмы.
Практическое значение. В случае значительных скоплений представ ляет интерес как свинцовая руда.
ДЖЕМСОНИТ — Pb4FeSb6S14 или 4PbS . FeS . 3Sb2S3. Разновидность, не содержащая железа, носит название плюмозита.
Химический состав не всегда точно отвечает формуле. Содержит Рb — 40–50 %, Fe — до 10 %, Sb — около 30 %, S — около 20 %. В виде примеси часто присутствуют медь, цинк и серебро.
Сингония моноклинная; призматический в. с. L2PC. Пр. гр. P21/a (С 52h). Часто встречается в виде призматических, игольчатых и волосовидных кристаллов, иногда в виде вростков в кристаллах кварца, сфалерита и дру гих, позднее кристаллизующихся минералов в друзовых пустотах.
Цвет джемсонита свинцово серый. Черта серовато черная. На гранях иногда наблюдается синевато серая побежалость. Блеск металлический.
Твердость 2–3. Хрупкий. Излом неровный. Спайность по {001} сред няя. Уд. вес 5,5–6,0.
Диагностические признаки. На глаз невозможно отличить от других суль фоантимонитов свинца, встречающихся в игольчатых формах. В случае па раллельно шестоватых агрегатов распознается, благодаря базальной спайно сти, перпендикулярной к направлению развития индивидов. Для точной диагностики необходимы химический анализ и рентгеновские исследования.
П.п. тр. плавится. На угле получается королек свинца. С содой дает
белый налет Sb2O3. В HNO3 легко растворяется.
Происхождение и месторождения. В России встречается в Саввинском
месторождении (Забайкалье), в гидротермальных свинцово цинковых ру дах в ассоциации с кварцем, галенитом, иногда сфалеритом и другими минералами, в друзовых пустотах. Описан также в Дарасунском золото рудном месторождении (Забайкалье).
В Украине джемсонит известен в полиметаллических жилах Наголь' ного кряжа в ассоциации с кальцитом и в других местах. Из месторожде ний зарубежных стран в значительных количествах был встречен в Ци' мапане (Мексика).
Раздел III
ГАЛОИДНЫЕ СОЕДИНЕНИЯ (ГАЛОГЕНИДЫ И ГАЛОГЕНОСОЛИ)
Общие замечания. Начиная с этого типа соединений мы будем иметь дело с минералами, резко отличающимися по своим свойствам от рас смотренных до сих пор. В подавляющей массе это будут уже соединения с типичной ионной или ковалентной полярной связью, обусловливающей совсем другие свойства минералов. Наиболее яркими представителями их являются галоидные соединения металлов.
С химической точки зрения относящиеся сюда минералы представ лены солями кислот: HF, HCl, HBr и HJ; соответственно этому среди этих минералов различают фториды, хлориды, бромиды и иодиды. Галогеносо ли являются комплексными соединениями, из которых здесь рассматри ваются фторалюминаты. Кроме того, существуют водные соли и более сложные соединения, содержащие добавочные кислородсодержащие ани оны: [ОН]1–, О2–, изредка [SO4]2– и [JO3]1–. Это так называемые оксигало идные соединения, переходные к типичным кислородным соединениям.
Как показано на рис. 133, главные элементы, образующие галогени ды, в противоположность тому, что мы наблюдали в ранее рассмотрен ных минералах, расположены в левой половине менделеевской таблицы, преимущественно в I и во II группах. Галоидные соединения тяжелых металлов, наоборот, играют совершенно ничтожную роль в минералогии природных образований и возникают в особых условиях.
Кристаллохимические особенности галоидных соединений. Установ лено, что галогениды легких металлов характеризуются структурами с ти
Рис. 133. Элементы, для которых характерны соединения с галоидами (набраны жирным шрифтом)
Раздел III. Галоидные соединения (галогениды и галогеносоли) |
275 |
пичной гетерополярной (ионной) связью, тогда как в соединениях тяже лых металлов, катионы которых обладают сильной поляризацией, возни кают гомополярные (ковалентные) или переходные к ним связи между иона ми. В соответствии с этим находятся и физические свойства минералов.
Так как в галогенидах с типичной ионной связью принимают участие катионы легких металлов с малыми зарядами и большими ионными радиу сами, а в связи с этим с весьма слабой способностью к активной поляриза ции, то естественно, что эти минералы обладают прозрачностью, бесцветно стью (наблюдаемые окраски, как правило, являются аллохроматическими), малыми удельными весами, а также такими свойствами, как необычайно легкая растворимость многих галогенидов в воде, низкие показатели пре ломления, а следовательно, и слабый стеклянный блеск минералов.
Что касается катионов тяжелых металлов с 18 электронной наруж ной оболочкой (Cu, Ag и др.), склонных к сравнительно резко выражен ной поляризации окружающих анионов и к образованию кристалличе ских структур с ковалентной связью, то здесь мы наблюдаем уже существенные отличия в свойствах галогенидов высокие удельные веса, наличие у ряда соединений хотя и слабой, но идиохроматической окрас ки, сильно повышенные показатели преломления, алмазный блеск, резко пониженная растворимость этих минералов и др.
Теперь перейдем к характеристике свойств, зависящих от главных анионов в галогенидах: F1–, Cl1–, Вr1– и J1–.
Прежде всего следует отметить, что анион F1– значительно отличает ся по своим размерам от остальных анионов, как это видно из сопостав ления их радиусов (в ангстремах):
F1– |
Cl1– |
Вr1– |
J1– |
1,33 |
1,81 |
1,96 |
1,19 |
Это обстоятельство весьма существенно сказывается на выборе тех или иных катионов для образования соединений (в соответствии с коор динационными числами и типом кристаллической структуры), на их ус тойчивости, а в связи с этим и на физических и химических свойствах. Не случайно, что главная масса фтора в земной коре связана с Са и отча сти с Аl и Si (в галогеносолях), тогда как хлор и резко подчиненные ему по распространенности бром и йод в основном связаны с Na, К, (Rb), (Cs) и Mg (в водных солях). В противоположность хлоридам, бромидам и иоди дам тяжелых металлов (Аu, Ag, Hg и др.) их фториды вовсе не встречают ся в природных условиях. Хлориды легких металлов чрезвычайно легко растворяются в водной среде, тогда как их фториды в большинстве своем устойчивы по отношению к воде. Насколько велика разница в раствори мости этих типов соединений, можно видеть из данных, приводимых в табл. 7.
276 |
Описательная часть |
Таблица 7
Растворимость галоидных соединений в воде при 18 °С (в молях на литр насыщенного раствора)
Анионы |
|
|
|
Катионы |
|
|
|
|
|
|
|
|
|
|
|
|
|
|
Li |
Na |
К |
Mg |
Ca |
Sr |
Ba |
Pb2+ |
F |
0,11 |
1,06 |
12,4 |
0,02 |
0,03 |
0,001 |
0,03 |
0,003 |
|
|
|
|
|
|
|
|
|
Cl |
13,1 |
5,42 |
3,9 |
5,1 |
5,4 |
3,0 |
1,7 |
0,05 |
|
|
|
|
|
|
|
|
|
Вr |
12,6 |
6,9 |
4,6 |
4,6 |
5,2 |
3,4 |
2,9 |
0,02 |
|
|
|
|
|
|
|
|
|
J |
8,5 |
8,1 |
6,0 |
4,1 |
4,8 |
3,9 |
3,8 |
0,02 |
|
|
|
|
|
|
|
|
|
Температуры плавления и кипения фторидов несравненно выше, чем хлоридов тех же металлов. Например, температура кипения SnF4 равна 705 °С, a SnCl4 — 114 °С, фторид алюминия AlF3 кипит при температуре выше 1000 °С, а его хлорид АlСl3 — при температуре всего лишь 81 °С и т. д.
Об особенностях поведения галогенов в природе. Крайне интерес ны геохимические черты галогенов F, Cl, Br и J, выражающиеся в поведе нии их при различных геологических процессах.
При магматических процессах не создается условий для концентрации этих элементов в сколько нибудь значительных количествах. Фтор и хлор лишь в качестве добавочных анионов входят в ряд минералов, преимущест венно силикатов и фосфатов (большей частью в пегматитах и в контактово метасоматических образованиях). Главная масса этих элементов, очевидно
ввиде летучих соединений с металлами, переходит в гидротермальные раст воры. О том, что хлор и фтор действительно являются составной частью ле тучих погонов магм, свидетельствуют выделения НСl и HF в газообразных продуктах вулканических извержений, иногда в весьма значительных коли чествах. Например, на Аляске в долине, известной под названием «Десять тысяч дымов», в 1919 г., по подсчетам, выделилось 1,25 млн т газообразной
НСl и 0,2 млн т HF вместе с парами Н2О.
Из галогенидов во многих гидротермальных образованиях широко пред
ставлен CaF2 (флюорит), отчасти фторалюминаты, однако хлориды метал лов не встречаются, если не считать крайне редких находок NaCl (галита)
ввиде микроскопических кристалликов в капельках растворов, обнаружи ваемых в виде включений в некоторых минералах (кварце, галените).
Зато в экзогенных условиях хлориды Na, в меньшей степени хлори ды, К, Mg и других металлов, образуются, нередко в огромных массах, в усыхающих соленосных бассейнах вместе с сульфатами, иногда бората ми и другими растворимыми в воде соединениями. Вместе с хлором со ответствующая концентрация наблюдается также для брома и йода. В на стоящее время 70–75 % всего имеющегося в земной коре хлора
