
- •2.2. Функциональные производные углеводородов. Галогенпроизводные углеводородов
- •Строение и номенклатура
- •Химические свойства
- •Особенности реакций ароматических галогенопроизводных с галогеном в ароматическом ядре
- •II. Реакции отщепления.
- •Физические свойства галогенопроизводных, их применение
- •Способы получения галогенопроизводных
- •Задания для выполнения кр № 2 по теме «функциональные производные углеводородов. Галогенопроизводные углеводородов» Галогенпроизводные углеводородов
- •2.3. Функциональные производные углеводородов. Кислородсодержащие производные углеводородов
- •2.3.1.Спирты
- •Химические свойства одноатомных спиртов
- •Способы получения одноатомных спиртов
- •Особенности многоатомных спиртов
- •Химические свойства
- •Физические и пожароопасные свойства многоатомных спиртов, их применение
- •Способы получения
- •Строение фенола
- •Химические свойства
- •Физические свойства и применение
- •Способы получения
- •Простые эфиры
- •Химические свойства
- •Физические и пожароопасные свойства простых эфиров
- •Способы получения простых эфиров
- •2.3.2. Альдегиды и кетоны
- •Номенклатура альдегидов и кетонов
- •Химические свойства
- •Физические и пожароопасные свойства альдегидов и кетонов, их применение
- •Способы получения альдегидов и кетонов
- •2.3.3. Карбоновые кислоты
- •Физические свойства.
- •Химические свойства
- •Особенности ненасыщенных карбоновых кислот.
- •Важнейшие представители карбоновых кислот и их производных.
Способы получения одноатомных спиртов
Метанол получают из СО и Н2 в крупнопромышленных масштабах.
СО + 2Н2 СН3ОН
Катализаторами реакции являются соединения цинка и хрома (ZnO + ZnCr2O4), температура реакции 250-3500С, давление до 300 атм.
Древнейшим методом получения этанола является ферментативный метод – сбраживание раствора сахаров (углеводов).
С6Н12О6 2СО2 + 2С2Н5ОН
В промышленности этанол получают каталитической гидратацией этилена. Одним из лучших катализаторов является силикагель, обработанный фосфорной кислотой.
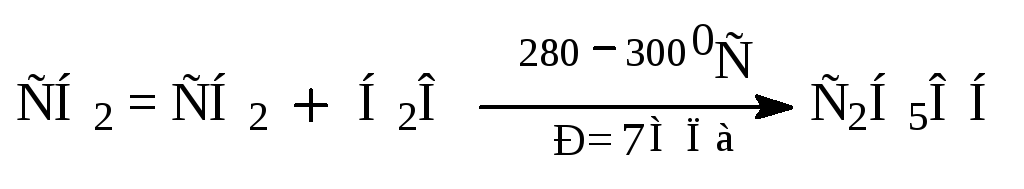
Особенности многоатомных спиртов
Представители спиртов:

Химические свойства
Увеличение кислотных свойств.
Введение второй и третьей гидроксильных групп усиливает кислотные свойства спиртов. Двух- и трехатомные спирты могут образовывать с гидроокисями тяжелых металлов гликоляты и глицераты металлов.
Пример:
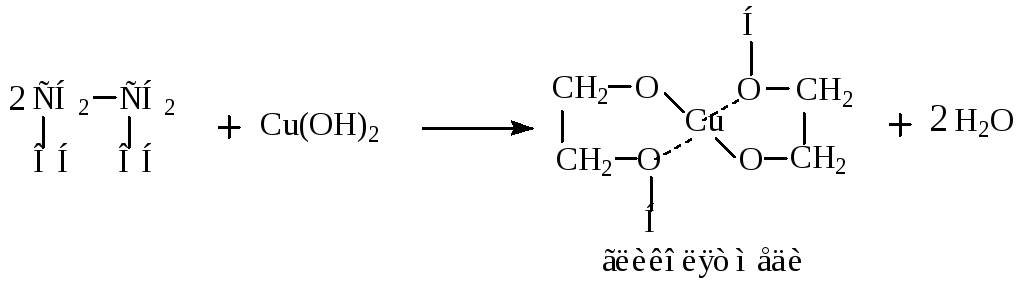
В процессе реакции гидроокись меди растворяется, и образуется раствор ярко синего цвета (качественная реакция на многоатомные спирты).
Образование сложных эфиров неорганических кислот.

Образуется тринитрат глицерина. Это сильнейшее взрывчатое вещество, взрывается от удара, в результате саморазложения. Его используют для получения динамита.
Дегидратация спиртов.
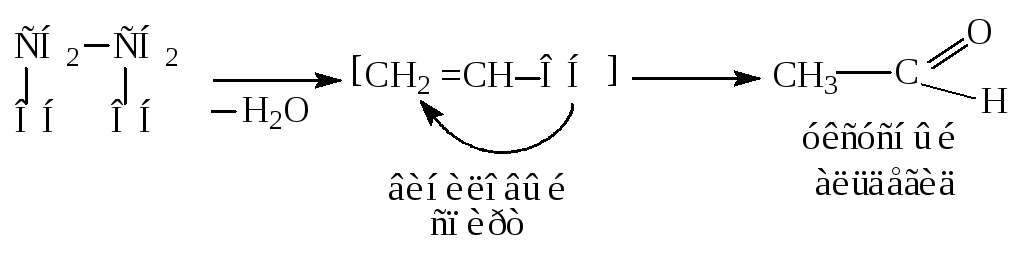

В качестве водоотнимающих средств используются: ZnCl2, H2SO4.
Физические и пожароопасные свойства многоатомных спиртов, их применение
Этиленгликоль – бесцветная, вязкая жидкость сладкого вкуса, хорошо смешивается с водой. Его используют для получения полимеров, растворителей. Смеси гликоля с водой имеют низкую температуру замерзания (до -750С), поэтому его применяют для охлаждения автомобильных и тракторных двигателей (антифризы).
Глицерин – очень вязкая, бесцветная жидкость со сладким вкусом. При температуре кипения разлагается. Смешивается с водой. При реакции с окислителями глицерин самовозгорается. Хранение глицерина с сильными окислителями недопустимо, так как в случае контакта может возникнуть пожар.
Глицерин используется для производства взрывчатых веществ, высокомолекулярных соединений, в меньших количествах – в косметических препаратах, в качестве мягчителя кож и текстильных материалов, в ликеро-водочной промышленности.
Способы получения
Получение этиленгликоля гидроксилированием этилена.

Синтез глицерина из пропена.
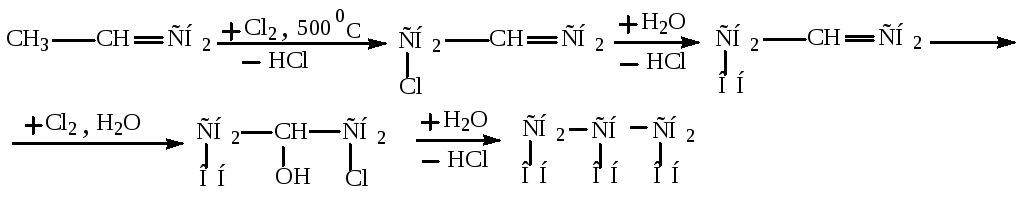
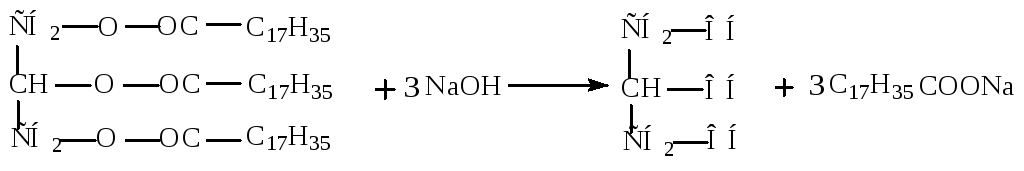
Синтез глицерина из жиров.
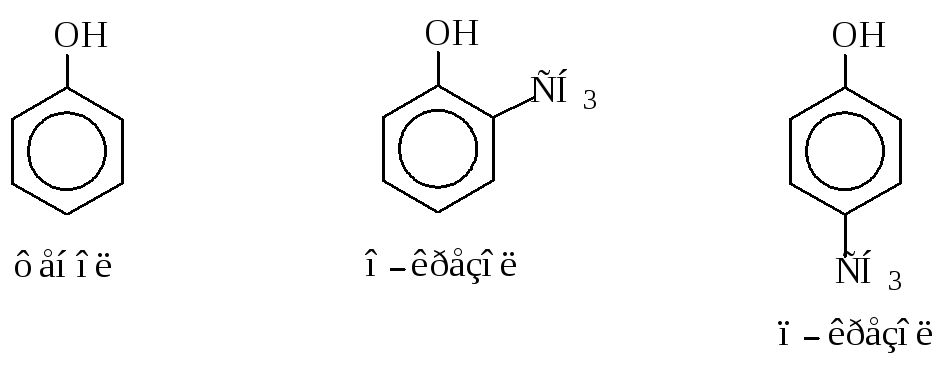
Фенолы
Фенолы – это гидроксильные производные ароматических углеводородов, содержащие гидроксильную группу у углеродного атома цикла. Названия фенолов образуют от названий соответствующих ароматических углеводородов, а наличие гидроксильной группы обозначают суффиксом -ол. Нумерацию начинают от углеродного атома при гидроксильной группе. Многие фенолы сохраняют тривиальные названия.
Строение фенола

В молекуле фенола атом кислорода не только оказывает сильное индукционное влияние на углеводородный остаток (-I – эффект), но и вступает с помощью pz – электронной пары в сопряжение с - электронной системой бензольного ядра (+С – эффект). Эффект сопряжения преобладает над индукционным эффектом, поэтому в орто- и пара- положениях локализуется дробный отрицательный заряд. В результате (+С )– эффекта фенолы становятся по кислотности на 8 порядков сильнее спиртов и очень активны в реакциях электрофильного замещения, которые проходят в орто – и пара – положения.
