
Лекции - часть 3
.pdf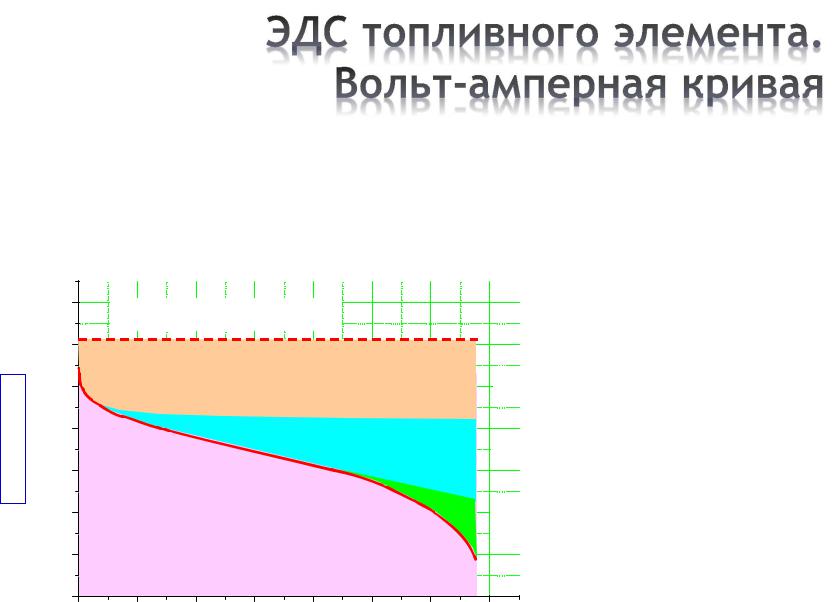
|
Кривая поляризации для топливного элемента |
|||||||
|
|
|
|
(где теряется ЭДС?) |
|
|||
|
1.4 |
1.23 V – стандартный |
|
|
|
|||
|
|
|
|
|
||||
|
1.2 |
|
|
|
|
|
|
|
|
1.0 |
|
|
Потери ЭДС |
|
Активность катализатора |
||
V |
0.8 |
|
|
|
|
|||
, |
|
|
|
|
|
|
|
|
ЭДС |
0.6 |
|
|
|
|
|
|
Омические потери |
|
|
|
|
|
|
|
||
|
|
|
|
|
|
|
|
|
|
0.4 |
ЭДС на выходе ТЭ |
|
|
Подвод реагентов |
|||
|
|
|
|
|||||
|
0.2 |
|
|
|
|
|
|
|
|
0.0 |
|
|
|
|
|
|
|
|
0 |
200 |
400 |
600 |
800 |
1000 |
1200 |
1400 |
|
|
|
|
Ток, mA/cm2 |
|
|
||
91

3. Макроструктура |
2. Мезоструктура |
1. Микроструктура |
Catalyst
Membrane
Nafion Catalytic binder
layer
Транспорт |
транспорт |
Активность |
реагентов и продуктов |
H+ и e- |
катализатора |
92

Механизм:
1. |
H2 |
k+T |
|
– р-ция Тафеля (медленно, лимитирует) |
+ 2S 2Hads |
||||
|
|
k-T |
|
|
|
|
1/K |
|
|
2. |
Hads VS + H+ |
+ e- |
– р-ция Фольмера (быстро, равновесие) |
|
3. |
H2 |
+ S Hads + H+ + e- |
– р-ция Гейровского (медленно, |
|
|
|
|
|
учитывают при высоких |
степенях покрытия по Hads)
Скорость электроокисления водорода по Тафелю-Фольмеру
WHOR k T H2 1 H 2
93

Химические потенциалы
Hads 0Hads RT ln H E( H )
S 0S RT ln 1 H
H 0H RT ln H
Равновесные условия
Hads S H e |
|
|
|
|
|
0 |
0 0 |
|
1 H |
|
|
|
|
||||
Hads S H E( H ) F RT ln |
H |
|
|||
|
|
|
H |
|
|
Изотерма
H+ из раствора
 Hads
Hads
e- из металла
Больше энергия связи EM-H – выше степень покрытия
E( H ) |
- Учет латеральных взаимодействий |
|
адсорбированных атомов |
Степень покрытия поверхности H зависит от потенциала . При увеличении потенциала катионы десорбируются. Анионы адсорбируются.
94

H2 из газовой фазы
d
Hads
Чем прочнее связь M-Hads, тем ниже активационный барьер и выше
скорость реакции
|
|
|
|
|
|
|
|
|
|
||
E |
E |
E |
|||||||||
H2 |
|
|
|||||||||
|
|
|
|
|
|||||||
|
|
|
|
|
|
|
|
|
2Hads |
||
|
|
|
|
|
|
|
|
|
|||
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
EHads |
|
|
2Hads |
|||||
|
|
|
|
|
|
|
|
|
|
|
|
Координата реакции d
Изменение энергии связи M-Hads Влияет на активационный барьер:
E = Eads
0.2 0.8 – фактор симметрии барьера
95

Eads => free => Wreaction
Eads => Eact => Wreaction
96

Энергия взаимодействия H с spэлектронами (Ehom) одинакова для разных металлов
E |
EF |
|
||
|
|
|
|
|
|
|
|
(Fermi |
|
EH |
level) |
|
||
|
|
|||
|
|
|
|
|
|
|
hom |
|
|
|
|
|
|
|
DOS для sp уровней
EHads Ehom Ehybr 245 |
kJ |
|
mol |
||
|
Энергия взаимодействия Н с d-электронами Ehybr зависит от положения центра d-полосы по отношению к уровню Ферми EF,,количества d- электронов и размера d-орбитали
Ed 2 f |
|
|
Vd H |
|
2 |
|
|
|
|||||
|
|
|
|
|||
|
|
|
|
|
||
Ed EH |
||||||
|
||||||
 Ed
Ed
2 Vd H
2
Ed EH
EH
DOS для d-уровня
2 1 f |
|
Vd H |
|
2 |
|
|||
|
|
|||||||
|
|
|
|
|
||||
E |
E |
H |
|
|||||
|
||||||||
|
|
d |
|
|
|
|||
Norskov JK, 1982 |
97 |

M-H
E , kJ/mol
0.5 EH-H
-220 |
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
Низкое покрытие |
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
Cu |
||||||||||||||||||||||||||||||||||||||||||||
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
||||||||||||||||||||||||||||||||||||||||||||||
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|||||||||||||||||||||||||||||||||||||||||||||
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
Ag |
|
|
|
|
|
|
Hads |
||||||||||||||||||||||||||||||||||||||||||||||
|
|
|
|
|
|||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||
|
|
|
|
|
|||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||
-240 |
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
Au |
||||||||||||||||||||||||||||||||||||||||||
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||
|
|
Tc |
|
Co |
Pd |
3d |
-260 |
|
|
|
|||
|
Fe |
Ni |
d-orb |
|||
|
|
Mn |
Rh |
Pt |
||
|
|
Ru |
Ir |
|
||
|
|
|
|
|||
|
W |
Re |
|
4d |
||
-280 |
|
|
||||
Os |
|
|
||||
|
Cr |
|
|
|
|
|
|
|
|
|
|
Y |
|
|
|
|
|
|
Высокое покрытие |
|
|||
|
|
|
|
|
|
|
|
|
|
|||||||
-300 |
|
|
|
|
La |
|
|
V |
|
Mo |
|
|||||
|
|
|
|
Sc |
|
|
|
|
|
|||||||
|
|
|
|
|
|
|
|
|
|
|
||||||
|
|
|
|
|
|
|
Zr |
|
|
Nb |
|
|
|
|
5d |
|
|
|
|
|
|
|
|
Ti |
|
|
|
|
|
|
|||
|
|
|
|
|
|
|
|
|
|
|
||||||
|
|
|
|
|
|
|
|
|
|
|
||||||
-320 |
|
|
|
|
|
|
Hf |
|
|
Ta |
|
|
|
Nordlander, 1984 |
|V |2 |
|
|
|
|
|
|
||||||||||||
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
f |
d-H |
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
EHads 2 1 f |
|
|
|
Vd H |
|
2 |
|
|
|
|||||||
|
|
|
|
|
|
|||||||||||
|
|
|
|
|
|
|
|
|||||||||
|
|
|
|
|
|
|
||||||||||
|
Ed EH |
|
98 |
|||||||||||||
|
|
|
|
|
|
|
|
|
|
|||||||
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|

Потенциальная энергия вдоль координаты реакции
kJ/mol |
100 |
|
|
|
|
|
50 |
|
|
Au |
|
||
|
|
|
|
|
||
, |
|
|
|
|
|
|
H-H |
0 |
|
|
|
Cu |
|
- E |
|
|
|
|
||
|
|
|
|
|
|
|
Hads |
-50 |
|
Hammer 1995 |
Pt |
|
|
|
|
|
||||
E |
|
|
|
|||
|
|
|
|
|
||
|
|
|
|
|
|
|
-100 |
3 |
2 |
1 |
|
0 |
|
|
4 |
|
||||
Reaction coordinate, rH2-S (A)
Eact = Eads
E , kJ/mol act
|
100 |
|
|
Высокая Eact |
|
|
|
|
|
|
|
|
Cu |
||||||
|
|
|
|
|
|
|
|
|
|
|
|||||||||
|
j |
|
|
< 0.01 mA/cm2 |
|
|
|
|
|||||||||||
|
|
|
|
|
|
|
|||||||||||||
|
80 |
ads |
|
|
|
|
|
|
|
|
|
|
|
Ag |
|||||
|
|
|
|
|
|
|
|
|
|
|
|
|
|
||||||
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
Au |
|
|
60 |
|
|
|
|
|
|
|
|
|
|
|
|
|
|
Pd |
|||
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|||||
|
40 |
|
|
|
|
|
|
|
Tc |
|
|
|
|
|
|
||||
|
|
|
|
|
|
|
|
|
|
|
|
|
|||||||
|
|
|
|
|
|
|
|
|
|
|
|
|
Co |
|
Ni |
||||
|
|
|
|
|
|
|
|
|
|
|
|
|
|
||||||
|
|
|
|
|
|
|
|
|
|
|
|
|
|||||||
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
20 |
|
|
|
|
|
|
|
|
|
Fe |
Rh |
|
Pt |
|
||||
|
|
|
|
|
|
|
|
|
|
|
|
||||||||
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|||||
|
|
|
|
|
|
|
|
|
|
|
|
|
|
||||||
|
|
|
|
|
|
|
|
|
Mn |
|
|
|
|
Ir |
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
||
|
0 |
|
|
|
|
|
W |
|
|
|
Ru |
|
|
|
|
|
|
||
|
|
|
|
|
|
|
Re |
|
Os |
|
|
|
|
|
|
||||
|
|
|
|
|
|
|
Cr |
|
|
|
|
|
|
|
|
||||
|
-20 |
|
|
|
|
|
|
|
|
|
|
|
|
|
|
||||
|
|
|
|
|
|
|
|
|
|
|
|
|
|
||||||
|
|
|
|
|
|
|
Низкая Eact |
|
|
|
|
|
|
||||||
|
|
|
|
|
|
|
|
|
|
|
|
|
|||||||
|
|
|
|
|
|
|
|
j > 0.01 mA/cm2 |
|
||||||||||
|
|
|
|
|
|
|
|
ads |
|
|
|
|
|
|
|
|
|
|
|
99

Red |
Ox |
Потенциал относительно |
|
|
СВЭ, V |
|
|
|
W |
W3+ |
0.11 |
Sb |
(SbO+) |
0.212 |
Bi |
Bi3+ |
0.215 |
Re |
Re3+ |
0.3 |
Cu |
Cu+ |
0.337 |
Tc |
Tc2+ |
0.4 |
Po |
Po2+ |
0.56 |
Ru |
(RuO2) |
0.79 |
Rh |
(Rh2O3) |
0.87 |
Ag |
Ag+ |
0.8 |
Os |
(OsO4) |
0.85 |
Pd |
Pd2+ |
0.987 |
Ir |
Ir3+ |
1.15 |
Pt |
Pt2+ |
1.188 |
Au |
Au3+ |
1.5 |
100
