
методичка лаба термодинамика
.pdf
l2 CT |
2 |
n |
RТ |
|
n 1 |
|
(8) |
|
1 |
( p2 )2n |
1 , кДж/кг, |
||||||
|
|
|
n 1 |
|
p |
|
|
|
|
|
|
|
|
|
1 |
|
|
(площадь1ab2’mn1) (рис.2) |
|
|
||||||
Р |
m |
|
2 |
2 |
|
2 |
|
|
Р2 |
|
|
|
|||||
Р5 |
|
|
f |
|
|
e |
|
|
Р4 |
|
|
|
|
a |
|
||
|
|
|
|
|
b |
|
||
|
|
|
|
|
|
c |
||
Р3 |
|
|
|
|
|
|
||
|
|
|
|
|
|
d |
||
Р1 |
|
|
|
|
|
|
1 |
|
n |
|
|
|
|
|
|
||
|
|
|
Рис.2 – p,v –диаграмма. |
V |
||||
|
|
|
|
|||||
а при трехступенчатом соответственно
|
3 CT |
|
n |
|
p |
2 |
|
n 1 |
|
|
|
|
|
||||||
l |
|
3 |
|
|
RТ1 ( |
|
)3n |
||
|
n 1 |
p |
|||||||
|
|
|
|
|
|
||||
|
|
|
|
|
1 |
|
|
||
1 , кДж/кг, |
(9) |
|
|
(площадь 1cdef2”mn1) (рис.2)
Выигрыш в работе при переходе от одноступенчатого к двухступенчатому сжатию
l = l - l 2-ст, кДж/кг |
(10) |
31
определится площадью ab2’2a, (рис.2), а при переходе от одноступенчатого к трехступенчатому сжатию
l = l - l 3-ст, кДж/кг, |
(11) |
и определится площадью cdef2”2c. (рис.2).
Определение параметров в случае двухступенчатого сжатия:
Давление р4 |
определится из соотношения |
|
||||||||||
|
р |
|
|
р |
|
|
р |
|
|
1 |
|
|
|
4 |
|
2 |
( |
2 |
)2 |
, |
(12) |
||||
|
р1 |
р4 |
р1 |
|||||||||
|
|
|
|
|
|
|
||||||
а температура Т2’ в конце процесса двухступенчатого сжатия
T |
|
р |
|
|
n 1 |
|
|||
|
|
|
|
|
|
||||
( |
2 |
)2n |
|
||||||
|
2 |
|
(13) |
||||||
T1 |
р1 |
||||||||
|
|
|
|
|
|
||||
Удельные объемы в точках а и 2’ можно определить из уравнения состояния.
Определение параметров в случае трехступенчатого сжатия: Давления
|
|
р |
|
|
|
р |
|
|
|
|
р |
|
|
|
р |
|
|
1 |
|
|
|
3 |
|
|
5 |
|
|
2 |
|
( |
2 |
)3 . |
(14) |
||||||||
|
|
р1 |
р3 |
р5 |
р1 |
|||||||||||||||
|
|
|
|
|
|
|
|
|
|
|||||||||||
Температура при сжатии в каждой ступени |
|
|||||||||||||||||||
T |
|
|
|
|
р |
|
|
n 1 |
|
|
|
|
|
|
|
|||||
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|||||
|
|
( |
2 |
)3n . |
|
|
|
|
|
|
|
|||||||||
|
2" |
|
|
|
|
|
|
|
|
(15) |
||||||||||
T1 |
|
|
|
|
|
|
|
|
|
|||||||||||
|
|
|
|
р1 |
|
|
|
|
|
|
|
|
|
|||||||
Удельные объемы определяются из уравнения состояния.
v |
|
RT2" |
; |
v |
|
RT2' |
. |
(16) |
|
|
|||||||
2" |
|
p |
2' |
|
p |
|
||
|
2 |
|
|
2 |
|
|
||
32

T |
|
Р2 |
Р5 |
T2 |
|
2 |
Р4 Р3 |
|
|
Р1 |
|
|
|
|
|
T2 |
2 |
a |
|
T2 |
2 |
|
|
е |
c |
||
|
|
|
|
|
f |
b d |
1 |
S
Рис.3- T,s - диаграмма
Лабораторная работа № 5
ОПРЕДЕЛЕНИЕ ЗАВИСИМОСТИ ТЕМПЕРАТУРЫ КИПЕНИЯ ВОДЫ ОТ ДАВЛЕНИЯ
Цель работы: Определение зависимости температуры кипения воды от давления.
Основные сведения
Фазовым переходом называют переход из одной фазы в другую, сосуществующую с первой. Говоря о фазах чистого вещества, обычно имеют в виду его агрегатные состояния и поэтому говорят о газовой, жидкой и твердой фазах. Под фазовым переходом подразумевается переход из одного агрегатного состояния в другое.
33
Одно и то же вещество в зависимости от внешних условий (давление и температура) может находиться в различных агрегатных состояниях. При изменении давления изменяются температуры затвердевания и кипения вещества. Вещество в разных агрегатных состояниях имеет различные физические свойства, в частности, плотность. При переходе вещества из жидкой фазы в газообразную, теплота фазового перехода тратится как на работу расширения, так и на преодоление сил межмолекулярного взаимодействия. При этом уменьшается и плотность вещества. При плавлении и сублимации теплота фазового перехода затрачивается на разрушение кристаллической решетки твердого тела.
Фазовый переход из твердой фазы в газообразную, происходящий при очень низких давлениях, называется сублимацией (обратный процесс – десублимация). Фазовый переход из твердой фазы в жидкую называется плавлением (обратный процесс – затвердевание).Фазовый переход из жидкой фазы в газообразную называется кипением или насыщением (обратный процесс – конденсация).
Принята следующая классификация точек фазового перехода : точка перехода жидкость - пар называется точкой кипения (она же точка конденсации), точка перехода твердое тело - жидкость - точка плавления (она же точка затвердевания), точка перехода твердое тело - пар - точка сублимации (десублимации).
С повышением температуры в веществе происходит некоторое дробление молекулярных ассоциаций (в твердой фазе - разрыхление кристаллов). Этот процесс заметно ускоряется вблизи точек перехода, в которых изменение молекулярной структуры вещества происходит скачкообразно.
При анализе фазовых равновесий и процессов фазовых переходов важную роль играет правило фаз Гиббса. Оно устанавливает зависимость между числом независимых интенсивных переменных, определяющих состояние термодинамической системы, находящейся в равновесии (эти независимые переменные называют степенями свободы системы), числом фаз и числом компонентов системы ( компонент - чистое вещество).
Правило фаз Гиббса формулируется следующим образом
34
= К - Р + 2 |
(1) |
- число степеней свободы термодинамической системы, К - число компонентов системы, Р - число фаз в системе.
Применительно к чистому веществу (однокомпонентная система ) (К = 1) число степеней свободы = 2. Такими независимыми переменными могут являться, например, давление Р и температура Т. Это означает, что если для такой системы произвольно задать , например, давление и температуру, то все другие интенсивные параметры системы (удельный объем, энтальпия, энтропия и т.д.) будут определены однозначно.
Рассмотрим систему, которая состоит, как и прежде, из чистого вещества, но содержит не одну, а две фазы, находящиеся в равновесии между собой. Поскольку в этом случае Р = 2, система обладает только одной степенью свободы, т.е. независимыми переменными , полностью определяющими равновесное состояние каждой фазы системы, могут являться, например, давление Р или температура Т. Этот вывод очень важен. В самом деле, если мы знаем температуру фазового перехода, то она однозначно определяет собой все другие интенсивные термодинамические величины каждой из фаз - давление в точке перехода, плотности вещества в каждой из сосуществующих фаз, удельную энтальпию, энтропию и т.д.
Линию фазового перехода можно изобразить на Р,Т - диаграмме, если нанести на нее состояния, соответствующие давлениям и температурам фазового перехода.
Для однокомпонентной трехфазной системы (Р = 3) число степеней свободы такой системы равно нулю. Отсутствие в этом случае степеней свободы означает, что в однокомпонентной системе три фазы могут находиться в равновесии лишь при вполне определенных температуре и давление, характерных для данного конкретного вещества на кривой фазового перехода в Р,Т - диаграмме состояние, в котором сосуществуют три фазы, изобразится точкой (так называемой тройной точкой). Для воды тройная точка соответствует температуре 0.01 0 С и давлению 610.8 Па.
35
Р
А Жидкая фаза
Твердая фаза К
ОГазообразная
Вфаза
Т
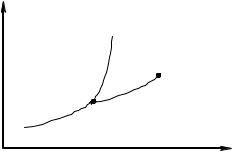
Рисунок 1 - Фазовая Р,Т- диаграмма
На рис. 1 изображена фазовая Р,Т- диаграмма вещества. Линия ОВ - кривая сублимации (десублимации) вещества, линия ОА - кривая плавления (затвердевания) , линия ОК - кривая кипения (конденсации). Кривую кипения называют обычно кривой насыщения. Точка О - тройная точка, в которой вещество сосуществует одновременно в трех фазах. Кривая сублимации ОВ продолжается вниз в сторону низких температур. Кривая ОА уходит вверх , в сторону больших давлений (порядка десятков и сотен тысяч атмосфер). Линия ОК заканчивается в точке К, называемой критической точкой. В критической точке исчезает различие между жидкой и газовой фазами. Влево от линии АОВ - область твердого состояния вещества, справа от линии КОВ расположена область газообразного состояния вещества, между линиями ОА и ОК - область жидкого состояния. Линия сублимации и линия насыщения имеют положительный наклон. Это означает,
что с ростом давления температура фазового перехода
(сублимации и кипения) повышается. Такая закономерность справедлива для всех известных чистых веществ. Линия плавления для различных веществ может иметь и положительный и отрицательный наклон.
Связь между температурой и давлением на линии фазового перехода определяется уравнением Клапейрона - Клаузиуса. Для фазового перехода жидкость - пар уравнение выглядит следующим образом
36

dps |
|
r |
(2) |
|
T(v" v') |
||
dT |
|
||
r = T(s”-s’) (кДж/кг) – скрытая теплота парообразованияколичество теплоты, которое необходимо подвести к кипящей жидкости, чтобы обратить ее в пар,
v” - удельный объем сухого насыщенного пара, м 3/кг; v’ - удельный объем кипящей жидкости ,м 3/кг;
s” - удельная энтропия сухого насыщенного пара, кДж/кг К; s’- удельная энтропия кипящей жидкости, кДж/кг К;
p s – равновесное давление в точках фазового перехода жидкость - пар.
Индекс s - означает на линии кипения (насыщения) (англ. s - saturation).
Поскольку плотность пара всегда меньше плотности жидкости, т.е. v”> v’, из уравнения Клапейрона - Клаузиуса следует, что для фазового перехода жидкость - пар
всегда dps 0, т.е. с ростом температуры давление насыщения dT
увеличивается.
7 |
3 |
2 |
5 |
|
|
|
1 |
|
|
|
|
|
4 |
6 |
8 |
|
в сеть
1.Стеклянный сосуд с водой; 2. Термометр;
3. Вакууметр; 4. Кран; 5. Вакуумный насос; 6. Нагреватель; 7. Регулировочный вентиль; 8. Барометр.
Рис. 1 - Схема экспериментальной установки
37
Порядок выполнения работы
1.Включить нагреватель 6 в сеть.
2.Включить вакуумный насос 5.
3.Регулировочным вентилем 7 при работающем насосе установить определенное разрежение в сосуде 1, зафиксировав его вакууметром 3.
4.Термометром 2 измерить температуру кипения при этом давлении.
5.Изменяя разрежение Рвак регулировочным вентилем 7 и каждый раз фиксируя его вакууметром 3, по термометру 2 определить температуру кипения воды ts при данном давлении.
6.Барометром 8 измерить атмосферное давление В.
7.Выключить насос 5.
8.Выключить нагреватель 6.
Таблица измерений
№ |
Рвак |
Р вак |
В |
Рэкспер |
ts экспер |
Ртабл |
ts табл |
(отсчет |
Па |
кПа |
Па |
С |
Па |
С |
|
|
по шкале ) |
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
Расчетные формулы
Вакууметр измеряет давление вакуума в сосуде. Абсолютное давление определяется
Р = В - Рвак |
(3) |
По таблицам «Вода и водяной пар в состоянии насыщения» построить теоретическую зависимость температуры кипения от давления. Нанести на нее точки, полученные в результате эксперимента, произвести сравнение.
38
Лабораторная работа № 6
ИЗУЧЕНИЕ ПРОЦЕССОВ ВО ВЛАЖНОМ ВОЗДУХЕ
Основные сведения
Влажный воздух представляет собой один из частных случаев газовой смеси - смесь сухого воздуха и водяного пара. С влажным воздухом приходится иметь дело в некоторых теплотехнических процессах и прежде всего в процессе сушки. Для практики представляет интерес влажный воздух при атмосферном (или близким к атмосферному давлении). При этом с достаточной для технических расчетов точностью можно рассматривать и сухой воздух, и содержащийся в нем водяной пар как идеальные газы.
В соответствии с законом Дальтона сумма парциальных давлений газов, входящих в газовую смесь, равна общему давлению газовой смеси. Так как обычно давление влажного воздуха равно атмосферному (В), можно написать
В = p возд + p п |
(1) |
Чем больше водяного пара находится во влажном воздухе, тем выше его парциальное давление. Парциальное давление пара во влажном воздухе не может быть выше p s - давления насыщения при данной температуре влажного воздуха
p п ps |
( 2) |
Максимальное |
парциальное давление водяного пара во |
влажном воздухе p s определяется только температурой смеси и не зависит от давления смеси p.
Влажный воздух, в котором p |
п |
p |
s |
называется |
ненасыщенным, а влажный воздух, |
у которого |
p |
п |
= p s - |
насыщенным. Водяной пар, содержащийся в ненасыщенном влажном воздухе, находится в перегретом состоянии. Если понижать температуру ненасыщенного влажного воздуха, сохраняя его давление постоянным, то можно достигнуть состояния насыщения. При этом перегретый водяной пар, имеющий
39
начальную температуру t 1 будет охлажден до температуры t 2 , для которой давление пара соответствует состоянию насыщения, и при дальнейшем понижении температуры из воздуха будет выпадать влага и уменьшаться парциальное давление пара. С этим мы сталкиваемся в повседневной жизни: так как атмосферный воздух всегда содержит какое-то количество водяных паров, то часто при понижении температуры воздух становится насыщенным, о чем свидетельствует появление тумана или росы. Поэтому температура, при которой давление p п становится равным p s, называется
точкой росы.
Массовое |
влагосодержание |
|
|
d- |
отношение |
массы |
влаги, |
||||
содержащейся во влажном воздухе G воды к массе сухого воздуха |
|||||||||||
G возд |
|
|
|
|
|
|
|
|
|
|
|
d |
Gводы |
, кг/кг сухого возд. |
|
|
|
(3) |
|||||
Gвозд |
|
|
|
||||||||
|
|
|
|
|
|
|
|
|
|
||
Мольное |
влагосодержание |
x |
- |
|
отношение |
числа |
молей |
||||
водяного пара к числу молей сухого воздуха. |
|
|
|||||||||
|
|
|
x |
Gводы |
|
возд |
|
|
(4) |
||
|
|
|
Gвозд |
воды |
|
||||||
|
|
|
|
|
|
|
|||||
так как возд= 28,96 и воды= 18,016, то с учетом (4) получим |
|||||||||||
|
|
|
|
x 1.61 d |
|
(5) |
|||||
или |
|
|
|
d 0.622 x |
|
|
|||||
|
|
|
|
|
|
(6) |
|||||
Величины d и х характеризуют влажный воздух, в котором вода может находится как в виде пара, так и в виде капелек влаги или кристалликов льда
Записав уравнение Клапейрона для сухого воздуха и для водяного пара, и разделив второе на первое. получим
40
