
методичка лаба термодинамика
.pdf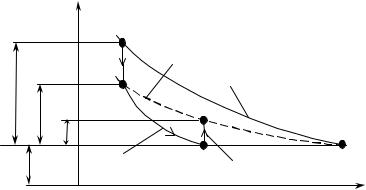
|
Расчет процессов |
|||
Рассчитать процесс - это значит найти параметры во всех |
||||
точках процесса, а также изменение внутренней энергии, |
||||
энтальпии, энтропии, подведенную (отведенную )теплоту и работу |
||||
процесса. |
|
|
|
|
Процесс сжатия 0-1 |
(рис. |
3) - политропный. Этот процесс |
||
характеризуется уравнением |
|
|
|
|
|
р vn = const, |
(12) |
||
где величина n называется показателем политропы. |
||||
Р |
1 |
|
|
|
|
|
|
|
|
|
|
Т =const |
|
|
Н0 |
|
|
PVn=const |
|
2 |
|
4 |
|
|
Н1 |
|
|
||
|
|
|
||
|
|
|
|
|
Н2 |
|
|
|
0 |
В |
PVk=const |
3 |
V=const |
|
|
|
|
Рис. 3 |
V |
|
|
|
|
|
Сжимая газ, мы подводим работу, которая приводит к |
||||
увеличению его внутренней энергии. Поскольку для идеального |
||||
газа внутренняя энергия зависит только от температуры, в этот |
||||
момент температура газа увеличивается, достигая температуры Т 1 |
||||
>Т о. Нарушение теплового равновесия системы с окружающей |
||||
средой приводит к потоку тепла, направленного в соответствии со |
||||
вторым законом термодинамики от более горячей системы к более |
||||
холодной окружающей среде. Работа, подведенная к системе в |
||||
политропном |
процессе, расходуется в |
соответствии с первым |
||
|
|
|
|
21 |
законом термодинамики на теплообмен с окружающей средой и изменение внутренней энергии системы.
Соотношение параметров в политропном процессе
|
T |
|
P |
|
n 1 |
|
||
|
|
|
|
|
|
|||
|
( |
) n |
|
|||||
|
1 |
1 |
(13) |
|||||
T0 |
P0 |
|||||||
|
|
|
|
|
||||
Из этого соотношения надо определить показатель политропы n. Для этого необходимо знать температуру Т 1. Эта температура определяется следующим образом. После того как в сосуд накачали воздух, давление в нем поднялось. Оба крана закрыты. Газ в сосуде имеет более высокую температуру, чем окружающая среда. Должно произойти выравнивание температур газа внутри сосуда и окружающей среды, т.е. процесс теплообмена между газом и средой. Температура газа в сосуде падает. Поскольку сосуд закрытый, рассматриваемый процесс является изохорным, в котором соотношение параметров будет определяться уравнением
|
T2 |
|
P2 |
(14) |
|
T1 |
P1 |
||||
|
|
|
При известных давлениях Р 1 = В + Но и Р 2 = В + Н1 и известной температуре Т2 = То определяется Т1.
Удельные объемы определяются из уравнения состояния
v |
|
|
RT0 |
|
|
(15) |
|||
|
p |
||||||||
0 |
|
|
|
|
|||||
|
0 |
|
|
|
|
||||
v |
RT1 |
|
|
(16) |
|||||
|
p |
||||||||
1 |
|
|
|
|
|||||
|
1 |
|
|
|
|
||||
Поскольку процесс 1-2 – изохорный, то v 2 |
= v 1 . |
||||||||
Проверить равенство значений этих удельных объемов |
|||||||||
можно. определив v2 из уравнения состояния |
|
||||||||
v |
|
RT2 |
|
(17) |
|||||
p |
|||||||||
2 |
|
|
|
|
|||||
|
2 |
|
|
|
|
||||
22

с учетом того, что Т2 = То.
Когда открывается кран 2, давление в сосуде падает до атмосферного. Если этот процесс происходит достаточно быстро, то его можно считать адиабатным. В процессе адиабатного расширения газ совершает работу. Поскольку процесс происходит достаточно быстро, теплообмен с окружающей средой не успевает произойти (dq = 0) и на основании первого закона термодинамики работа совершается за счет уменьшения внутренней энергии газа, которая зависит только от температуры. В связи с этим падает температура газа в сосуде. Соотношение параметров в адиабатном процессе 2-3
p v K |
p v K |
(18) |
||
2 |
2 |
3 |
3 |
|
где к - показатель адиабаты, определенный из опыта.
По известным P2, v2 ,P3 определяется удельный объем v3.
v3 ( p2 )1k v2
p3
Температуру Т3 можно определить из уравнения состояния
T |
p3v3 |
(19) |
|
R |
|||
3 |
|
Проверить значение температуры Т3 можно, воспользовавшись соотношением для адиабатного процесса
|
T |
|
P |
|
k 1 |
|
||
|
|
|
|
|
|
|||
|
( |
) k |
|
|||||
|
3 |
3 |
(20) |
|||||
T2 |
P2 |
|||||||
|
|
|
|
|
||||
После адиабатного расширения газа и закрытия крана 2 в закрытом сосуде начинает расти давление. Это связано с тем. что после адиабатного расширения газ охлаждается до температуры , меньшей чем температура окружающей среды. Затем начинается процесс выравнивания температур газа внутри сосуда и окружающей среды. Газ в закрытом сосуде начинает нагреваться. Это процесс изохорного подвода тепла 3-4. При известных Р4 и Т4= Т0 = Т2 можно определить
23
v |
|
RT4 |
(21) |
|
p |
||||
4 |
|
|
||
|
4 |
|
||
Поскольку процесс 3-4 - изохорный,
v 4 = v 3. |
(22) |
Определение изменения внутренней энергии, энтальпии, энтропии, теплоты и работы в различных процессах
0-1 - Политропный процесс р vn = const
Изменение внутренней энергии
u0-1 = C v (T1 - T0), |
(23) |
||||||
Подведенная (отведенная) теплота |
|
||||||
q0-1 = C n (T1 - T0), |
(24) |
||||||
Теплоемкость политропного процесса |
|
||||||
|
|
cn |
cv |
n k |
- |
(25) |
|
|
|
n 1 |
|||||
|
|
|
|||||
Изменение энтальпии |
|
||||||
h 0-1 = C p (T1 - T0), |
(26) |
||||||
Изменение энтропии |
|
||||||
s 0-1 = C n ln (T1 / T0), |
(27) |
||||||
Работа процесса |
|
|
|||||
l |
|
|
R |
|
(T T ), |
(28) |
|
|
n 1 |
||||||
|
0 1 |
|
0 |
1 |
|
||
24
l |
0 1 |
|
povo |
(1 |
T1 |
), |
|
|
|
|
|
(29) |
|||||||||||
|
|
|
|
|
|
|
|
|
|||||||||||||||
|
|
|
n 1 |
|
T |
|
|
|
|
|
|
|
|
|
|||||||||
|
|
|
|
|
|
|
|
|
|
|
|
|
o |
|
|
|
|
|
|
||||
|
|
l |
|
|
|
|
1 |
|
(p v p v ) |
(30) |
|||||||||||||
|
|
|
|
|
|
|
|
|
|
||||||||||||||
|
|
|
0 1 |
|
|
n 1 |
o o |
|
|
1 |
1 |
|
|||||||||||
|
|
|
|
|
|
|
|
|
|
1-2 Изохорный процесс v1 = v 2 = const |
|
||||||||||||
|
u 1-2= C v (T2- T1 ), |
|
(31) |
||||||||||||||||||||
|
h 1-2 |
=Cp (T2- T1 ), |
|
(32) |
|||||||||||||||||||
|
s 1-2= C v ln(T2/ T1 ), |
|
(33) |
||||||||||||||||||||
|
q1-2= u 1-2 |
|
|
|
|
|
|
|
|
(34) |
|||||||||||||
|
|
l1-2= 0 |
|
|
|
|
|
|
|
|
|
|
|
|
(35) |
||||||||
|
|
|
|
|
|
|
|
|
|
|
2-3 Адиабатный процесс р vк = const |
|
|||||||||||
|
|
|
|
q2-3 = 0, |
|
|
|
|
|
|
|
|
(36) |
||||||||||
|
|
|
|
u 2-3 = C v (T3- T2 ), |
(37) |
||||||||||||||||||
|
|
|
|
l |
|
= |
|
|
R |
(T - T ), |
(38) |
||||||||||||
|
|
|
|
|
|
|
|
||||||||||||||||
|
|
|
|
|
|
2-3 |
|
|
|
n 1 |
2 |
|
|
3 |
|
|
|||||||
|
|
|
|
l |
|
|
|
|
|
p2v2 |
|
|
|
T |
|
|
|||||||
|
|
|
|
2 3 |
|
(1 |
|
3 |
), |
(39) |
|||||||||||||
|
|
|
|
|
|
|
|
||||||||||||||||
|
|
|
|
|
|
|
|
|
|
n 1 |
|
T |
|
|
|||||||||
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
2 |
|
|
|
|
|
|
|
l |
|
|
|
|
1 |
|
(p |
v |
|
p v ) , |
(40) |
||||||||
|
|
|
|
|
|
n 1 |
|
||||||||||||||||
|
|
|
|
|
2 3 |
|
|
|
2 |
|
2 |
|
|
3 3 |
|
||||||||
|
|
|
|
h 2-3 |
=Cp (T3- T2 ), |
(41) |
|||||||||||||||||
|
|
|
|
s 2-3 = 0. |
|
|
|
|
|
|
|
|
(42) |
||||||||||
25
3-4 Изохорный процесс v3 =v 4 = const |
|
u3-4= C v (T4- T3 ), |
(43) |
h 3-4 =Cp (T4- T3 ), |
(44) |
s 3-4= C v ln(T4/ T3 ), |
(45) |
q3-4= u 3-4, |
(46) |
l3-4= 0. |
(47) |
0-2-4 Изотермический процесс T4= T2 =T0 |
|
u 0-4= 0, |
(48) |
h 0-4 =0, |
(49) |
l0-4= RT ln (v4 /v0), |
(50) |
l0-4= RT ln (po /p4), |
(51) |
l0-4= p1v1 ln (v4 /v0), |
(52) |
l0-4= p1v1 ln (po /p4), |
(53) |
q0-4= l0-4, |
(54) |
s 0-4= q0-4/ T, |
(55) |
s 0-4= R ln (po /p4), |
(56) |
s 0-4= R ln(v4 /v0), |
(57) |
0-3 Изобарный процесс р0 = р3 =const |
|
u 0-3= C v (T3- T0 ), |
(58) |
26
h 0-3 =Cp (T3- T0 ), |
(59) |
l0-3= р(v3- v0 ), |
(60) |
l0-3= R(T3- T0 ), |
(61) |
s 0-3= Cp ln(T3/ T0), |
(62) |
q0-3= h 0-3. |
(63) |
Построение процессов в T,s- диаграмме
Построение процессов в T,s- диаграмме начинается с определения координат тч. 0. (T0 ,s 0.). Значение s 0. определяется по таблицам термодинамических свойств воздуха по температуре T0. Далее от полученной точки откладывается изменение энтропииs0-1 в процессе 0-1 влево, если s 0-1 <0 и вправо, если s 0-1 >0. Получаем значение энтропии s 1. T1 известна, таким образом.
тч.1 определена. От тч. 1 откладывается значение s 1-2 влево, если
s 1-2 <0 и вправо, если s 1-2>0. Получаем значение энтропии s 2. в тч. 2. При известной T2 у нас определена тч. 2. По такой же схеме действуем и далее.
Лабораторная работа №4
ИЗУЧЕНИЕ ПРОЦЕССОВ СЖАТИЯ ИДЕАЛЬНОГО ГАЗА В КОМПРЕССОРЕ
Цель работы: Определение начальных и конечных параметров процесса сжатия газа в компрессоре.
Определение технической работы компрессора при сжатии а) одноступенчатом, б)двухступенчатом, в) трехступенчатом.
27
Процесс сжатия принять
политропным,
адиабатным,
изотермическим.
Изобразить индикаторную p,V- диаграмму, а также T,s - диаграмму процесса сжатия в компрессоре для вышеуказанных случаев.
Основные положения:
Компрессор - машина для сжатия газов. Компрессоры применяются а) как самостоятельные устройства, б) как элементы газотурбинных установок, в) как элементы холодильных установок и установок для сжижения газов.
По конструкции компрессоры делятся на 2 группы: - объемные (компрессоры статического сжатия) и лопаточные (компрессоры динамического сжатия). Объемные, в свою очередь, делятся на 2 типа - поршневые и ротационные.
По конечному давлению различают:
вакуум-компрессоры - машины, которые отсасывают газ из пространства с давлением ниже атмосферного,
компрессоры низкого давления служат для нагнетания газа при давлении от 0.15 до 1.2 МПа,
компрессоры среднего давления служат для нагнетания газа при давлении от 1.2 до 10 МПа,
компрессоры высокого давления служат для нагнетания газа при давлении от 10 до 100 МПа,
компрессоры сверхвысокого давления служат для нагнетания газа при давлении выше 100 МПа.
28
|
|
|
3 |
|
|
5 |
|
|
|
|
2 |
|
6 |
7 |
4 |
|
|
~ |
|
|
1 |
|
|
|
|
|
|
|
|
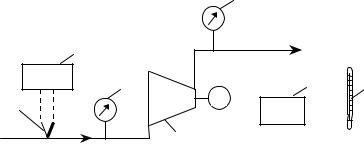
1 |
– компрессор; |
5 |
– милливольтметр; |
|
2, 3 – манометры; |
6 |
– барометр; |
|
|
4 – хромель-копелевая |
7 |
- термометр |
|
|
термопара; |
|
|
|
|
|
Рис.1. Cхема экспериментальной установки |
|
||
Порядок выполнения работы
Включить установку в сеть. Газ низкого давления поступает в компрессор. Избыточное давление газа на входе в компрессор регистрируется манометром 2, а температура - хромель-копелевой термопарой 4, показания которой выведены на милливольтметр 5. Избыточное давление газа за компрессором определяется по манометру 3. По термометру 7 определяется температура окружающей среды tос, необходимая для определения поправки на холодный спай термопар. По барометру определяется атмосферное давление В.
Таблица наблюдений
№№ |
Рман1, |
Рман2, |
Р 1 , |
Р 2 , |
t 1 , |
t 1 |
В, |
t ос,ОС |
пп |
ати |
ати |
МПа |
МПа |
мВ |
,ОС |
кПа |
|
|
|
|
|
|
|
|
|
|
29
Расчетные формулы
Абсолютные давления соответственно на входе в компрессор и на выходе из него
|
Р 1 = Рман1 ∙9.81∙ 104 + В, Па |
(1) |
||||||||||||||||||||||||||||
Р 2 = Рман2 ∙9.81∙ 104 + В, Па |
(2) |
|||||||||||||||||||||||||||||
Температура газа на выходе определится из соотношения |
|
|||||||||||||||||||||||||||||
Т |
|
|
( |
p |
|
) |
n 1 |
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|||||||
2 |
|
2 |
n |
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
(3) |
||||||||||
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|||||||||
|
Т1 |
p1 |
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|||||||||
n- показатель политропы, |
|
n=1.3 |
|
|
||||||||||||||||||||||||||
Техническая работа компрессора при одноступенчатом сжатии |
||||||||||||||||||||||||||||||
L |
|
n |
pV |
|
|
|
|
p2 |
|
|
|
n 1 |
|
|
||||||||||||||||
|
|
|
|
|
|
|
|
|
|
|
||||||||||||||||||||
|
|
( |
|
) n |
1 , кВт, |
(4) |
||||||||||||||||||||||||
n 1 |
|
|
|
|
||||||||||||||||||||||||||
|
|
|
|
|
|
|
1 |
1 |
|
|
|
|
p |
|
|
|||||||||||||||
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
1 |
|
|
|
|
|
|
|
|
|
где V1 - объемный расход газа, м3/с |
|
|||||||||||||||||||||||||||||
или |
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
L |
|
|
n |
GRТ |
|
|
|
|
p2 |
|
|
|
n 1 |
|
|
|||||||||||||||
|
|
|
|
|
|
|
|
|
|
|
||||||||||||||||||||
|
1 |
( |
|
) n |
1 , кВт, |
(5) |
||||||||||||||||||||||||
|
|
|
|
|
||||||||||||||||||||||||||
|
|
|
|
|
n 1 |
|
|
|
|
|
|
|
|
p |
|
|
||||||||||||||
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
1 |
|
|
|
|
|
|
|
|||
где G - массовый расход газа, кг/с. |
|
|||||||||||||||||||||||||||||
G = N / l, |
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
(6) |
||||||||
N = 0,2 кВт - мощность компрессора, |
|
|||||||||||||||||||||||||||||
l - удельная работа компрессора, кДж/кг. |
|
|||||||||||||||||||||||||||||
l |
n |
|
|
RТ |
|
|
p |
|
|
|
|
n 1 |
|
|
||||||||||||||||
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
||||||||||||||||
|
|
|
1 |
( |
|
2 |
) n 1 , кДж/кг, |
(7) |
||||||||||||||||||||||
n 1 |
|
|
||||||||||||||||||||||||||||
|
|
|
|
|
|
|
|
|
p |
|
|
|
|
|
|
|
|
|
|
|
|
|
||||||||
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
1 |
|
|
|
|
|
|
|
|
|
|
|
|
||
(площадь 12mn1) (рис.2)
При двухступенчатом сжатии в компрессоре удельная техническая работа определяется как
30
