

А.А. Евстрапов. Курс лекций «Нанотехнологии в экологии и медицине»
Так как размер наночастицы соизмерим с размерами белка, то это делает наноматериалы удобными для биомаркировки. Чтобы обеспечить взаимодействие с биологическим объектом, наночастица должна иметь соответствующее внешнее покрытие (слой), который обеспечивает специфическое взаимодействие. Примерами таких слоев могут являться антитела, биополимеры, монослои молекул, делающие наночастицы биологически совместимыми. Если используются оптические методы регистрации этих частиц, то частица должна обладать соответствующими оптическими свойствами (высоким поглощением, рассеянием, флуоресценцией). Если частица выполняет только транспортные функции, то важными становятся ее магнитные и электрические свойства, способность «вмещать» определенное количество «перевозимого» материала, устойчивость к проявлению внешних воздействий.
В настоящее время множество применений нашли магнитные наночастицы (рис. 7.1.6), в том числе для изучения клеток. Поскольку химия металлических поверхностей хорошо развита, то к металлическим наночастицам могут быть присоединены различные компоненты. Более того, можно пометить частицу даже несколькими флуоресцентными зондами так, что спектр флуоресценции будет нести информацию о том, какая реакция произошла. Магнитные свойства частицы могут использоваться при управлении их движением – перемещением в нужную область.
Рисунок 7.1.6. Магнитные наночастицы.
7.7.Применение квантовых точек при обнаружении биологических объектов.
Квантовая точка (quantum dot - QD) — фрагмент проводника или полупроводника, ограниченный по всем трём пространственным измерениям и содержащий электроны проводимости. Точка должна быть настолько малой, чтобы были существенны квантовые эффекты.
121
А.А. Евстрапов. Курс лекций «Нанотехнологии в экологии и медицине»
Диагностика заболеваний с помощью квантовых точек основана на отслеживании перемещения внутри организма различных веществ (лекарств, токсинов и т.д.). Определив эти движения, области накопления метки можно узнать степень распределения и введения новых препаратов. До применения квантовых точек вместо них использовали маркеры на основе органических красителей, что приводило к негативным побочным эффектам. В отличие от них квантовые точки как полупроводниковые кристаллы нанометрового размера лишены этого недостатка.
Квантовые точки (КТ) составных полупроводников успешно используются как замена органических флуоресцентных меток в различных биоаналитических применениях, а возможность объединения нескольких точек в одной конструкции – микрочастице, позволяет обеспечить флуоресценцию частицы на разных длинах волн. Такой подход позволяет реализовать различные комбинаторные методы исследования. Основной проблемой является создание вокруг КТ инертной стабильной оболочки, препятствующей прямому контакту КТ с биологическим образцом. Эта же оболочка должна позволять проводить иммобилизацию специфичных молекул или биологических маркеров, т.е. квантовые точки должны быть химически связаны с биологическими молекулами (антителами, пептидами, белками или ДНК), что позволит КТ избирательно соединяться с аналитом.
Примером практического использования квантовых точек для детектирования искомых объектов могут служить разработки Американской Военно-морской Научно-
исследовательской лаборатории (The U.S. Naval Research Laboratory - NRL). В этой лаборатории были созданы люминесцентные детекторы на основе полупроводниковых нанокристаллов или квантовых точек. КТ (CdSe или CdTe) имеют следующие привлекательные свойства для оптического обнаружения в видимой области спектра:
возбуждение в широкой полосе и фотолюминесценцию с узкой полосой эмиссии
(ширина в 0.5 максимума ~ 25-45нм). При этом удается одновременно возбуждать несколько частиц. К тому же КТ обладают исключительной фотохимической стабильностью и высоким квантовым выходом. Созданный в NRL наносенсор состоит из КТ, окруженных меченым белком. При реакции с меченым белком аналит замещает окрашенный меченый комплекс, изменяя флюоресценцию наносенсора, что может быть зарегистрировано оптическими методами. В NRL разрабатываются наносенсоры на КТ с целью получения высокоселективных и чувствительных детекторов патогенов и взрывчатых веществ.
В Корнельском университете (Cornell University) ученые занимаются созданием КТ для исследований живых тканей и клеток. Предложенная технология заключается в обработке КТ специальными покрытиями для придания нужных свойств. "Cornell dots" или "CU dots" - наночастицы, состоящие из ядра диаметром 2,2 нм, помещенного в кремниевую оболочку с флуоресцирующими молекулами. Такие КТ были успешно использованы при визуализации раковых клеток в образцах ткани человека, больного лейкемией.
8. Медицинские наномашины. 8.1.Нанороботы.
Нанороботы или наноботы — управляемые устройства, размер которых сопоставим с размерами молекул (в некоторых случаях допускается – до микронных размеров), составленные из наноразмерных компонентов и обладающие функциями движения, обработки и передачи информации, а также исполнения программ.
122

А.А. Евстрапов. Курс лекций «Нанотехнологии в экологии и медицине»
Нанороботостроение – мультидисциплинарная область, в которой сосредоточены совместные усилия физиков, химиков, биологов, программистов, инженеров и других специалистов для получения положительных результатов (рис. 8.1).
Рисунок 8.1. Взаимосвязь различных дисциплин при создании бионанороботов (C.
Mavroidis, 2008).
Существуют и другие определения, которые описывают наноробота как машину, способную точно взаимодействовать с наноразмерными объектами или способную манипулировать объектами в наномасштабе. Иногда даже крупные аппараты, такие как атомно-силовой микроскоп, считают нанороботами, т. к. они производит манипуляции
собъектами на наноуровне.
Вто время как микророботы, при создании которых используются технологии МЭМС, состоят из миллиардов атомов, нанороботы, вероятно, будут изготавливаться путем сборки индивидуальных атомов или молекул.
Существует множество сходств и различий между микро- и наноразмерными роботами. Различия, главным образом, касаются основных законов динамики. Макроразмерные роботы по существу подчиняются законам ньютоновой механики, тогда для нанороботов имеют место законы молекулярной квантовой механики. Кроме того, принципы неопределенности играют существенную роль в наноразмерных системах. Неопределенность положения наносистемы определяется правилами квантования и тепловыми полями.
Так как нанороботы невидимы для невооруженного глаза, то для работы с ними необходимо использовать методы высокоразрешающей микроскопии (сканирующей электронной микроскопии, атомно-силовой микроскопии, микроскопии ближнего поля). Для получения более полной информации о наноструктурах применяются методы моделирования виртуальной реальности (ВР) на основе получаемых сигналов от наноструктур. Эти методы в настоящее время отрабатываются в нанотехнологии и биотехнологии, как способ усилить восприятие оператора (визуальное и осязательное) для более адекватного представления о наноструктурах. Методы ВР также могут позволить: а) развить технологии сборки нано- и биокомпонентов роботов,
123
А.А. Евстрапов. Курс лекций «Нанотехнологии в экологии и медицине»
обслуживания и ремонта наноструктур; б) получить новые знания о процессах движения и взаимодействия на наноуровне.
Нанороботы с полностью искусственными компонентами пока еще не созданы и находятся в стадии научно-исследовательской разработки, но, тем не менее, имеются некоторые прототипы молекулярных машин. Исследования в этой области, в основном, сосредоточены на молекулярных машинах, идея которых подсказана природой.
Малые размеры нанороботов требуют большого их количества для выполнения микроскопических и макроскопических работ. Это приводит к необходимости рассмотрения некоторой колонии (стаи) роботов, их взаимодействия между собой и процессов управления. Выделяют нанороботов: а) способных к самостоятельному воспроизводству (репликации) в окружающей среде ("серая слизь" и др.) и б) не способных к репликации ("сервисный туман").
Серая слизь (термин впервые был использован Э. Дрекслером в его книге «Машины созидания», 1986 г.) — гипотетический сценарий конца света, связанный с разработкой молекулярных нанотехнологий и предсказывающий, что неуправляемые самореплицирующиеся нанороботы поглотят всю биомассу Земли, выполняя программу саморазмножения (сценарий известен также под названием «экофагия»). Дрекслер отмечает, что размножение в геометрической прогрессии из-за самовоспроизводства, по своей природе ограничено доступностью подходящего сырья.
Другой известный исследователь и эксперт в области нанотехнологий Р. Фрейтас для описания возможного сценария развития биосферы при выходе нанотехнологий из-под контроля предложил термин экофагия (от греч. Οικος — дом и Φαγος пожирающий). Сценарий предполагает, что никем не контролируемые самовоспроизводящиеся нанороботы «съедят» всё живое вещество на планете. Термин экофагия может применяться по отношению к любому явлению или процессу, способному изменить биосферу — ядерной войне, космическим катаклизмам, резкому сокращению биоразнообразия, чрезмерному размножению одного вида. Такие события могут привести к экоциду — нарушению способности биосферы к самовосстановлению.
Э. Дрекслер в своих работах описал некоторые методы лечения и диагностики на основе нанотехнологий. Ключевой проблемой этих методов является создание машин для ремонта клеток, прототипами которых являются нанороботы (ассемблеры или репликаторы). Медицинские нанороботы должны диагностировать болезни, доставлять лекарства и проводить хирургические операции. Кроме того, представляется актуальным проводить с помощь нанороботов анализ деятельности нервной системе, а также корректировку ДНК.
Типичный медицинский наноробот, по видимому будет иметь микронные размеры, которые дают возможность двигаться по капиллярам, и состоять (на базе нынешних взглядов) из высокопрочных и химически инертных материалов на основе углерода и его производных. В качестве основных источников энергии предполагается использовать локальные запасы глюкозы и аминокислот в теле человека. Лечение будет заключаться во введении нанороботов в человеческое тело для анализа ситуации и принятия решения о выборе метода лечения. Для коммуникации нанороботов в жидких средах могут быть использованы акустические сигналы, световые (электромагнитные) излучения, химические процессы. Химические реакции могут быть полезными для ближней ориентации и коммуникации нанороботов. Акустические сигналы являются
124
А.А. Евстрапов. Курс лекций «Нанотехнологии в экологии и медицине»
более предпочтительными на дальних расстояниях, а оптическая связь, хотя и является более быстродействующей, потребляет значительное количество энергии.
Существует классификация медицинских роботов в зависимости от выполняемых программ на микрофагоциты, респироциты, клоттоциты, васкулоиды и другие.
Микрофагоциты являются искусственными иммунными клетками, предназначенными для очищения крови от вредных микроорганизмов, обеспечения свертывания крови, транспорта кислорода и углекислого газа и расширения возможностей иммунной системы. Микрофагоциты будут находить в организме человека чужеродные элементы и перерабатывать их в нейтральные соединения.
Респироциты – аналоги эритроцитов (красных кровяных телец, доставляющих кислород к клеткам), которые должны иметь большую функциональность, чем природные эритроциты.
Клоттоциты - аналоги тромбоцитов (клеток, участвующих в свертывании крови). Эти машины позволят быстро прекращать кровотечения. Их функция заключается в оперативной доставке к месту кровотечения связывающей сети, которая должна задерживать кровяные клетки, останавливая ток крови. Время и место выброса сети задается внешними сигналами или определяется по парциальному давлению газов.
Васкулоид - механический протез, созданный на основе микрофагоцитов, респироцитов и клоттоцитов, и входящий в состав проекта по созданию робототехнической крови ("Roboblood", разработанный К. Фениксом и Р. Фрайтасом). В этом проекте описан комплекс медицинских нанороботов, способных жить и функционировать в теле человека, выполняя все функции естественной кровеносной системы.
В настоящее время развиваются разнообразные направления проектирования нанороботов: создаются элементы для зондирования, навигация, инструментарий для манипуляций, двигательные аппараты, молекулярные моторы и процессоры, предназначенные для решения медицинских задач. Хотя большая часть проблем наноизготовления не решена и отсутствуют детальные инженерные подходы, но уже создано «Сотрудничество по разработке нанофабрик» (основанное Р. Фрейтасом и Р. Меркле в 2000 году). Деятельность «Сотрудничества» связана с разработкой практической программы исследований по созданию контролируемой алмазной механосинтетической нанофабрики, которая будет способна производить медицинские нанороботы на основе алмазных соединений. Существуют и другие подходы к созданию нанороботов, основанные на использовании биологических молекул и структур.
Предполагается, что нанороботы могут составлять любую пассивную или активную структуру (в наномасштабе) способную к некоторым действиям, чувствительности к компонентам, передаче сигналов, обработке информации, интеллектуальному поведению роя роботов. Поэтому уместно привести некоторые характерные способности, желательные для функционирования нанороботов:
1.Интеллект роя (кооперативный и распределенный интеллект),
2.Совместное (взаимоувязанное) поведение,
3.Самосборка и репликация,
4.Обработка информации и программируемость (важно для автономных нанороботов),
125
А.А. Евстрапов. Курс лекций «Нанотехнологии в экологии и медицине»
5. Наличие соответствующей архитектуры интерфейсов от нано- к макро, позволяющей получить мгновенный доступ к нанороботу для его управления и обслуживания.
Эксперты выделяют следующие потенциальные сферы применения нанороботов в недалеком будущем:
•диагностика рака и целенаправленная доставка лекарств в раковые клетки,
•биомедицинский инструментарий,
•хирургия,
•фармакокинетика,
•мониторинг больных диабетом,
•производство посредством молекулярной сборки нанороботами устройства из отдельных молекул по его чертежам,
•военные технологии,
•космические исследования и разработки.
8.2.Бионанороботы. Основные принципы создания бионаноробототизированных систем. Управление нанороботами.
Бионанороботы – нанороботы, при создании которых используются биологические материалы (в том числе белки, ДНК и т.д.). Например, К. Мавродис (Constantinos Mavroidis) полагает, что при разработке бионанороботов следует руководствоваться следующими принципами:
−использование модульной организации и иерархии;
−применение концепции универсального шаблона, из которого можно создать любую требуемую систему;
−создание информационных модулей, в том числе для хранения, обработки информации и программирования;
−объединение информационных модулей с функциональными возможностями роста и развития (основа бионаноинтеллекта).
Модульная организация определяет фундаментальные правила и иерархию построения бионаноробототизированных систем. Построение осуществляется через устойчивую интеграцию индивидуальных биомодулей или нанокомпонентов, которые впоследствии и составят наноробот. Модульная организация позволяет бионанороботам с определенными свойствами организовывать рои, что является желательным для некоторых применений.
Модульная организация дает возможность создавать достаточно сложные многофункциональные бионанороботы, например, состоящие из биомодулей A, B, C и D (рис. 8.2). В модуле А (SPHERE) могут быть расположены система энергоснабжения и информационный блок робота. Элемент DISC представляет некоторую пространственную область, определенную для Модуля D и для возможных его связей с другими внутренними ядрами. Окружающее ядро кольцо представляет пространственную область, определенную на внутреннем ядре для закрепления Модуля B и Модуля C.
Модульная конструкция предполагает наличие универсального шаблона для бионаносистем и элементов, которые возможно трансформировать в любую наносистему с требуемыми свойствами. Эта концепция повторяет природную концепцию развития
126

А.А. Евстрапов. Курс лекций «Нанотехнологии в экологии и медицине»
эмбриональных стволовых клеток, которые являются своего рода примитивными клетками, но дают начало всем другим специализированным тканям человеческого тела.
Чтобы точно управлять биомолекулами необходимы инструменты, которые могут взаимодействовать с этими объектами в нано масштабе в естественных окружающих средах. Существующие бионанометоды манипуляции могут быть классифицированы как бесконтактные манипуляции, включая методы оптического и магнитного пинцета, и контактные манипуляции, например, взаимодействия через зонд АСМ.
Управление наноробототехническими системами может осуществляться: i) внутренними механизмами управления, ii) внешними механизмами управления или гибридом внутренних и внешних механизмов управления.
Внутренний механизм управления может быть активным и пассивным. Пассивный механизм - традиционный тип управления, который зависит от биохимической чувствительности и селективности связей биомолекул с другими элементами. Этот механизм эффективен, если известно как различные биомолекулы влияют на целевую молекулу. Активный механизм управления является более сложным, так как предполагает изменение свойств элементов наноробота в зависимости от внешнего окружения (или от ситуации). В этом случае полезным является использование концепций молекулярных компьютеров.
Внешний механизм управления предполагает воздействие внешних полей на наноробот, приводящее к изменению динамики его движения в среде. Аналогичный подход используется, например, при управлении движением и ориентацией магнитных наночастиц в градиенте магнитного поля.
Рисунок 8.2. Модульная организация бионаноробота.
127
А.А. Евстрапов. Курс лекций «Нанотехнологии в экологии и медицине»
8.3.Молекулярные машины. Наноразмерные исполнительные механизмы.
Всовременной инженерии (в том числе и роботостроении) достаточно часто и успешно используется биомиметика, позволяющая создавать эффективные конструкции. Биомиметика (от лат. bios — жизнь, и mimesis — подражание) - подход к созданию технологических устройств, при котором идея и основные элементы устройства заимствуются из живой природы.
Важным элементом наноробота является механизм, позволяющий ему перемещаться в пространстве. В природе встречается множество отработанных в течение столетий нанотехнологических механизмов и конструкций, принципы действия которых успешно используются в технике. Например, в некоторых конструкциях применяется принцип «ресничного» движения, встречающийся в природе (рис. 8.3 а). За счет колебания упругих элементов - «ресничек» осуществляется перемещение предметов или же движение объекта по поверхности (рис. 8.3 б).
Биологические системы имеют совершенные молекулярные машины, действующие по адаптивной программе, зачастую поражающей своей эффективностью, а порой - и сложностью. К таковым следует отнести и молекулярные двигатели. Большинство естественных молекулярных механизмов в природе создано на основе белков, которые служат для решения задач транспорта, катализа реакций и т.д., в то время как ДНК выполняет в основном роль информационного хранилища.
Молекулярные двигатели - наноразмерные машины, способные осуществлять вращение при приложении к ним энергии. Традиционно термин "молекулярный двигатели" применяется, когда речь заходит об органических белковых соединениях. Однако, в настоящее время его применяют и для обозначения неорганических молекулярных двигателей и используют в качестве обобщающего понятия. Возможность создания молекулярных моторов впервые была озвучена Р. Фейнманом в 1959 году.
8.3.1. АТФ-синтаза.
АТФ-синтаза — фермент, осуществляющий реакцию синтеза АТФ из АДФ и фосфатаниона за счёт энергии трансмембранного протонного градиента, преобразуя её, таким образом, в энергию химических связей, которая может быть использована клеткой в биохимических реакциях. В случае, если фермент проводит обратный процесс: формирует трансмембранный протонный градиент за счёт гидролиза АТФ — его называют аденозинтрифосфатазой, или АТФ-азой. Было установлено, что при гидролизе АТФ одна из частей энзима совершает вращательное движение, что может быть использовано при создании молекулярного двигателя.
Аденозинтрифосфорная кислота (АТФ, аденинтрифосфорная кислота) — нуклеотид, играет исключительно важную роль в обмене энергии и веществ в организмах; в первую очередь соединение известно как универсальный источник энергии для всех биохимических процессов, протекающих в живых системах. Главная роль АТФ в организме связана с обеспечением энергией многочисленных биохимических реакций. Являясь носителем двух высокоэнергетических связей, АТФ служит непосредственным источником энергии для множества энергозатратных биохимических и физиологических процессов. Все это - реакции синтеза сложных веществ в организме: осуществление активного переноса молекул через биологические мембраны, в том
128

А.А. Евстрапов. Курс лекций «Нанотехнологии в экологии и медицине»
числе, для создания трансмембранного электрического потенциала; осуществления мышечного сокращения.
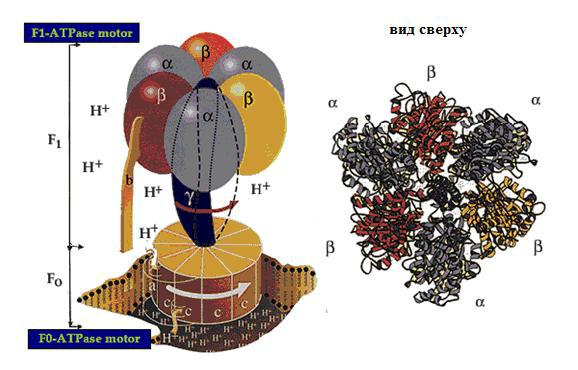
АТФ-аза состоит из двух отдельных частей: (1) F0, гидрофобной части, связанной с мембраной, ответственной за транспорт протонов, и (2) F1, гидрофильной части, ответственной за синтез и гидролиз АТФ (см. рис.8.4). Размер комплекса АТФ-азы ~ 12 нм в диаметре. По мере того как протоны протекают через F0 часть энзима, γ- субъединица части F1-ATФазы вращается по часовой стрелке и идет синтез АТФ.
Рисунок 8.3. Принцип «ресничного» движения: a) система перемещения объекта, используемая в природе. б) изображение микроконвейера, основанного на принципе «ресничного» движения [H. Fujita, Университет Токио, Японии]
Гидролиз АТФ происходит при вращении γ-субъединицы против часовой стрелки; при этом направление протекания протонов меняется на обратное. Субъединицы a, b, и c части F0-АТФ-азы формируют канал переноса протонов через клеточную мембрану. Места катализа и присоединения нуклеотидов были обнаружены исследователями (Kinosita и др., 1998) на трех α и трех β субъединицах части F1-ATФ-азы. γ- субъединица расположена в центре гексамера α3β3 и вращается при синтезе или гидролизе АТФ. Итак, АТФ-аза превращает движение протонов внутри клетки в механическое вращение по оси, помогая образовывать АТФ. Причем действие АТФазы обратимо: если на этот цилиндрический моторчик подавать АТФ, он будет "сжигать" ее, и ось придет во вращение. Японские биохимики из Токийского технологического института смогли наблюдать это движение, прикрепив к концу оси
129
А.А. Евстрапов. Курс лекций «Нанотехнологии в экологии и медицине»
флуоресцирующую молекулу. Исследователи заключили, что кпд такого двигателя близок к ста процентам.
Рисунок 8.4. Строение и модель энзима АТФ-аза
8.3.2. Кинезин, миозин, жгутиковый молекулярный двигатель.
Другой известный биологический двигатель - молекула белка кинезина. Представители семейства кинезинов играют важную роль во многих клеточных процессах. Молекула кинезина может двигаться вдоль полимерных нитей, используя в качестве "топлива" молекулы АТФ. К подобным двигателям относятся белки актомиозинового комплекса, входящего в состав сократительного аппарата мышц. Движение микроворсинок (жгутиков и ресничек бактерий и простейших) определяется взаимодействием другой пары моторных белков - динеина и тубулина. Смещение головок динеина относительно тубулиновых микротрубочек белков обеспечивает волнообразные движения микроворсинок. Среди большого числа моторных белков миозин скелетных мышц и кинезин из клеток мозга являются наиболее изученными молекулярными моторами. Несмотря на то, что функции миозина и кинезина в клетке различаются, они похожи по своему строению и механизмам действия.
Совместно с микротрубками цитоскелета молекула кинезина выполняет транспорт веществ внутри клетки и перемещение везикул. Микротрубки играют роль своеобразных направляющих, по которым перемещаются молекулы белков кинезина с полезным грузом. Один конец этой молекулы прикрепляется к везикуле, которую необходимо транспортировать, а другой - к микротрубке, которая направляет движение
(рис. 8.5).
Молекула кинезина представляет собой димер, образованный двумя одинаковыми полипептидными цепями. С одной стороны каждой полипептидной цепи кинезина
130
