
МОЛЕКУЛЯРНАЯ ФИЗИКА И ТЕРМОДИНАМИКА_пособие
.pdf
используется в холодильных машинах (за счет работы внешних сил теплота переносится к телу с более высокой температурой).
КПД кругового процесса: в результате кругового процесса система возвращается в исходное состояние, следовательно, полное изменение внутренней энергии равно нулю. Поэтому ΔQ ΔU A А , т.е. работа, совершаемая за цикл, равна количеству полученной извне теплоты. Если в ходе кругового процесса система не только получает количество теплоты Q1, но и теряет (отдает) количество теплоты Q2 , то Q Q1 Q2 .
Термический коэффициент полезного действия для кругово-
го процесса - это величина, равная отношению работы, совершенной системой, к количеству теплоты, полученному в этом цикле системой:
η A Q1 Q2 1 Q2 Q1 Q1 Q1
Термодинамический процесс называется обратимым, если он может происходить как в прямом, так и в обратном направлении. Причем, если такой процесс происходит сначала в прямом, а затем в обратном направлении и система возвращается в исходное состояние, то в окружающей среде и в этой системе не происходит никаких изменений. Всякий процесс, не удовлетворяющий этим услови-
ям, является необратимым.
Реальные процессы необратимы, в них всегда происходит диссипация (потеря) энергии (из-за трения, теплопроводности и т.д.). Обратимые процессы - это физическая модель (идеализация реальных процессов).
2.6. Энтропия
Количество тепла δQ , которое должно быть доставлено системе или отнято у неё при переходе от одного состояния в другое, не определяется однозначно начальным и конечным состояниями, но существенно зависит от способа осуществления этого перехода (δQ не является функцией состояния системы).
Однако приведенное количество теплоты - отношение теплоты δQ к температуре T системы при бесконечно малых изменени-
ях состояния системы - есть функция состояния системы. В любом
δQ
обратимом круговом процессе:  T 0 . Следовательно, подинте-
T 0 . Следовательно, подинте-
гральное выражение есть полный дифференциал некоторой функции, которая определяется только начальным и конечным состоя-
30

ниями системы и не зависит от пути, каким система пришла в это состояние.
Энтропией S называется функция состояния системы, диф-
ференциалом которой является δQ :
T
dS δQ . T
Таким образом, первое начало термодинамики δQ dU δA можно записать в виде TdS dU δA.
В замкнутой системе для обратимых процессов ΔS 0; для необратимых циклов ΔS 0. Последние два условия можно предста-
вить виде неравенства Клаузиуса: энтропия замкнутой системы может либо возрастать (в случае необратимых процессов) либо оставаться постоянной (в случае обратимых процессов):
ΔS 0.
Поскольку dS и δQ имеют один и тот же знак, то по характе-
ру изменения энтропии можно судить о направлении процесса теп-
лообмена. При нагревании тела δQ 0 , и его энтропия возрастает dS 0, при охлаждении δQ 0 , и энтропия тела убывает dS 0 .
Изоэнтропийным называется процесс, протекающий при по-
стоянной энтропии (S const ). В обратимом адиабатном процессе
δQ TdS 0, так что dS 0 и S const , поэтому адиабатный процесс является изоэнтропийным.
Рассмотрим для примера идеальный газ, совершающий равновесный переход из состояния 1 в состояние 2. Изменение его энтропии
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
2 |
δQ |
2 |
dU δA |
|
|
|
|
||
|
|
|
|
|
|
|
|
|
|
|
|
|
ΔS1 2 S2 S1 |
|
. |
|
|
|
||||||||||||
|
|
|
|
|
|
|
|
|
|
|
|
|
|
T |
T |
|
|
|
||||||||||||
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
1 |
|
|
|
1 |
|
|
|
|
|
|
|
|
Используя |
|
|
известные |
|
|
|
|
соотношения: |
dU |
m |
CVdT ; |
||||||||||||||||
|
|
|
|
|
|
|
|
|||||||||||||||||||||||
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
M |
|
δA pdV |
m |
RT |
dV |
; |
R Cp CV |
|
и |
T2V1 |
|
p2 |
|
, можно получить выражение |
||||||||||||||||||
|
|
|
|
|
|
p1 |
||||||||||||||||||||||||
|
|
|
|
M |
|
V |
|
|
|
|
|
|
|
|
T V |
2 |
|
|
|
|
|
|
|
|
||||||
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
1 |
|
|
|
|
|
|
|
|
|
|
||
ΔS |
1 2 |
|
m |
(C |
V |
ln |
p2 |
C |
p |
ln |
V2 |
) |
, |
которое показывает, что изменение эн- |
||||||||||||||||
|
|
|
||||||||||||||||||||||||||||
|
|
M |
|
p |
1 |
|
|
V |
|
|
|
|
|
|
|
|
|
|
|
|
|
|
||||||||
|
|
|
|
|
|
|
|
|
|
|
|
|
1 |
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
||
тропии идеального газа при переходе его из состояния 1 в состояние 2 не зависит от вида процесса этого перехода (табл.1).
31
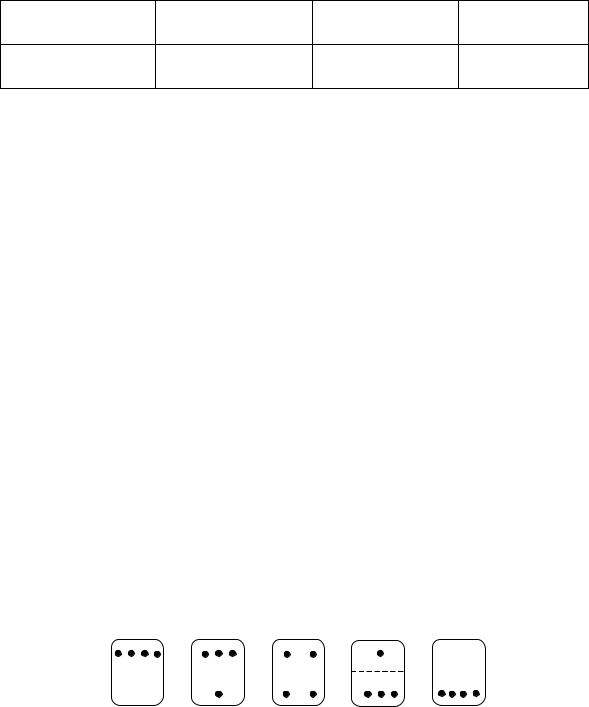
Таблица 1 Изменение энтропии в процессах идеального газа
Изохорный |
Изобарический |
Изотермический |
Адиабатический |
(V const ) |
(p const ) |
(T const ) |
(S const ) |
|
m |
T2 |
|
m |
V2 |
|
m V2 |
ΔS 0 |
||||
ΔS |
|
CVln |
|
ΔS |
|
Cpln |
|
ΔS |
|
Rln |
|
|
M |
T |
M |
V |
M |
V1 |
|
||||||
|
|
|
1 |
|
|
|
1 |
|
|
|
|
|
Статистическое толкование энтропии
Термодинамическая вероятность W состояния тела или сис-
темы – это число способов, которыми может быть реализовано данное конкретное термодинамическое состояние (макросостояние). Иначе говоря, это число всевозможных микрораспределений частиц по координатам и скоростям (микросостояний), которыми может быть осуществлено данное макросостояние.
Термодинамическая вероятность связана с энтропией формулой Больцмана:
S kln W ,
где k - постоянная Больцмана.
Энтропия является мерой неупорядоченности системы: чем больше число микросостояний, реализующих данное макросостояние, тем больше энтропия.
Пусть имеется замкнутый объем, разделенный на две половины проницаемой перегородкой (мембраной). В этом замкнутом объеме имеются четыре, пронумерованные молекулы – 1, 2, 3, 4 - которые могут располагаться по разные стороны мембраны. Возможные варианты распределения молекул представлены на рис.13. Подсчитаем число способов, с помощью которых может реализоваться та или иная комбинация распределения молекул в этом объеме.
I |
II |
III |
IV |
V |
Рис.13. Варианты распределения четырех молекул в замкнутом объеме |
||||
|
Состояние I реализуется всего одним способом. |
|
|
Состояние II реализуется четырьмя способами: 234 1, |
134 2, |
124 3, 123 4. |
|
|
|
Состояние III реализуется шестью способами: 12 34, |
13 24, |
14 23, |
23 14, 24 13, 34 12. |
|
32
Состояние IV реализуется четырьмя способами: 1 234, 2 134,
3 124,4 123.
Состояние V реализуется одним способом.
Ясно, что состояние III наиболее вероятно, оно и реализуется наибольшим числом способов - шестью. Состояния II и IV менее вероятны, они характеризуются меньшим числом способов - четырьмя. Состояния I и V маловероятны и реализуются всего одним способом.
В математике известна формула, с помощью которой можно подсчитать число сочетаний W из N элементов по n :
|
|
WNn |
|
|
N! |
|
|
|
|
|
|
n! N n ! |
|
|
|||||
Например, W0 |
|
4! |
|
1, |
W1 |
4! |
4 и т.д. |
||
0! 4 0 ! |
|
|
|||||||
4 |
|
|
|
4 |
1! 4 1 ! |
||||
Таким образом, число сочетаний W соответствует вероятности данного состояния.
Принцип возрастания энтропии. Все процессы в замкну-
той системе ведут к увеличению её энтропии. В замкнутой системе процессы идут в направлении от менее вероятных, состояний к более вероятным, до тех пор, пока вероятность состояния не станет максимальной. В состоянии равновесия - наиболее вероятном состояния системы - число микросостояний максимально, при этом максимальна и энтропия.
2.7. Второе и третье начала термодинамики
Второе начало термодинамики: любой необратимый процесс в замкнутой системе происходит так, что энтропия системы при этом возрастает (закон возрастания энтропии).
Если первое начало термодинамики выражает закон сохранения и превращения энергии применительно к термодинамическим процессам безотносительно их направления, то второе начало термодинамики определяет направление протекания термодинамических процессов, указывая, какие процессы в природе возможны, а какие - нет.
Существуют ещё две формулировки второго начала термодинамики:
1)по Кельвину: невозможен круговой процесс, единственным результатом которого является превращение теплоты, полученной от нагревателя, в эквивалентную ей работу;
2)по Клаузиусу: невозможен круговой процесс, единственным результатом которого является передача теплоты от менее нагретого тела к телу более нагретому.
33

Третье начало термодинамики - теорема Нернста-Планка -
постулирует поведение термодинамических систем при нуле Кельвина: энтропия всех тел в состоянии равновесия стремится к нулю по мере приближения температуры к нулю Кельвина:
lim S 0 .
T0
2.8.Тепловые двигатели и холодильные машины
Тепловой двигатель - это периодически действующий двигатель, совершающий работу за счет полученной извне теплоты.
Термостатом называется термодинамическая система, которая может обмениваться теплотой с телами практически без изменения собственной температуры.
Рабочее тело - это тело (газ или пар), совершающее круговой процесс и обменивающееся энергией с другими телами.
Принцип работы теплового двигателя: от термостата с более высокой температурой T1 , называемого нагревателем, за цикл отнимается количество теплоты Q1 , а термостату с более низкой температурой T2 , называемому холодильником, за цикл передается количество теплоты Q2 . При этом рабочее тело расширяется и совершает работу A Q1 Q2 (рис.14).
T1 T2 |
|
T1 |
|
|
|
|
Q1 |
Q1 |
|||||
|
|
|
A |
|
|
|
A |
|
|
|
|
Холодильная |
|||
Тепловой двигатель |
|
|
|
||||
|
|
машина |
|
||||
|
|
|
|
|
|
||
|
|
|
|
|
|
|
|
|
Q 2 |
Q 2 |
|||||
|
T2 T1 |
|
|
|
T2 |
|
|
|
|
|
|
|
|
|
|
Рис.14. Принцип работы теплового двигателя и холодильной машины
Термический КПД двигателя:
η A Q1 Q2 1 Q2
Q1 |
Q1 |
Q1 |
Чтобы КПД был равен 1, |
необходимо, чтобы Q2 0, а это |
|
«запрещено» вторым началом термодинамики.
Процесс, обратный происходящему в тепловом двигателе,
используется в холодильной машине: от термостата с более низкой температурой T2 за цикл отнимается количество теплоты Q2 и отда-
34

ется термостату с более высокой температурой T1. При этом
Q Q1 Q2 A или Q1 Q2 A .
Количество теплоты Q1, отданное системой термостату T1 , больше количества теплоты Q2 , полученного от термостата T2 , на величину работы, совершенной над системой.
Эффективность холодильной машины характеризует холодильный коэффициент η' - отношение отнятой от термостата с более низкой температурой количества теплоты Q2 к работе A , которая затрачивается на приведение холодильной машины в действие:
η' |
Q2 |
|
|
Q2 |
. |
|
A |
|
|
||||
|
|
Q Q |
2 |
|
||
|
|
|
1 |
|
|
|
Теорема Карно
Из всех периодически действующих тепловых машин, имеющих одинаковые температуры нагревателей T1 и холодильни-
ков T2 , наибольшим КПД обладают обратимые машины. При этом КПД обратимых машин равны друг другу и не зависят от природы рабочего тела, а определяются только температурами нагревателя и холодильника.
P |
1 |
|
|
Для |
построения |
рабочего |
|
|
|
цикла использует обратимые процессы. |
|||||
Иэотермы |
|
||||||
|
|
|
|||||
|
Q1 0 |
Например, цикл Карно (табл.2) состоит |
|||||
|
|
Адиабаты |
|||||
|
AП 0 2 |
из двух изотерм (1–2, 2-4), в которых |
|||||
|
4 |
|
|
теплота полностью превращается в ра- |
|||
|
Q2 0 3 |
боту, и двух адиабат (2-3, 4–1), в кото- |
|||||
0 |
|
V |
рых изменение |
внутренней |
энергии |
||
|
полностью |
превращаются в |
работу |
||||
|
Рис.15. Цикл Карно |
||||||
|
(рис.15). |
|
|
|
|||
|
|
|
|
|
|
|
|
|
Рассмотрим изменение энтропии рабочего тела. Общее из- |
||||||
менение энтропии в цикле: |
ΔS ΔS12 ΔS23 |
ΔS34 ΔS41 Так как мы рас- |
|||||
сматриваем только обратимые процессы, общее изменение энтропии
ΔS 0.
35
Таблица 2 Последовательные термодинамические процессы в цикле Карно
Процесс |
|
|
|
|
|
Работа |
|
|
|
|
|
Изменение |
Результат |
||||||||||||||||||
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
энтропии |
|
|||||||
Изотермическое |
|
|
|
|
|
|
|
|
|
|
m |
|
|
|
|
|
V |
|
ΔS12 |
|
|Q1 | |
Тело принимает |
|||||||||
расширение 1—2 |
A |
12 |
Q |
1 |
|
|
|
|
RT ln |
2 |
|
|
|
|
|
|
теплоту |
||||||||||||||
|
|
|
T1 |
|
|
||||||||||||||||||||||||||
|
|
V |
|
|
|||||||||||||||||||||||||||
|
|
|
|
|
|
M |
|
1 |
|
|
|
|
|
|
|
|
|
|
|||||||||||||
T const; V2 V1, |
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
1 |
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
||
Адиабатическое |
A23 |
|
m |
|
CV |
(T2 |
T1) |
|
ΔS23 0 |
|
|
Охлаждение |
|||||||||||||||||||
расширение 2—3 |
|
M |
|
|
|
|
|
|
|
|
|
до Т2 |
|||||||||||||||||||
δQ 0; T2 T1 |
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
Изотермическое |
|
|
|
|
m |
|
|
|
|
|
|
V |
|
|
|
|
|
|
|
|
|Q |
2 |
| |
|
Тело отдает теплоту |
||||||
сжатие 3-4 |
|
A |
|
|
|
|
|
|
RT ln |
|
4 |
|
|
Q |
|
ΔS |
34 |
|
|
|
|
|
|||||||||
|
|
|
|
|
|
|
|
|
|
|
|
|
|||||||||||||||||||
|
|
34 |
|
|
M |
|
|
2 |
|
|
V |
|
|
|
|
2 |
|
|
|
T |
|
|
|
|
|||||||
T const;V3 |
V4 , |
|
|
|
|
|
|
|
|
|
|
|
|
|
|
3 |
|
|
|
|
|
|
|
|
2 |
|
|
|
|||
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
||
Адиабатическое |
|
|
|
|
m |
|
|
|
|
|
|
|
|
|
|
|
|
|
ΔS41 0 |
|
|
Восстановление |
|||||||||
сжатие |
|
A41 |
|
|
CV (T1 |
T2 ) A23 |
|
|
|
|
|
|
|
|
начального состояния |
||||||||||||||||
|
|
M |
|
|
|
|
|
|
|
|
|||||||||||||||||||||
δQ 0; T T |
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
p1,V1,T1 |
|
1 |
2 |
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
Общее изменение энтропии в равновесном цикле:
|
Q1 |
|
Q2 |
|
T |
|
|
Q2 |
, поэтому |
|
T |
- максимальный |
ΔS |
|
0 |
|
0 0 |
2 |
|
|
|
ηmax 1 |
2 |
||
|
|
|
|
|
||||||||
T1 |
T2 |
T1 |
|
Q1 |
T1 |
|||||||
|
|
|
|
|
|
|
|
КПД теплового двигателя.
Следствия:
1.КПД цикла Карно не зависит от рода рабочего тела.
2.КПД определяется только разницей температур нагревателя и холодильника.
3.КПД не может быть 100% даже у идеальной тепловой машины, так как при этом температура холодильника должна быть T2 0 , что запрещено законами квантовой механики и третьим зако-
ном термодинамики.
4. Невозможно создать вечный двигатель второго рода, работающий в тепловом равновесии без перепада температур, т.е. приT2 T1, так как в этом случае ηmax 0.
Тепловые двигатели повышают энтропию замкнутой систе-
мы.
36

3.РЕАЛЬНЫЕ ГАЗЫ
3.1.Уравнение Ван-дер-Ваальса
Как показывают эксперименты, модель идеального газа позволяет описывать поведение разреженных реальных газов лишь при «нормальных» условиях, т.е. при достаточно низком давлении и высокой температуре. При высоких давлениях или низких температурах уравнение состояния дает большие расхождения с результатами экспериментов.
При выводе уравнения состояния идеального газа не учитывались размеры молекул и потенциальная энергия их взаимодействия. Поэтому физическая природа газа не играла никакой роли, и уравнение состояния универсально и применимо ко всем газам. Повышение давления приводит к уменьшению среднего расстояния между молекулами, значит, необходимо учитывать объем молекул и взаимодействие между ними.
Учитывая собственный объем молекул и силы межмолекулярного взаимодействия, Ван-дер-Ваальс вывел уравнение состояния реального газа, введя в уравнение Клапейрона-Менделеева две поправки: учет собственного объема молекул и учет притяжения молекул.
1. Учет собственного объема молекул. Для движения моле-
кул предоставлен не весь объем Vm , занимаемый газом, а меньший на величину объема всех молекул газа - Vm b , где b - суммарный объем молекул газа, Vm - молярный объем. Расчеты показывают, что константа b численно равна учетверенному объему молекул, содер-
жащихся в моле газа. Размерность поправки b м3 .
моль
2. Учет притяжения молекул. Действие сил притяжения молекул газа приводит к появлению дополнительного давления на газ,
называемого внутренним давлением. Внутреннее давление p' равно
p' ~ |
a |
|
|
, |
|
V2 |
||
|
m |
|
где a – постоянная Ван-дер-Ваальса, характеризующая силы притя-
жения молекул. Размерность коэффициента: a H м4 .
моль2
Вводя эти поправки, получим уравнение Ван-дер-Ваальса для моля газа (уравнение состояния реальных газов):
37

|
a |
|
|
|
|
|
p |
V |
b RT . |
(23) |
|||
V2 |
||||||
|
|
m |
|
|
||
|
m |
|
|
|
||
Для произвольного количества вещества ν газа с учетом того, что V νVm , уравнение (23) примет вид:
|
ν |
2 |
a |
|
p |
|
V νb νRT , |
||
|
|
2 |
||
|
V |
|
||
|
|
|
||
где поправки a и b - постоянные для каждого газа величины, определяемые опытным путем.
3.2. Внутренняя энергия реального газа
Внутренняя энергия реального газа будет определяться суммой кинетической энергии ЕК теплового движения его молекул и потенциальной энергии взаимодействия молекул между собой ЕП :
U EK EП .
Потенциальная энергия реального газа обусловлена только силами притяжения между молекулами. Наличие последних приво-
дит к возникновению внутреннего давления p' на газ.
Работа, затрачиваемая на преодоления сил притяжения, равна приращению энергии. Следовательно, можно записать:
δA dEП p'dV Va2 dVm .
m
Проинтегрировав это уравнение, получим:
EП
a
Vm
Здесь постоянная интегрирования принята равной нулю; знак минус означает, что молекулярные силы, создающие дополнительное давление, являются силами притяжения. Окончательно внутренняя энергия моля реального газа
U |
C |
V |
T |
a |
. |
(24) |
|
||||||
m |
|
|
V |
|
||
m
Из формулы для внутренней энергии реального газа следует, что его внутренняя энергия растет как с увеличением температуры, так и с увеличением объема. Если реальный газ будет расширяться или сжиматься адиабатически и без совершения внешней работы, то для него, согласно первому началу термодинамики:
ΔQ ΔU ΔA; ΔQ 0,ΔA 0; ΔU 0 U const ,
и внутренняя энергия должна оставаться постоянной.
38
Поэтому из формулы (24) для реального газа, совершающего адиабатический переход без совершения работы, можно записать:
|
|
|
a |
1 |
|
1 |
|
|
T T |
2 |
|
|
|
|
|
|
. |
|
V |
V |
||||||
1 |
|
CV |
|
|
||||
|
|
|
|
|
m1 |
|
m2 |
|
Из этого уравнения следует, что изменение объема и изменение температуры имеют разные знаки. Следовательно, при адиабатном расширении в вакуум реальный газ должен охлаждаться, а при сжатии - нагреваться.
Отметим, что для идеального газа этот эффект не наблюда-
ется:
ΔU CVΔT 0 ΔT 0 T const .
39
