
- •Понятие об антигенах
- •Понятие об иммуногенности антигена
- •Иммуногенность
- •Условный образ антигена
- •Понятие об антителах
- •Пространственное расположение гипервариабельных участков внутри вариабельного домена тяжелой цепи иммуноглобулина g человека
- •Компьютерная модель иммноглоблина g
- •Упрощенное двумерное изображение атигенсвязывающго центра антитела
- •Характеристика иммуноглобулинов класса g иммуноглобулины g
- •Характеристика иммуноглобулинов класса а
- •Иммуноглобулины а
- •Механизм секреции иммуноглобулина а на поверхность слизистой оболочки
- •Характеристика иммуноглобулинов класса е
- •Иммуноглобулины е
- •Характеристика иммуноглобулинов класса м
- •Иммуноглобулины м
- •Характеристика иммуноглобулинов класса d
Условный образ антигена

Рис. Условный образ антигена. На рисунке представлены антигенные детерминанты – участки полипептида, характеризующиеся особенностями включения иммунной системы в работу. Отмечены:
разные по специфичности эпитопы для В-лимфоцитов (В-клеточные эпиопы), которые инициируют иммунный ответ только при участии Т-хелперов
участки, называемые "несущей частью" антигена (эпитопы для Т-лимфоцитов)
в процессе презентации антигена в иммуногенной форме в комплексе с молекулами МНС включены участки антигена, называемые агретопами
ряд антигенов, имеющих повторяющиеся однотипные эпитопы и митогенные участки, инициируют иммунный ответ без участия Т-хелперов.
Понятие об антителах
БЕЛКОВЫЕ
МОЛЕКУЛЫ,
которые СТРОГО
СПЕЦИФИЧЕСКИ взаимодействуют с
определенными
антигенами
и
либо
непосредственно
их обезвреживают,
либо
облегчают
последующий фагоцитоз антигенов
фагоцитами,
либо
активируют
систему комплемента по классическому
пути,
в результате чего образуется
мембранноатакующий
комплекс,
вызывающий
повреждение антигена.
АНТИТЕЛА
СТРУКТУРА ИММУНОГЛОБУЛИНА G

ПРИНЦИП ДОМЕННОЙ ОРГАНИЗАЦИИ
МОЛЕКУЛЫ ИММУНОГЛОБУЛИНА

Рис. Принцип доменной организации молекулы иммуноглобулина (на примере иммуноглобулина G). Каждый домен включает приблизительно 100-110 аминокислотных остатков; причем около 60 аминокислотных остатков домена оказываются заключенными в петлю дисульфидной (S-S-связью); около 20 аминокислотных остатков домена, которые не входят в состав петли, служат для соединения с другими доменами. Цифры обозначают последовательность аминокислотных остатков в полипептидных цепях. VL и CL – вариабельный и константный домены легкой цепи. VH – вариабельный домен тяжелой цепи, CH1 CH2 CH3 – константные домены тяжелой цепи.
Пространственное расположение гипервариабельных участков внутри вариабельного домена тяжелой цепи иммуноглобулина g человека

Конформационная особенность вариабельного домена состоит в том, что все 3 гипервариабельных участка в результате формирования третичной структуры полипептидной цепи оказываются в непосредственной близости друг от друга (черные участки рисунка). Каркасные (инвариантные) участки обеспечивают взаимодействие с каркасными участками вариабельного домена легкой цепи. В результате взаимодействия вариабельного домена легкой и тяжелой цепей и формируется антигенсвязывающий центр иммуноглобулина
Компьютерная модель иммноглоблина g
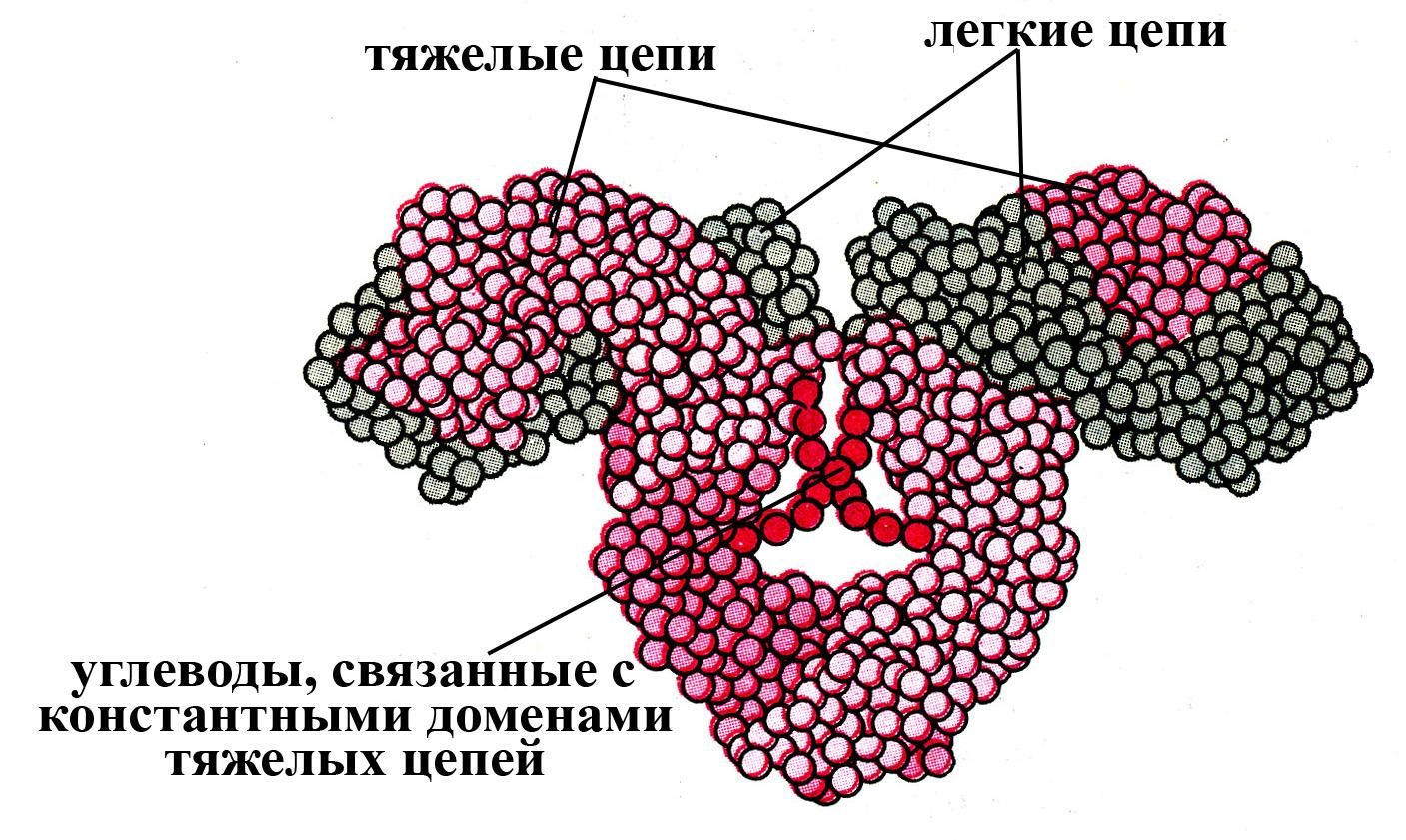
СТРУКТУРА ГЛОБУЛЯРНЫХ ДОМЕНОВ (вариабельного и константного) ЛЕГКОЙ ЦЕПИ (по данным рентгеноструктурного анализа белков Бенс-Джонса)

Одна поверхность каждого домена состоит из 4-х цепей (серые стрелки), образующих антипараллельную -складчатую структуру, стабилизированную межцепочечными водородными связями (между группа СО и NH на протяжении всего пептидного остова). Другая поверхность каждого домена образована тремя цепями (розовые стрелки). Полипептидные цепи, образующие две поверхности домена связаны друг с другом межцепочечной дисульфидной связью (обозначена самой темной полосой). Описанная структура характерна для всех иммуноглобулиновых доменов.
