
- •1 Краткая история развития учения о ферментах
- •2 Общие свойства ферментов и химических катализаторов небелковой природы
- •3 Отличительные признаки ферментативного и химического катализа
- •4 Строение ферментов
- •5 Механизм действия ферментов
- •6 Единицы ферментативной активности
- •7 Специфичность ферментов
- •8 Термолабильность ферментов
- •9 Влияние кислотности среды
- •10 Концентрация фермента
- •11 Концентрация субстрата
- •12 Активаторы и ингибиторы ферментов
- •13 Аллостерические ферменты
- •14 Изоферменты
- •15 Классификация и номенклатура ферментов
- •16 Использование ферментных препаратов
- •17 Иммобилизованные ферменты
- •18 Витамины
- •19 Классификация витаминов
- •20 Жирорастворимые витамины
- •20.1 Витамины группы А
- •20.3 Витамины группы Е
- •20.4 Витамины группы К
- •21 Водорастворимые витамины
- •21.1 Общая характеристика витаминов группы B
- •21.2 Витамин РP (ниацин)
- •21.3 Витамин C
- •21.4 Биотин (витамин H)
- •21.5 Витамин P (Цитрин)
- •21.6 Фолиевая кислота. Витамин Bc птероилглутаминовая кислота
- •21.7 Витамин U
- •22 Витаминоподобные вещества
- •22.1 Парааминобензойная кислота
- •22.2 Витамин В15
- •22.3 Инозит
- •22.4 Холин
- •22.5 Антивитамины
- •Рекомендуемая литература

Биологическая роль
Витамин K принимает участие в механизме свертывания крови. Он необходим для нормального образования в плазме крови белка протромбина, являющегося неактивным предшественником тромбина – фермента, превращающего белок плазмы крови фибриноген в фибрин – нерастворимый волокнистый белок, способствующий формированию сгустка крови. Чтобы протромбин мог активироваться и превратиться в тромбин, он должен связывать ионы Са2+. При недостатке витамина K в организме животных синтезируются дефектные молекулы протромбина, которые не могут связывать ионы Са2+.
Источник
Наиболее богаты витамином K зеленые листья каштана, крапивы, люцерны, овощи – капуста, шпинат, тыква, зеленые томаты, растительное масло, ягоды рябины.
Из животных продуктов он содержится только в печени свиньи. Суточная потребность в витамине K для человека не установлена, так как он синтезируется микрофлорой кишечника.
21 Водорастворимые витамины
21.1Общая характеристика витаминов группы B
Увитаминов группы B много общего. Они чаще всего содержатся в одних и тех же продуктах питания (например, в печени, хлебе из муки грубого помола с
отрубями, пивных дрожжах).
Кроме того, витамины группы B растворимы в воде. Поэтому они быстро вымываются из организма и нуждаются в постоянном накоплении.
Витамины группы B в природе никогда не встречаются в изолированном виде, а только в комплексе. Никогда не бывает так, чтобы, к примеру, однаединственная молекула витамина B6 затесалась в самый дальний уголок салатного листа, а её братьев и сестёр поблизости не оказалось.
33

Таким образом, витамины группы B за миллионы лет привыкли совместно бороться за решение важных задач обмена веществ. Поэтому не имеет смысла покупать в аптеке, например, витамин B3 и пытаться что-то лечить с его помощью. Если нет всех остальных витаминов группы B, то витамин B3 сам по себе не испытывает ни малейшего желания проявить себя. Но когда все соберутся вместе, то в организме начинается подлинная оздоровительная революция. Прежде всего, это благотворно сказывается на мышцах, пищеварительном тракте, коже, волосах, глазах, ротовой полости и печени, а также на состоянии нервной системы.
К сожалению, мы почти все страдаем дефицитом витаминов группы B. Это связано с тем, что любимое место их обитания – ростки и оболочка семян злаковых культур, патока, которые удаляются в процессе очистки продуктов питания и выбрасываются на корм скоту. Так, из полезного неочищенного риса получается пустой полированный рис, а из ценной пшеницы – белая мука, в которой отсутствуют многие необходимые организму вещества.
Следствием этого становятся такие проявления нехватки витаминов, как раннее поседение и выпадение волос, депрессия, повышение содержания холестерина в крови. Витамины группы B активно включаются в обмен веществ в составе кофакторов ферментов. При их отсутствии кофакторы ферментов не образуются, в результате чего приостанавливается или задерживается образование важнейших для организма ферментов и нарушается течение нормального процесса обмена веществ.
21.1.1 Витамин B1 (тиамин; антиневритный)
В его структуре содержатся два кольца – пиримидиновое и тиазоловое, соединённые метиленовой связью:
|
H |
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
CH3 |
|
|
|
|
С |
|
|
|
|
|
|
|
|
|
|
|
|
|
||
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|||
N |
4 |
С |
CH2 |
|
N |
|
|
С |
|
|
|
|||||
|
|
|
|
|
|
|||||||||||
3 |
|
|
5 |
NH2 |
3 |
|
|
4 |
|
|
|
|
||||
С |
|
|
С |
|
|
|
|
|
|
|
|
СН2ОН |
|
|||
|
|
|
|
|
|
|
|
|
|
|
||||||
|
|
HC |
|
|
С |
Cl |
||||||||||
H3C 2 |
N |
6 |
|
2 |
S |
5 |
CH |
|
|
|||||||
|
1 |
|
|
|
|
|
|
|
|
|
2 |
|
|
|
||
|
|
|
|
|
|
|
|
|
1 |
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
Пиримидиновый |
|
|
|
Тиазоловый |
|
|
|
|||||||||
|
цикл |
|
|
|
|
|
|
цикл |
|
|
|
|||||
В тканях животных витамин B1 присутствует в виде кофермента – пирофосфорного эфира – тиаминпирофосфата (ТПФ):
|
|
|
Н |
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
CH3 |
|
|
|
|
|
|
|
|
|
|
|
|
|||||
|
N С |
C |
|
CH |
|
|
|
+ |
|
|
|
- |
|
|
|
|
|
|
|
||||||||||||||
|
|
|
N |
|
С |
|
|
OH |
|||||||||||||||||||||||||
|
|
|
|
|
|
|
|||||||||||||||||||||||||||
|
|
|
|
|
|
|
2 |
|
|
|
|
|
|
|
|
|
|
|
|
|
|
O |
|
|
|||||||||
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
||||||||||||||
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
С |
С |
NH2 |
НС |
|
|
|
С |
|
СН2 |
|
CH2 |
|
O |
|
P |
|
|
O |
|
P |
|
OH |
||||||||||
|
|
|
|
|
|
|
|
|
|
|
|||||||||||||||||||||||
H3C |
|
|
N |
|
|
|
|
|
|
S |
|
|
|
|
|
|
|
|
|
|
|
|
|||||||||||
|
|
|
|
|
|
|
|
|
O |
|
|
O |
|||||||||||||||||||||
|
|
|
|
|
|
|
|
Тиаминпирофосфат |
|
|
|
||||||||||||||||||||||
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|||||||||||||
ТПФ
Витамин B1 устойчив в кислой среде, даже при нагревании. В нейтральной и щелочной разрушается. Этот процесс разрушения витамина имеет место и в неко-
34

торых пищевых технологиях. Например: при использовании щелочных разрыхлителей (соды, карбоната аммония), при выпечке некоторых мучных изделий.
Витамин B1 всасывается в кишечнике, не накапливается в организме, его избыток выводится с мочой. Отсутствие или недостаточное поступление витамина B1 вызывает заболевание полиневрит или бери-бери, признаки которого – нарушение деятельности сердечно-сосудистой, нервной системы, отмечается потеря кожной чувствительности, а так же нарушение пищеварительного тракта.
При биохимических исследованиях у больных отмечается накопление в моче и крови α-кетокислот (α-кетоглутаровой кислоты, пировиноградной) и пентозосахаров.
Биологическая роль
Витамин B1 в форме ТПФ является составной частью ферментов декарбоксилаз, участвующих в реакции декарбоксилирования α-кетокислот – пировиноградной (ПВК) и α-кетоглутаровой, которые образуются в углеводном обмене и при распаде некоторых аминокислот.
|
|
СООН |
|
|
|
|
|
O |
|
|
H3C |
|
С |
|
пируват-декарбоксилаза |
|
|
+ |
|
||
|
|
|
|
H3C |
|
С |
СО2 |
|||
|
|
ТПФ (В1) |
|
|
||||||
|
|
|
|
|
|
|
|
|
||
|
|
O |
|
|
|
|
|
H |
|
|
|
|
ПВК |
|
уксусный альдегид |
||||||
|
|
|
|
|
|
|
|
|
||
При недостатке в пище витамина B1 эти ферменты не образуются, расщепления α-кетокислот не происходит, накапливающаяся в тканях пировиноградная кислота является ядом для нервной системы.
ТПФ в составе фермента транскетолазы осуществляет перенос гликоальдегидного радикала от кетосахаров на альдосахара в пентозофосфатном цикле.
Имеются сведения, что этот витамин участвует в окислительно-восстанови- тельных процессах, а также в биосинтезе аминокислот валина и лейцина.
Источником витамина B1 в основном является растительная пища – оболочечные части и зародыши злаков, бобовые (соя, горох, фасоль), хлеб из муки грубого помола, крупы. В овощах – моркови, картофеле, капусте его немного. Из продуктов животного происхождения богаты витамином B1 печень, почки, мозги, желтки яиц, молоко. Ценным источником витамина B1 являются пивные дрожжи. Рекомендуемая доза витамина B1 колеблется от 1,3–1,9 мг/сутки в зависимости от возраста, пола и характера работы.
21.1.2 Витамин B2 (рибофлавин)
Впервые его выделили из молока. Раствор витамина имеет оранжево-жел- тую окраску. В основе строения витамина лежит гетероциклическое соединение
35

изоаллоксазин (сочетание бензольного, пиразинового и пиримидинового колец), к которому в положении 9 присоединен 5-атомный спирт рибитол.
|
|
|
|
|
|
OH |
|
OH |
OH |
||||||||
|
|
|
H2C |
|
|
|
|
|
|
|
|
|
|
|
CH2 |
|
OH |
|
|
|
|
|
|
CH |
|
|
|
CH |
CH |
|
|||||
|
|
|
|
|
|
|
|
|
|||||||||
H3C |
|
|
N |
|
|
N |
|
|
O |
|
|
|
|
|
|
||
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
H3C |
|
|
N |
|
|
|
|
NH |
|
|
|
|
|
|
|||
|
|
|
|
|
|
|
|
|
|
|
|
||||||
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|||
O
Рибофлавин
Рациональное название его 6,7-диметил-9-D-рибитилизоаллоксазин. Подобно витаминам B1 и PP устойчив в кислой среде, но разрушается в ней-
тральных и щелочных. Активно разрушается на свету под действием УФ-излуче- ния, легко подвергается обратимому восстановлению, присоединяя водород по месту двойных связей и превращаясь в бесцветную лейкоформу.
Признаки недостаточности витамина B2 – воспалительные процессы слизистых оболочек; языка, появляются трещины в уголках губ, кератозы (шелушение кожи), ухудшение зрения, мышечная слабость, быстрая утомляемость, бессонница, неврологические расстройства.
Биологическая роль
Свойство рибофлавина легко окисляться, и восстанавливаться лежит в основе его биологического действия в клеточном метаболизме. Все эти симптомы недостаточности B2 связаны с тем, что не образуются активные формы витамина B2 флавинмононуклиотид (ФМН) и флавинадениндинуклиотид (ФАД).
Эти активные формы витамина B2 являются простетическими группами окислительно-восстановительных – ферментов аэробных дегидрогеназ (флавопротеинов).
|
|
|
O |
O |
|
аденин |
|
CH2 |
(СНОН)3 CH2 O P O |
P O |
H2C |
||
|
O |
|||||
|
|
|
OH |
OH |
|
|
|
|
|
H |
H |
||
H3C |
N |
N |
O |
|
||
|
H |
H |
||||
|
|
|
|
|
|
|
|
|
|
NH |
|
OH OH |
|
H3C |
N |
|
|
|
|
|
|
|
|
|
|
||
O
ФМН
36

Эти ферменты катализируют транспорт электронов и протонов в окисли- тельно-восстановительных реакциях.
|
|
O |
|
|
|
H |
O |
|
H C |
N |
C |
Н |
|
H3C |
N |
C |
Н |
3 |
C |
N |
|
+2Н |
|
|
|
N |
|
|
|
|
|
||||
|
C |
C |
|
-2Н |
|
|
|
C |
H3C |
N |
N |
O |
|
H3C |
N |
N |
O |
|
R |
|
|
|
|
R |
H |
|
ФМН или ФАД ФМНН2 или ФАДН2
За каталитический перенос водорода этими ферментами отвечает изоаллоксазиновая группировка, которая легко может подвергать обратимому гидрированию и дегидрированию.
Протоны и электроны присоединяются по месту двойных связей во 2-ом и 3-ем кольцах.
Ферменты флавопротеины активно участвуют в обмене углеводов, белков, липидов, нуклеиновых кислот. При недостатке B2 происходит нарушение в обмене всех этих веществ, т.к. не образуют активные формы – ФАД или ФМН.
Пример реакции с участием ФАД:
НООС |
|
CH2 |
|
CH2 |
|
СООН + ФАД |
сукцинат- |
НООС |
CH |
|
CH |
|
СООН+ ФАДН2 |
|
|
|
|
|
|
|
|
||||||||
|
|
|
дегидрогеназа |
|
|
|||||||||
янтарная кислота |
фумаровая кислота |
|||||||||||||
|
|
|
|
|
|
|
|
|
||||||
Источники
Те же, что и для витамина B1: хлеб грубого помола, отруби, семена злаков, печень, почки, молоко, пивные дрожжи.
Потребность: 2 – 4 мг в сутки.
21.1.3 Витамин B3 (пантотеновая кислота)
Выделена в 1933 г. из дрожжей и печени. Содержится во всех живых объектах (микроорганизмы, растения, животные), в связи с чем было предложено название «пантотеновая кислота» (от греческого pantoten – повсюду).
Строение:
|
CH3 |
OH |
|
|
|
|
НОСН2 |
C |
СН2 |
СО |
NH CH |
CH |
СООН |
γ |
CHβ |
α |
|
2 |
2 |
|
|
|
|
|
|||
|
3 |
|
|
|
|
|
β -аланин
α ,γ -диокси-β ,β -диметилмасляная кислота
Пантотеновая кислота
Основными компонентами пантотеновой кислоты являются β-аланин и α,γ- диокси-β,β-диметилмасляная кислота.
37
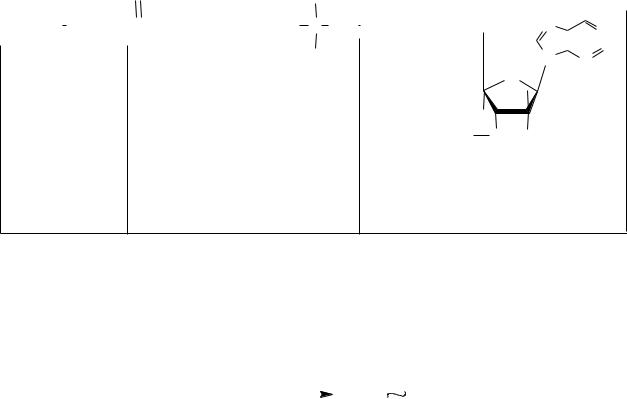
Пантотеновая кислота – вязкая светло-желтая жидкость, легко гидролизуется кислотами и щелочами по месту пептидной связи, легко окисляется.
Этот витамин содержится во всех биологических объектах животного, растительного и микробного происхождения. Обнаружено несколько изомеров пантотеновой кислоты, но биологической активностью обладают только правовращающий оптический изомер.
Основные признаки недостаточности или отсутствия пантотеновой кислоты в организме – дерматиты, поражение слизистых оболочек, изменение желез внутренней секреции, сердца, нервной системы, почек, прекращение роста, снижение аппетита, истощение организма. Это связано с тем, что в отсутствии этого витамина не образуется органическое соединение коэнзим А.
Биологическая роль
Коэнзим А в качестве кофактора входит в состав ферментов биологического ацилирования, участвует в биосинтезе и распаде жирных кислот, жиров, холестерина, стероидных гормонов, гемоглобина.
Во всех реакциях принимает участие HS-группа коэнзима А, потому принято его сокращенное обозначение в виде HS-KoA. В основе его структуры лежит остаток 3’-фосфоаденозин-5’-дифосфата, соединенный с остатком пантотеновой кислоты, карбонильная группа которой в свою очередь связана с остатком β-мер- каптоэтиламина (тиоэтиламина).
|
|
|
|
|
|
O |
|
|
|
|
O |
|
|
OH |
CH3 |
|
|
O |
|
|
O |
|
|
|
|
|
NH |
|||||||||||||||||
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
||||||
HS |
|
СН2 СН2 |
|
NH |
|
C |
|
СН2 |
|
СН2 |
|
NH |
|
|
|
|
|
|
|
C CH2 O |
|
|
|
|
O |
|
|
|
|
5/ |
|
N |
|
|
|
2 |
||||||||
|
|
|
|
|
|
|
|
C |
|
|
CH |
|
|
P |
|
|
|
P |
|
O |
|
|
CH2 |
|
|
|
|
|
N |
|||||||||||||||
|
|
|
|
|
|
|
|
|
|
|
|
|
||||||||||||||||||||||||||||||||
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
||||||||||||||||||||||||
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
||||||||||||||||||||||
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
CH3 |
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
OH |
|
OH |
|
O |
|
N |
|
N |
|||||||||||||||
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
3/ |
|
|
|
|
|
|
|
|
||||||||
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
||||||||||
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
H |
|
H |
|
|
|
|
||||
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
Н2О3Р O |
OH |
|
|
|
|
|||||||||||||
тиоэтиламин пантотеновая кислота |
3/-фосфоаденозин-5/-дифосфат |
HS-КоА (Коэнзим А)
Кофермент А активирует слабореакционные карбоновые кислоты. Реакция активации жирных кислот катализируется ферментом ацил-КоА
синтетазой.
|
|
|
|
|
|
|
|
|
O |
|
|
|
||
R |
|
СООН + |
HS |
|
КоА + АТФ |
ацил-КоА- |
|
|
|
|
|
|
|
КоА +АМФ + Н4Р2О7 |
|
|
R |
|
С |
S |
|
||||||||
|
|
синтетазы |
|
|
||||||||||
В результате реакции образуется ацил-КоА, являющийся активной формой жирной кислоты (содержащий высокоэнергетическую тиоэфирную связь).
38

HS-KоA участвует в распаде углеводов, в составе мультиферментного комплекса в реакциях окислительного декарбоксилирования α-кетокислот – пировиноградной, α-кетоглутаровой.
Образовавшийся ацетил КоА является узловым соединением, на котором происходит перекрещивание путей обмена жиров, углеводов и липидов.
CH |
|
|
|
|
CH3 |
|||||
|
3 |
O + HS |
|
КоА + НАД+ |
|
пируват- |
|
|
S КоА + НАДН + Н++ СО2 |
|
|
|
|
|
|
||||||
|
|
|
|
|
|
|
||||
C |
|
|
|
|
С |
|||||
|
|
дегидрогеназный |
||||||||
|
||||||||||
|
|
|
|
|
||||||
|
|
|
|
|
|
|||||
|
|
|
|
|
|
|
комплекс |
|
|
|
СООН |
|
|
|
O |
||||||
ПВК |
|
|
|
|
ацетил КоА |
|||||
Основные источники: дрожжи, печень, яичный желток, зеленые части растений и микрофлора кишечника.
Суточная потребность 10 – 12 мг.
21.1.4 Витамин B6
Витамин B6 (пиридоксин, антидерматитный) открыт в 1904 г. В отличие от известных к тому времени водорастворимых витаминов B1, B2 и РР он устранял особую форму дерматита конечностей у крыс, названого акроденией.
Выделен из дрожжей и печени. Установлено, что B6 витаминной активностью обладают три производных 3-оксипиридина: пиридоксин (пиридоксол), пиридоксаль и пиридоксамин, которые отличаются друг от друга природой замещающей группы в положении 4-пиридинового ядра.
|
|
OH |
O |
|
H |
|
|
|
|
NH2 |
||||||
|
|
H2C |
|
|
|
C |
|
|
H2C |
|||||||
HO |
|
HO |
|
|
HO |
|||||||||||
|
|
CH2 |
|
|
CH2 |
|
|
|
|
|
CH2 |
|||||
|
|
|
|
|||||||||||||
|
|
|
OH |
|
|
|
|
|
OH |
|
|
|
|
|
|
OH |
|
|
|
|
|
|
|
|
|
|
|
||||||
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
H3C |
|
N |
H3C |
N |
H3C |
|
|
N |
||||||||
Пиридоксол |
Пиридоксаль |
Пиридоксамин |
||||||||||||||
Все эти соединения могут переходить друг в друга. Их водные растворы устойчивы к действию кислот и щелочей, но разрушаются в нейтральных растворах под действием света.
Основные признаки недостаточности В3 – пеллагроподобные дерматиты, не поддающиеся лечению никотиновой кислотой; нарушения в процессе кроветворения. При биохимических исследованиях крови и мочи отмечались нарушения в азотном обмене. Последние исследования показали, что недостаток B6 ведет к нарушению липидного обмена и развитию атеросклероза.
Биологическая роль
Оказалось, что, хотя все три производные 3-оксипиридина наделены витаминными свойствами, однако кофакторные функции выполняют только фосфорные эфиры пиридоксаля и пиридоксамина.
39

Известно более 20 пиридоксалевых ферментов, катализирующих ключевые реакции азотистого обмена во всех живых организмах.
Эти кофакторы входят в состав ферментов аминотрансфераз в качестве простетической группы и катализируют реакцию переаминирования – обратимый перенос аминогруппы (NH3 – группы) от аминокислот на α-кетокислоту.
O |
|
|
H |
H2C |
NH2 |
|
|
|
OH |
||||||||||||||||
|
|
|
|
|
|
|
|||||||||||||||||||
HO |
|
|
|
|
|
|
|
|
OH |
HO |
|
CH2 |
|
O |
|
P |
|
O |
|||||||
|
|
|
|
|
|
|
|
|
|
|
|
||||||||||||||
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|||||||
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
||||
|
|
|
|
CH2 |
|
O |
|
P |
|
O |
|
|
|
|
|
|
|
|
|
|
|
|
|||
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|||||||
|
|
|
|
|
|
|
|
|
|
|
|
|
H3C N |
|
|
|
|
|
OH |
||||||
|
|
|
|
|
|
|
|
|
|
OH |
|
|
|
|
|
|
|
|
|
||||||
H3C |
N |
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
||||||
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
||||
Пиридоксальфосфат Пиридоксаминфосфат
Например, реакция переаминирования между аланином и α-кетоглуторатом выглядит следующим образом:
|
|
|
|
|
|
|
|
СООН |
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
СООН |
|||||||||||
|
|
|
CH3 |
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
CH3 |
|
|
|
|
|
|
|
|
|
|
|
|
||||
|
|
|
+ |
|
CH2 |
|
|
|
|
|
|
В6 |
|
|
|
|
|
|
|
|
|
+ |
CH2 |
|
|
|||||||||||||||||
|
HC |
|
|
|
NH2 |
|
CH2 |
|
|
|
|
|
|
|
|
|
|
|
|
|
C |
|
O |
|
|
CH2 |
|
|
||||||||||||||
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|||||||||||||||||||
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|||||||||||||||||||||
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|||||||||||||||||||||||
|
|
|
|
|
|
|
аминотрансфераза |
|
|
|
|
|
|
|
||||||||||||||||||||||||||||
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|||||||||||||||||
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
||
|
|
|
СООН |
|
C O |
|
|
|
|
|
|
|
|
|
|
|
|
|
|
СООН |
|
|
HC |
NH2 |
||||||||||||||||||
|
аланин |
|
|
|
|
|
|
|
|
|
|
|
|
|
|
пировиноградная |
|
|
|
|
|
|
|
|
||||||||||||||||||
|
|
СООН |
|
|
|
|
|
|
|
|
|
|
|
кислота |
|
|
|
|
|
СООН |
||||||||||||||||||||||
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|||||||||||||||||||
|
|
|
|
|
|
|
α -кетоглутаровая |
|
|
|
|
|
|
|
|
|
|
|
|
|
|
глутаминовая |
||||||||||||||||||||
|
|
|
|
|
|
|
|
|
кислота |
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
кислота |
|||||||||||||
1) |
|
|
CH3 |
|
|
|
|
O |
|
|
|
|
|
|
|
|
|
|
CH3 |
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
||||||||
|
HC |
|
|
NH2 |
+ |
Е |
|
|
C |
|
|
Н |
|
|
|
C |
|
O + |
Е |
|
|
CH2 |
|
|
NH2 |
|||||||||||||||||
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|||||||||||||||||||||||||||||
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|||||||||||||||||||||||||||
|
|
|
|
|
|
|
пиридоксаль |
|
|
|
|
|
|
|
|
|
|
|
|
пиридоксамин |
||||||||||||||||||||||
|
|
СООН |
|
|
фосфат |
|
|
|
СООН |
|
|
|
||||||||||||||||||||||||||||||
|
|
|
|
|
|
|
|
|
|
|
|
фосфат |
||||||||||||||||||||||||||||||
аланин |
|
|
|
(акцептор |
пировиноградная |
|
|
|||||||||||||||||||||||||||||||||||
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
||||||||||||||||||||||||||||
|
|
аминогруппы) |
|
|
|
|
|
|
|
|
|
|
|
|
||||||||||||||||||||||||||||
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
кислота |
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
||||||
2) |
СООН |
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
СООН |
|
|
|
|
|
|
|
|
O |
|
|
||||||||||||||
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
||||||||||||
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|||||
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
CH2 |
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
||||||
|
CH2 |
+ |
Е |
|
|
CH2 |
|
|
|
NH2 |
|
|
|
|
|
+ |
|
Е |
|
|
|
C |
|
|
|
Н |
||||||||||||||||
|
|
|
|
|
|
|
|
|
|
|
|
|
|
CH2 |
|
|
|
|
|
|
||||||||||||||||||||||
|
|
|
|
|
|
(донор |
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|||||||||||||||||
|
CH2 |
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|||||||||||||||||||
|
|
|
|
|
|
|
аминогруппы) |
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|||||||||||
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
HC |
NH2 |
|
|
|
|
|
|
|
|
|
|
|
|
||||||||||
|
C |
O |
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|||||||||||||
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|||||||||||||
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
СООН |
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
||||
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|||||
|
СООН |
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
||||||||||
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
||||||
α -кетоглутаровая кислотата |
|
|
|
глутаминовая кислота |
|
|
|
|
|
|
|
|
|
|
||||||||||||||||||||||||||||
40

Реакции переаминирования служат для образования новых аминокислот. ПФ в составе декарбоксилаз аминокислот катализирует реакции отщепления СО2 от карбоксильной группы с образованием биогенных аминов.
Например:
NH2 CH |
CH2 CH |
CH2 CH COOH декарбоксилазаNH |
|
CH |
CH |
|
NH |
|||||||
2 |
|
2 |
|
|
|
В6 |
2 |
CH |
2 |
CH |
2 |
CH |
2 |
|
|
|
|
|
|||||||||||
|
|
|
|
|
|
|
|
|
2 |
|
2 |
|
2 |
|
|
лизин |
|
|
|
NH2 |
|
|
|
кадаверин |
|
|
|||
|
|
|
|
|
|
|
|
|
|
|||||
CH2 |
CH2 |
|
|
CH3 |
декарбоксилаза |
|
|
|
|
|
|
|
||
NH2 |
|
CH2 |
|
|
CH |
|
|
CH2 CH CH2 |
CH NH2 |
|||||
|
|
|
В6 |
NН |
||||||||||
|
|
|
||||||||||||
|
|
|
|
|
|
|
|
2 |
|
|
2 |
|
2 |
|
арнитин |
|
|
NH2 |
|
|
|
путресцин |
|
|
|||||
|
|
|
|
|
|
|
|
|
||||||
Декарбоксилирование аминокислот лизина и арнитина приводит к образованию токсичных диаминов (трупных ядов – кадаверина и путресцина).
В организме человека витамин В6 участвует в биосинтезе витамина РР из аминокислоты триптофан.
Источники: хлеб, злаки, бобовые, мясо, печень, почки, икра, желток. Витамин В6 частично синтезируется микрофлорой кишечника.
Суточная норма 2 – 3 мг.
21.1.5 Витамин B12
Витамин В12 (кобаламин; антианемический витамин) выделен из печени в кристаллическом виде в 1948 г. Регулирует процесс кроветворения и оказывает лечебный эффект при пернициозной (злокачественной) анемии у людей.
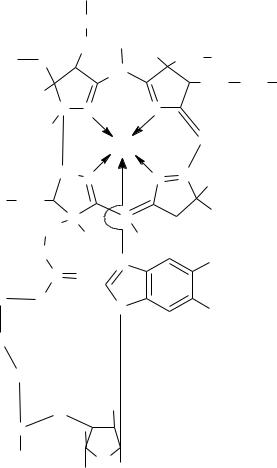
В 1955 г. Д. Ходжкин расшифровала его структуру, определила пространственную конфигурацию, главным образом при помощи физических методов исследования (рентгеноструктурный анализ), за это получила Нобелевскую премию. На основании этих данных, а также результатов изучения химического состава для витамина В12 было предложено следующее строение:
41
|
H2NOC |
|
|
|
|
|
|
H2C |
|
|
|
|
|
|
H C H3C |
|
|
|
||
H NOC |
CH |
2 |
|
H3C |
CH2 |
CONH2 |
|
|
|||||
2 |
2 |
|
HC |
|
|
|
|
|
A |
B |
|
CH2 CH2 CONH2 |
|
|
H3C |
|
|
|||
|
N |
|
N |
|
|
|
|
C |
+ |
|
|
||
|
H3C |
|
|
CH |
||
|
|
|
Со |
|||
|
|
|
|
|
||
|
CH N |
|
N |
C |
CH3 |
|
H2NOC |
CH2 C |
C |
D |
CH3 |
||
|
CH |
C |
|
|
||
|
CH3 |
CH |
|
|
||
|
2 |
|
|
|||
|
H2C |
|
|
3 |
|
CH3 |
|
|
N |
|
|
||
|
C |
O |
|
|
||
|
|
|
|
|
||
H2C |
NH |
|
N |
|
|
CH3 |
|
|
|
|
|
||
CH
H3C
O
OHO
O P
P
O- HOH2C O H
Это единственный витамин, который содержит металл кобальт.
В молекуле витамина В12 центральный атом Со соединен атомами азота 4-х пиррольных колец, образуя порфириноподобное корриновое ядро. В корриновом кольце В12 имеется менее обширная система сопряженных связей, чем в порфиринах. И как результат, большое число хиральных центров, расположенных по переферии колец, несколько выходящих из плоскости объединенного цикла. В составе имеются остатки фосфорной кислоты, рибозы, аденина, аминогрупп, и эта структура называется «кобаламин».
При недостатке витамина В12 развивается злокачественная анемия (нарушение процесса кроветворения), отмечается нарушение деятельности нервной системы, снижается кислотность желудочного сока.
Биологическая роль
Различают две кофакторные формы витамина В12:
1)метилкобаламин, содержится в цитоплазме;
2)дезоксиаденозилкобаламин, содержится в митохондриях.
Ферменты, содержащие метилкобаламин катализируют реакции трансметилирования, в которых метилкобаламин выполняет роль промежуточного переносчика метильной группы; реакции синтеза метианина, ацетата, нуклиотидов и нуклеиновых кислот, т.е. катализируют реакции белкового, углеводного, липидного и нуклеинового обмена.
42
