
- •1 Краткая история развития учения о ферментах
- •2 Общие свойства ферментов и химических катализаторов небелковой природы
- •3 Отличительные признаки ферментативного и химического катализа
- •4 Строение ферментов
- •5 Механизм действия ферментов
- •6 Единицы ферментативной активности
- •7 Специфичность ферментов
- •8 Термолабильность ферментов
- •9 Влияние кислотности среды
- •10 Концентрация фермента
- •11 Концентрация субстрата
- •12 Активаторы и ингибиторы ферментов
- •13 Аллостерические ферменты
- •14 Изоферменты
- •15 Классификация и номенклатура ферментов
- •16 Использование ферментных препаратов
- •17 Иммобилизованные ферменты
- •18 Витамины
- •19 Классификация витаминов
- •20 Жирорастворимые витамины
- •20.1 Витамины группы А
- •20.3 Витамины группы Е
- •20.4 Витамины группы К
- •21 Водорастворимые витамины
- •21.1 Общая характеристика витаминов группы B
- •21.2 Витамин РP (ниацин)
- •21.3 Витамин C
- •21.4 Биотин (витамин H)
- •21.5 Витамин P (Цитрин)
- •21.6 Фолиевая кислота. Витамин Bc птероилглутаминовая кислота
- •21.7 Витамин U
- •22 Витаминоподобные вещества
- •22.1 Парааминобензойная кислота
- •22.2 Витамин В15
- •22.3 Инозит
- •22.4 Холин
- •22.5 Антивитамины
- •Рекомендуемая литература
 O C R
O C R
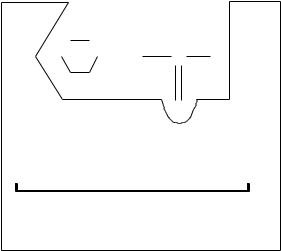
Связывающий O
центр Каталитический центр
Активный центр
Рисунок 1 – Строение активного центра фермента
Структура активного центра комплементарна структуре его субстрата. Поэтому данный фермент из множества веществ находящихся в клетке, присоединяет только свой субстрат. У ферментов, имеющих четвертичную структуру, число активных центров может быть равно числу субъединиц.
5 Механизм действия ферментов
Хотя детальный механизм действия каждого фермента уникален, все ферменты «работают» сходным образом.
Процесс ферментативного катализа можно условно подразделить на три стадии.
1. Стерическое связывание субстрата S с активным центром фермента E (с образованием промежуточного фермент-субстратного комплекса ES). При этом субстраты ориентируются таким образом, что приобретают оптимальное положение для образования переходного состояния ES. Сближение и необходимая ориентации реагентов значительно повышают вероятность образования продуктивного комплекса ES*. Высокая избирательность действия фермента обеспечивается тем, что субстрат связывается в активном центре фермента в нескольких точках и это исключает ошибки. Кроме того, связывание субстрата в активном центре приводит к удалению гидратной оболочки субстрата. В результате удаления молекул воды в активном центре фермента во время катализа создаются совершенно другие условия, чем в растворе. Таким образом, переходное состояние в случае ферментативной реакции требует меньшей энергии активации:
S + E ↔ SE ↔ SE* ↔ P + E
2. Вторая стадия является, собственно, актом катализа, в ходе которого происходят конформационные изменения молекул фермента и субстрата. Эти изменения могут способствовать «растягиванию» разрываемой связи или, наоборот, сближению молекул при реакциях синтеза, в результате чего образуется активный продуктивный комплекс SE*, который и обусловливает снижение энергии активации ферментативной реакции.
7
Многие ферменты во время катализа переносят специфические группировки с субстрата или на субстрат. Особенно часто осуществляется перенос протонов. Этот ферментативный кислотно-основной катализ значительно более эффективен, чем обмен протонов с кислотами и основаниями в растворе. Часто химические группировки ковалентно присоединяются к остаткам фермента. Это – ковалентный катализ.
3. Третья стадия – отделение конечного продукта реакции Р и фермента. Ферменты – высокоэффективные катализаторы. Они повышают скорость катализируемой реакции в 1012 раз и более.
6 Единицы ферментативной активности
Ферменты в клетках находятся в ничтожно малых концентрациях. Поэтому определяют не концентрацию фермента, а его активность. Об активности фермента судят по скорости убыли субстрата или скорости образования продуктов реакции.
За единицу активности фермента (Е) принято такое его количество, которое катализирует превращение 1 микромоля вещества за одну минуту при оптимальных условиях pH и температуры.
Часто определяют удельную активность фермента: она равна числу единиц фермента в образце, делённому на массу белка (в мг) в этом образце.
Молярная активность (число оборотов) определяется как число молекул субстрата, которое превращается молекулой фермента за 1 минуту. В системе СИ за единицу активности фермента принят катал (кат) – это такое количество фермента, которое катализирует превращение одного моля субстрата за 1 секунду.
7 Специфичность ферментов
Ферменты обладают высокой специфичностью действия. Т.е. избирательно действовать на субстрат и определять путь его превращения. Это свойство существенно отличает их от неорганических катализаторов. Так, мелкоизмельчённые платина и палладий могут катализировать восстановление (с участием молекулярного водорода) десятки тысяч химических соединений различной структуры. Высокая специфичность ферментов обусловлена конформационной и электростатической комплементарностью между молекулами субстрата и фермента и уникальной структурной организацией активного центра, обеспечивающими «узнавание» высокое сродство и избирательность протекания одной какой-либо реакции из тысяч других химических реакций, протекающих одновременно в живых клетках.
В зависимости от механизма действия различают ферменты с относительной (или групповой) и абсолютной специфичностью. Так, для действия ферментов с групповой специфичностью наибольшее значение имеет тип химической связи в молекуле субстрата. Например, пепсин в одинаковой степени расщепляет белки животного и растительного происхождения, несмотря на то, что эти белки существенно отличаются друг от друга как по химическому строению и аминокислотному составу, так и по физико-химическим свойствам. Однако пепсин не
8

расщепляет ни углеводы, ни жиры. Объясняется это тем, что точкой приложения, местом действия пепсина является пептидная связь:
O
║
─C─N─.
|
H
Для действия липазы, катализирующей гидролиз жиров на глицерин и жирные кислоты, подобным местом является сложноэфирная связь. Относительной специфичностью наделены некоторые внутриклеточные ферменты, например, гексокиназа, катализирующая при участии АТФ фосфорилирование почти всех гексоз, хотя одновременно в клетках имеются и специфические для каждой гексозы ферменты, выполняющие такое же фосфорилирование.
При абсолютной специфичности фермент катализирует превращение только единственного субстрата. Любые изменения в структуре субстрата делают его недоступным для действия этого фермента. Имеются экспериментальные доказательства существования так называемой стереохимической специфичности, обусловленной существованием оптически изомерных L- и D- форм или геометрических (цис- и транс-) изомеров химических веществ. Так, известны оксидазы L- и D- аминокислот, хотя в природных белках обнаружены только L-аминокислоты. Каждый из видов оксидаз действует только на свой специфический стереоизомер:
L-аминокислота |
|
+½O2 |
α – кетокислота + NH3 + H2O |
||
|
|
|
|
||
|
|
||||
Оксидаза L-аминокислот |
|
||||
D-аминокислота |
+½O2 |
α-кетокислота + NH3 + H2O |
|||
|
|
||||
|
|||||
Оксидаза D-аминокислот |
|
||||
Наглядным примером стереохимической специфичности является бактериальная аспартатдекарбоксилаза, катализирующая отщепление CО только от L-ала- нин. Если какое-либо соединение существует в форме цис- и транс-изомеров с различным расположением групп атомов вокруг двойной связи, то, как правило, только один из этих изомеров может служить в качестве субстрата для действия фермента. Например, фумараза катализирует превращение только фумаровой кислоты (транс-изомер), но не действует на малеиновую кислоту (цис-изомер):
9
HOOC |
HC |
|
COOH |
HC |
|
|
COOH |
|||||
|
|
|
||||||||||
|
||||||||||||
|
|
|
|
|
|
|
|
|
|
|
|
|
CH |
HC |
|
|
COOH |
||||||||
|
|
|
||||||||||
|
|
|||||||||||
Фумаровая кислота |
Малеиновая кислота |
|||||||||||
Специфичность действия ферментов пытался объяснить Э. Фишер. Согласно его гипотезе «фермент подходит к субстрату как ключ к замку», при этом топография активного центра не только высоко упорядочена, но и жёстко закреплена. Активный центр фермента соответствует топографии одногоединственного субстрата, поэтому он может подвергаться действию активного центра. Гипотеза «ключа и замка» вполне удовлетворительно объясняет абсолютную специфичность, однако объяснить групповую специфичность по этой гипотезе затруднительно.
Теория индуцированного соответствия (теория Кошланда) устраняет это противоречие. Суть теории в том, что пространственное соответствие структуры субстрата и активного центра фермента создаётся в момент их взаимодействия друг с другом. В зависимости от конформационной подвижности активного центра фермент способен взаимодействовать либо с немногими, либо с самыми разными субстратами. Фермент и субстрат в процессе образования фермент-суб- стратного комплекса как бы подстраиваются друг к другу (как перчатка к руке).
Теория химического соответствия, сохраняя основные положения теории Кошланда, фиксирует внимание на том, что специфичность действия ферментов объясняется узнаванием ферментом той части субстрата, которая при катализе не изменяется. Между этой частью субстрата и субстратным центром возникают взаимодействия и только тогда, когда совпадение это достаточно полно, может образоваться фермент-субстратный комплекс и начаться процесс катализа.
8 Термолабильность ферментов
Скорость химических реакций зависит от температуры, поэтому катализируемые ферментами реакции также чувствительны к изменениям температуры. Установлено, что скорость большинства химических реакций повышается в двачетыре раза при повышении температуры на 10°С и, наоборот, снижается в два раза при понижении температуры на 10°С. Этот показатель получил название температурного коэффициента Q10. Однако вследствие белковой природы фермента тепловая денатурация при повышении температуры будет снижать эффективную концентрацию фермента с соответствующим снижением скорости реакции. Так, при температуре, не превышающей 45–50°С, скорость реакции увеличивается согласно теории химической кинетики. При температуре выше 50°С на скорость реакции большое влияние начинает оказывать тепловая денатурация белкафермента, приводящая к полному прекращению ферментативного процесса.
10
