
- •1 Классификация липидов и природных жиров
- •1.1 Жиры
- •1.2 Воски
- •1.3 Стериды
- •1.4 Глицерофосфолипиды
- •1.5 Гликолипиды
- •1.6 Сфингофосфолипиды
- •2 Биологическая роль липидов
- •3 Жирные кислоты
- •4 Номенклатура
- •5 Изомерия
- •6 Обмен липидов
- •6.1 Определение содержания сырого жира в аппарате Сокслета
- •6.2 Определение общих липидов по цветной реакции с сульфофосфованилиновым реактивом
- •6.3 Качественное определение ненасыщенности жиров пробой с раствором брома
- •7 Прогоркание жиров
- •7.1 Гидролитическое прогоркание жиров
- •7.3 Кинетика действия липазы
- •7.4 Гидролитическое расщепление жира под действием липазы
- •7.5 Определение числа омыления
- •7.6 Определение кислотного числа
- •7.7 Определение эфирного числа
- •7.8 Окислительное прогоркание жиров
- •7.9 Определение активности липоксигеназы
- •7.10 Определение йодного числа жиров
- •7.11 Определение перекисного числа
- •7.12 Анализ карбонильных соединений
- •8 Фосфолипиды
- •8.1 Выделение лецитинов из яичного желтка
- •8.2 Гидролиз лецитина и определение продуктов гидролиза

|
|
|
|
|
|
|
|
O |
|
|
|
|
|
|
|
|
|
|
|
||||
|
CH2 |
|
O |
|
|
|
|
|
|
|
|
С17Н35 |
|
|
|
||||||||
|
|
|
|
|
C |
|
|
|
|||||||||||||||
|
|
|
|
|
|
|
|
||||||||||||||||
|
|
|
|
|
|
|
O |
|
|
|
|
|
|
|
|
|
Остаток элаидиновой кислоты |
||||||
|
|
|
|
|
|
|
|
|
|
|
|
|
( |
|
|
)7 |
|
|
|
|
|
||
HC |
|
O |
|
|
C |
|
CH2 |
|
C |
|
|
H |
(транс-изомер) |
||||||||||
|
|
|
|
|
|
|
|||||||||||||||||
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|||||
|
CH2 |
|
|
|
|
|
|
|
|
O |
|
|
|
H |
|
C |
|
|
(СН2)7 |
CH3 |
|||
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|||||||||
|
|
O |
|
|
|
|
|
|
|
|
|
С17Н35 |
|
|
|
||||||||
|
|
|
|
|
|
C |
|
|
|
|
|
||||||||||||
|
|
|
|
|
|
|
|
|
|
|
|||||||||||||
Транс-1,3-дистеаро-2-элаидин
Число геометрических изомеров в глицеридах растет с увеличением количества двойных связей в радикалах кислотных остатков.
В глицеридах природных жиров непредельные жирные кислоты находятся, как правило, в цис-конфигурации.
6 Обмен липидов
6.1Определение содержания сырого жира в аппарате Сокслета
Большинство методов количественного определения жира основаны на его способности растворяться в органических растворителях (диэтиловом, петролейном эфирах, хлороформе, четыреххлористом углероде и др.) При обработке сырья (животного, растительного) органическими растворителями в раствор переходят не только жиры, но и жироподобные вещества: свободные жирные кислоты, воска, стерины, пигменты и вещества, относящиеся к другим классам органических соединений – альдегиды, кетоны и др. Поэтому получаемый продукт называют «сырым жиром». Экстракция сырого жира проводится в аппарате Сокслета (рис 5).
Аппарат Сокслета состоит из трех частей, пришлифованных друг к другу: холодильника 1, экстрактора 2 и приемной колбы 3, эфир 4.
Техника определения. Навеску продукта (муки, семян) в количестве 2- 10 г (в зависимости от предполагаемого содержания масла) переносят в сухую фарфоровую ступку и растирают с безводным сернокислым натрием до однородной массы. Соли берут в 3 раза больше чем навеска.
Растертую массу переносят в пакетик из фильтровальной бумаги, высушенный до постоянной массы. Пакетик заворачивают, как порошок в аптеке. Взвешивают на аналитических весах и переносят в экстрактор аппарата Сокслета.
В приемную колбу наливают эфир на 1/3 емкости и соединяют ее с экстрактором. Эфир наливают в экстрактор так, чтобы его уровень покрыл пакетики. Затем с помощью шлифа соединяют его с холодильником, и аппарат ставят в холодную водяную баню. Пакетики с материалом настаивают 3-4 часа, после этого включают нагрев. Пары эфира из приемной колбы по широкой трубке поступают в холодильник, конденсируются и стекают в экстрактор, извлекая жир
22
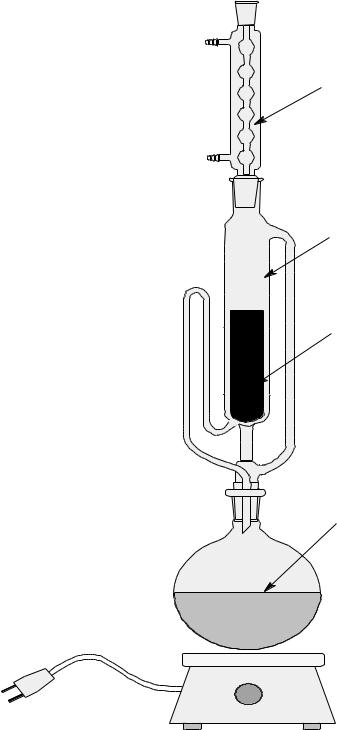
из материала. Как только уровень эфира достигает верхнего края сифонной трубки, он сразу начнет переливаться в приемную колбу. Процесс экстракции продолжается непрерывно.
1
2
3
4
5 |
6 |
7 |
4 |
|
38
2 |
9 |
1 |
1 1 |
Рисунок 5 – Прибор для определения жира по методу Сокслета
Экстракцию жира ведут 5-6 часов. После чего пакетики с обезжиренным материалом вынимают из экстрактора, подсушивают на стекле в вытяжном шкафу, чтобы испарился эфир и высушивают во взвешенных бюксах при температуре 100-1050С до постоянной массы. Содержание жира (в процентах на су-
23
хое вещество) рассчитывают, зная массу пакетика до и после экстракции, а также массу пустого пакетика. Берут среднее из 3-4 определений.
Х = m1 − m2 × 100 , m3
где m1 – масса пакетика с навеской и с безводным сернокислым натрием до экстрагирования, г; m2 – масса пакетика с навеской и с безводным сернокислым натрием после экстрагирования, г; m3 – масса навески после сушки, г.
Материалы, реактивы и оборудование. Мука или семена льна, подсолнуха, орехи, др. продукты; диэтиловый (петролейный) эфир (безводный), безводный сернокислый натрий, прокаленный в муфельной печи в течении 3-4 суток; фильтровальная бумага; аппарат Сокслета; водяная баня; бюксы.
Подготовка эфира к экстракции. В склянку с эфиром прибавляют прокаленный хлористый калий или окись кальция. Сосуд укупоривают корковой пробкой, в которую вставляют трубку с прокаленным хлористым кальцием. Через 1-2 суток эфир сливают и повторяют операцию. Через 6-8 часов эфир сливают в сосуд. Эфир должен быть свободным от перекисей.
6.2 Определение общих липидов по цветной реакции с сульфофосфованилиновым реактивом
Продукты распада ненасыщенных липидов, полученные в результате гидролиза липидов серной кислотой, образуют с реактивом, состоящим из фосфорной кислоты и ванилина, стабилизированный и окрашенный в красный цвет, комплекс. Интенсивность окраски комплекса пропорциональна содержанию общих липидов.
OH
O CH3
C
O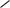
 H
H
Ванилин
Техника определения. К 0,05 см3 опытного раствора (экстракт липидов) прибавляют 2,5 см3 концентрированной серной кислоты. Содержимое пробирок тщательно перемешивают и помешают на 10 минут в кипящую водяную баню. Контрольную колбу ставят как опытную, но вместо экстракта липидов берут 0,05 см3 воды. Пробирки вынимают и охлаждают водой до температуры 18-25 0С. Из каждой пробирки отбирают по 0,2 см3 смеси и переносят в пробирку с 3 см3 фосфорнованилиновой смеси. После перемешивания пробы оставляют на 45 минут в темноте. Измеряют поглощение на ФЭК при 500-560 нм (зеленый светофильтр). Для построения калибровочного графика из основного раствора (стандартного) готовят рабочие стандарты, как указано в таблице 2.
24

Таблица 2 – Данные к построению калибровочного графика определения липидов
№ пробы |
Основной стандартный |
Хлороформ, см3 |
Концентрация ли- |
|
||||
|
раствор ванилина, см3 |
|
|
|
пидов, мг/ см3 |
|
||
1 |
0,17 |
|
|
0,83 |
|
2 |
|
|
2 |
0,33 |
|
|
0,67 |
|
4 |
|
|
3 |
0,50 |
|
|
0,50 |
|
6 |
|
|
4 |
0,67 |
|
|
0,33 |
|
8 |
|
|
5 |
0,83 |
|
|
0,17 |
|
10 |
|
|
6 |
1,00 |
|
|
- |
|
12 |
|
|
Из каждого разведения берут по 0,05 см3, обрабатывают как опытные про- |
||||||||
бы. |
|
|
|
|
|
|
|
|
Концентрацию липидов определяют по формуле |
|
|
|
|||||
|
СОП = |
|
АОП |
|
, |
|
|
|
|
|
А × С |
|
|
|
|
||
|
|
|
СТ |
СТ |
|
|
|
|
где Соп – концентрация липидов в опытной пробе; |
Аоп |
– поглощение |
||||||
опытного образца раствора; Аст – поглощение стандартного |
раствора; Сст – |
|||||||
концентрация основного раствора стандартного. |
|
|
|
|||||
Материалы, реактивы и оборудование. Серная кислота (концентрированная), ортофосфорная кислота (концентрированная), 0,6 %-й: раствор ванилина; фосфорнованилиновая смесь – 4 части концентрированной ортофосфорной кислоты смешивают с 1 частью 0,6 %-го раствора ванилина; хлороформ; стандартный раствор триолеина (12 мг/см3) в хлороформе; пробирки, пипетки на 0,1 см3 и на 1 см3, бюретки на 50 см3, водяная баня, фотоэлектроколориметр (ФЭК).
6.3 Качественное определение ненасыщенности жиров пробой с раствором брома
а) В пробирку помещают 15 капель 1 %-го раствора подсолнечного масла в четыреххлористом углероде и добавляют 1 мл бромной воды. Взбалтывают. Наблюдают и отмечают обесцвечивание раствора брома.
Объяснить опыт и написать реакцию на примере 1,2-диолео-3-линолеина. б) В 3 пробирки вносят по 1 см3 1 %-х растворов подсолнечного масла,
маргарина и коровьего масла в четыреххлористом углероде.
В каждую из пробирок приливают по каплям из бюретки 2 %-й раствор брома в том же растворителе до прекращения обесцвечивания растворов и установления устойчивой лимонно-желтой окраски раствора брома.
Отмечают по бюретке количество раствора брома, затраченное на каждый из образцов жира до приобретения указанной окраски, и располагают их в ряд по возрастающей степени ненасыщенности.
Написать реакцию на примере следующих глицеролов: 1,2-дистеаро-3-олеина; 1,3- диолео-2-линолеина;
1-пальмито-2,3-дилинолеина.
25
