
- •5 Биохимия
- •1.Отличительные признаки живой материи.
- •2.Биомолекулы (простые и сложные); биополимеры. Структурная организация клетки
- •3.Классификация природных а-аминокислот:
- •4.Основные биологические функции а-аминокислот и белков в живых организмах.
- •5.Биохимические превращения протеиногенных а-аминокислот (аланина, лизина): дезаминирование и декарбоксилирование.
- •6.Биохимические превращения протеиногенных а-аминокислот: а) трансаминирование; б) дезаминирование.
- •7. Понятие об изоэлектрической точке а-аминокислот и белков.
- •8. Первичная структура белков: определение, пептидная группа, тип химической связи.
- •9. Вторичная структура белков: определение, основные виды
- •10.Третичная и четвертичная структуры белков: определение, типы связей участвующие в их образовании.
- •11.Строение полипептидной цепи пептидов белков. Привести примеры.
- •12.Структурная формула трипептида аланилсерилтирозин.
- •13.Структурная формула трипептида цистеилглицинфенилаланина.
- •14.Классификация белков по: а) химическому строению; б) пространственной структуре.
- •15.Физико-химические свойства белков: а) амфотерность; б) растворимость; в) электрохимические; г) денатурация; д) реакция осаждения.
- •16.Углеводы: общая характеристика, биологическая роль, классификация. Доказательство строения моносахаридов на примере глюкозы и фруктозы.
- •Классификация углеводов
- •17. Реакции окисления и восстановления моносахаридов на примере глюкозы и фруктозы.
- •18. Гликозиды: общая характеристика, образование.
- •Классификация гликозидов
- •19. Брожение моно- и дисахаридов (спиртовое, молочнокислое, маслянокислое, пропионовокислое).
- •20.Восстанавливающие дисахариды (мальтоза, лактоза): строение, биохимические превращения (окисление, восстановление).
- •21. Невосстанавливающие дисахариды (сахароза): строение, инверсия, применение.
- •22.Полисахариды (крахмал, целлюлоза, гликоген): строение, отличительные биологические функции.
- •23.Нуклеиновые кислоты (днк,рнк):биологическая роль,общая характеристика,гидролиз.
- •24.Структурные компоненты нк: главные пуриновые и пиримидиновые основания, углеводная составляющая.
- •Азотистое основание Углеводный компонент Фосфорная кислота
- •Пуриновые Пиримидиновые Рибоза Дезоксирибоза
- •26.Строение полинуклеотидпой цепи (первичная структура), например, построить фрагмент Ade-Thy-Guo; Cyt-Guo-Thy.
- •27.Вторичная структура днк. Правила Чартгоффа Вторичная структура днк характеризуется правилом э. Чаргаффа (закономерность количественного содержания азотистых оснований):
- •28.Основные функции т рнк, м рнк, р рнк. Структура и функции рнк.
- •Этапы репликации:
- •Транскрипция
- •Этапы транскрипции:
- •29.Липиды (омыляемые, неомыляемые): общая характеристика, классификация.
- •Классификация липидов.
- •30.Структурные компоненты омыляемых липидов (вжк, Спирты).
- •31.Нейтральные жиры, масла: общая характеристика, окисление, гидрогенизация.
- •32.Фосфолипиды: общая характеристика, представители (фосфатидилэтаноламины, фосфатидилхолины, фосфатидилсерины, фосфатидилглицерины).
- •33.Ферменты: определение, химическая природа и строение.
- •34.Общие свойства химических ферментов и биокатализаторов.
- •35.Факторы, влияющие на каталитическую активность ферментов:
- •36.Механизм действия ферментов.
- •37.Номенклатура, классификация ферментов.
- •38.Общая характеристика отдельных классов ферментов: а)оксидоредуктазы; б) трансферазы; в) гидролазы.
- •39.Общая характеристика классов ферментов: а) лиазы; б) изомеразы; в)л и газы.
- •40.Общая характеристика витаминов, классификация витаминов; представители водорастворимых и жирорастворимых витаминов. Их биологическая роль.
- •1)По растворимости:
- •2)По физиологической активности:
- •41.Понятие о метаболических процессах: катаболические и анаболические реакции.
- •42.Особенности метаболических процессов.
- •43.Основные источники энергии для живой материи (фотосинтез, энергия, образующаяся при окислении органических соединений).
11.Строение полипептидной цепи пептидов белков. Привести примеры.
Специфичность пептидов и белков определяется двум факторами: аминокислотным составом и аминокислотной последовательностью.
А.к. состав- природа и количественное соотношение а-аминокислот входящих в состав белка.
А.К. последовательность- это порядок чередования а-аминокислот в полипептидной цепи.
О О O
׀ ׀ ׀׀ ׀ ׀
N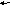 H2-CH-C-O-NH-CH-C-H
–NH-CH-C-OH
Asp-Asp-Ala
H2-CH-C-O-NH-CH-C-H
–NH-CH-C-OH
Asp-Asp-Ala
׀ ׀ ׀
CH2 CH2 CH3
׀ ׀
C=O C=O
׀ ׀
ОН ОН
Белки – это природные высокомолекулярные соединения, соединения, построенные из остатков α-аминокислот,соединенных пептидными связями.
Общий вид:
NH2-CH-C-NH-CH-C-NH-CH…NH-CH-COOH

 ׀ ׀׀ ׀ ׀׀ ׀ ׀
׀ ׀׀ ׀ ׀׀ ׀ ׀
N-конец R1 O R2 O R3 Rn С-конец
-C-NH- -пептидная группа; R1,R2,R3,Rn-боковые радикалы α- аминокислот
׀׀
O
12.Структурная формула трипептида аланилсерилтирозин.
Качественные реакции, с помощью которых можно доказать строение данного трипептида.
О О O
׀ ׀ ׀׀ ׀ ׀
NH2-CH-C-O-NH-CH-C-H –NH-CH-C-OH
׀ ׀ ׀
CH3 CH2 CH3
׀ ׀
ОН
РЕАКЦИЯ ПИОТРОВСКОГО (БИУРЕТОВАЯ РЕАКЦИЯ)
В белках аминокислоты связаны друг с другом по типу полипептидов и дикетопиперазинов. Образование полипептидов из аминокислот происходит путем отщепления молекулы воды от аминогруппы одной молекулы аминокислоты и карбоксильной группы другой молекулы:
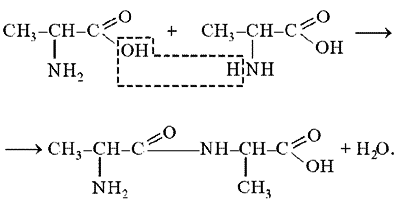
Образующаяся группа –С(О)–NН– называется пептидной группой, связь С–N, соединяющая остатки млекул аминокислот, – пептидной связью. При взаимодействии дипептида с новой молекулой аминокислоты получается трипептид и т. д.
РЕАКЦИЯ РУЭМАННА (НИНГИДРИНОВАЯ РЕАКЦИЯ (1911))
-Аминокислоты реагируют с нингидрином, образуя сине-фиолетовый комплекс (пурпур Руэманна), интенсивность окраски которого пропорциональна количеству аминокислоты.
Реакция идет по схеме:
Реакция с нингидрином используется для визуального обнаружения -аминокислот на хроматограммах (на бумаге, в тонком слое), а также для колориметрического определения концентрации аминокислот по интенсивности окраски продукта реакции.
Описание опыта. В пробирку наливают 1 мл 1%-го раствора глицина и 0,5 мл 1%-го раствора нингидрина. Содержимое пробирки осторожно нагревают до появления сине-фиолетового окрашивания.
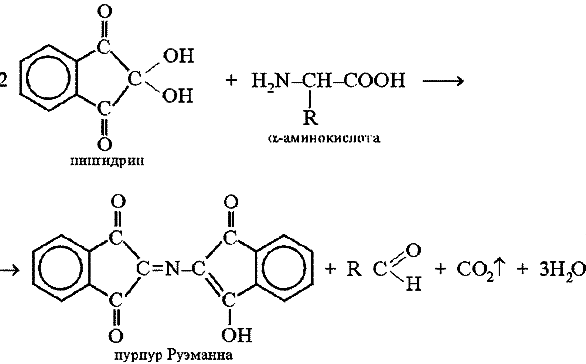
РЕАКЦИЯ С ФОРМАЛЬДЕГИДОМ
При взаимодействии -аминокислот с формальдегидом образуются относительно устойчивые карбиноламины – N-метилольные производные, содержащие свободную карбоксильную группу, которую затем титруют щелочью:
Эта реакция лежит в основе количественного определения -аминокислот методом формального титрования (метод Сёренсена).
Описание опыта. В пробирку наливают 5 капель 1%-го раствора глицина и прибавляют 1 каплю индикатора метилового красного. Раствор окрашивается в желтый цвет (нейтральная среда). К полученной смеси добавляют равный объем 40%-го раствора формальдегида (формалин). Появляется красное окрашивание (кислая среда):
![]()
РЕАКЦИЯ Циммермана
Это реакция на аминокислоту глицин.
КСАНТОПРОТЕИНОВАЯ РЕАКЦИЯ
Эта реакция используется для обнаружения -аминокислот, содержащих ароматические радикалы. Тирозин, триптофан, фенилаланин при взаимодействии с концентрированной азотной кислотой образуют нитропроизводные, имеющие желтую окраску. В щелочной среде нитропроизводные этих -аминокислот дают соли, окрашенные в оранжевый цвет
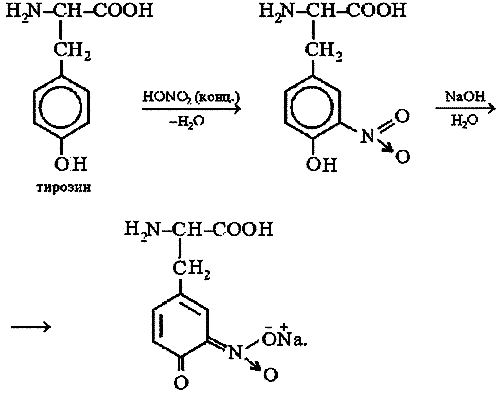
РЕАКЦИЯ НА ПРИСУТСТВИЕ СЕРОСОДЕРЖАЩИХ -АМИНОКИСЛОТ В БЕЛКЕ
Качественной реакцией на серосодержащие -аминокислоты является реакция Фоля. Белки, содержащие остатки цистеина или цистина, также дают эту реакцию.
РЕАКЦИЯ НА ТРИПТОФАН
Триптофан, реагируя в кислой среде с альдегидами, образует окрашенные продукты конденсации. Например, с глиоксиловой кислотой (являющейся примесью к концентрированной уксусной кислоте) реакция протекает по уравнению:

По аналогичной схеме протекает и реакция триптофана с формальдегидом.
