
Вьюник. Лекция № 6
.pdf
Принцип Гейзенберга |
Хвильова функцiя |
Рiвняння Шредингера |
Квантовi числа |
Екранування та проникнення |
Орбiтальне квантове число. Форма орбiталей.
В таблицi 2 наведено межi змiни орбiтального квантового числа.
n |
l |
Число значень l |
Позначення орбiталi |
1 |
0 |
1 |
1s |
|
|
|
|
2 |
0,1 |
2 |
2s2p |
|
|
|
|
3 |
0,1,2 |
3 |
3s3p3d |
|
|
|
|
4 |
0,1,2,3 |
4 |
4s4p4d4f |
|
|
|
|
Таким чином, для e¯ 1-го енергетичного рiвня можлива лише одна форма орбiталi, для другого рiвня – двi форми, для 3-го – 3, для 4-го – 4 i т.д.
21/37
Принцип Гейзенберга |
Хвильова функцiя |
Рiвняння Шредингера |
Квантовi числа |
Екранування та проникнення |
Магнiтне квантове число
Магнiтне орбiтальне квантове число (ml) характеризує розмiщення (орiєнтацiю) орбiталей (хмаринок) в просторi. Приймає значення вiд −l до +l у тому числi i 0.
Число значень ml залежить вiд l i вказує на число орбiталей з даним значенням l дорiвнює (2l + 1). Межi змiни магнiтного квантового числа наведено у таблицi 3.
l |
m |
Число |
Схематичне позначення |
|
|
ор- |
|
|
|
бита- |
|
|
|
лей |
|
|
|
2l +1 |
|
|
|
|
|
0 |
0 |
1 |
s |
|
|
|
|
1 |
-1,0,+ 1 |
3 |
px, py, pz |
2 |
-2,-1,0,+ 1,+ 2 |
5 |
dz2, dxz, dyz, dxy, dx2−y2 |
3 |
-3,-2,-1,0,+ 1,+ 2,+ 3 |
7 |
fz3, fxz2, fyz2, fxyz, fz(x2−y2), fx(x2−3y2), fy(3x2−y2 |
22/37
Принцип Гейзенберга |
Хвильова функцiя |
Рiвняння Шредингера |
Квантовi числа |
Екранування та проникнення |
Орбiталi
Орбiталi з однаковим значенням енергiї називаються виродженими: Px,Py,Pz-трикратно виродженi, d- орбiталi- п‘ятикратно виродженi, f - семикратно виродженi.
Загальна кiлькiсть орбiталей даного енергетичного рiвня дорiвнює n2.
За характером орiєнтацiї в просторi p-орбiталi позначають:
px,py,pz,
d-орбiталi dx2−y2, dz2, dxy, dxz, dyz,
f -орбiталi fx(x2−3y2), fz3, fy3, fx3, fx(x2−y2) ,fy(x2−y2) , fz(x2−y2).
23/37
Принцип Гейзенберга |
Хвильова функцiя |
Рiвняння Шредингера |
Квантовi числа |
Екранування та проникнення |
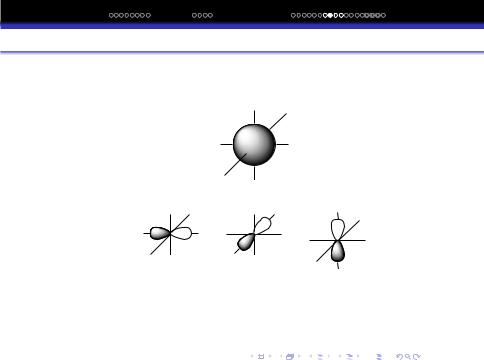
Орбiталi
z |
y |
|
|
|
x |
s
z |
y |
z |
y |
z |
|
y |
|||||
|
|
|
|
||
|
x |
|
|
x |
|
|
|
|
|
x |
px py pz
24/37
Принцип Гейзенберга |
Хвильова функцiя |
Рiвняння Шредингера |
Квантовi числа |
Екранування та проникнення |
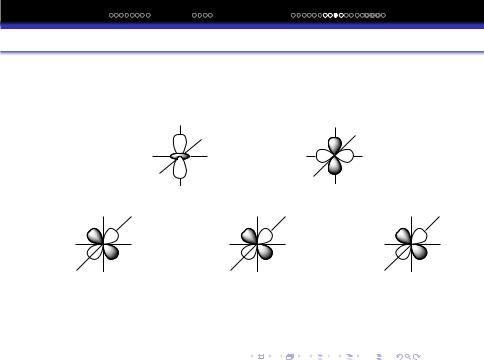
Орбiталi
|
z |
|
|
y |
|
|
y |
|
|
|
|
|
x |
|
|
x |
|
|
|
|
|
z |
|
|
dz2 |
|
|
dx2−y2 |
|
z |
y |
y |
x |
x |
z |
|
|
|
|||
|
x |
|
z |
|
y |
dxz |
|
dyz |
|
dxy |
|
25/37
Принцип Гейзенберга |
Хвильова функцiя |
Рiвняння Шредингера |
Квантовi числа |
Екранування та проникнення |
Орбiталi
Рiзниця в орiєнтацiї електронних хмаринок однiєї по вiдношенню до другої дозволяє пояснити спектри атомiв у магнiтному полi.
В спектрах атомiв розмiщених в магнiтному полi вiдбувається розщеплення лiнiй – виникнення нових близько розмiщених лiнiй, оскiльки в магнiтному полi енергiя e¯ змiнюється, так як в магнiтному полi вiдбувається зняття виродження.
26/37
Принцип Гейзенберга |
Хвильова функцiя |
Рiвняння Шредингера |
Квантовi числа |
Екранування та проникнення |
Радiальна функцiя розподiлу електронної густини
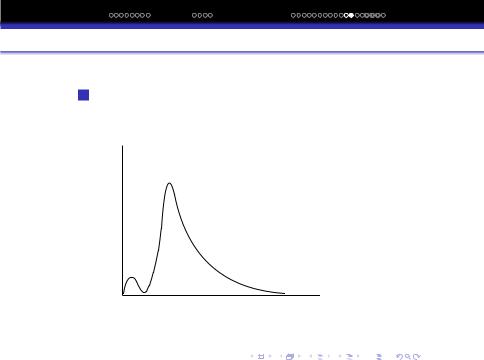
Радiальний розподiл електронної густини поблизу ядра атома гiдрогену в нормальному та збудженому станах.
На кривих розподiлу електронної густини маємо максимуми, число i положення яких визначаються головним квантовим числом. Для s- електронiв число максимумiв дорiвнює n, для p- електронiв на 1 менше, для d-електронiв на
2одиницi менше n.
1 З ростом n середнi розмiри орбiталей збiльшуються (се-
реднiй радiус стану) r¯ = a |
n2 |
h |
3 |
− |
l(l + 1) |
i, де z заряд |
|
|
2 |
||||
|
z 2 |
|
2n |
|||
◦ |
|
|
|
|||
ядра, a = 0.53A. |
|
|
|
|||
2 Лише s-орбiталi мають вiдмiнну вiд 0 густину в ядрi.
27/37
Принцип Гейзенберга |
Хвильова функцiя |
Рiвняння Шредингера |
Квантовi числа |
Екранування та проникнення |
Радiальна функцiя розподiлу електронної густини
3Серед орбiталей з одним i тим же n найвищу електронну густину поблизу ядра мають тi, у яких l менше, при цьому головний максимум тим дальше вiд ядра, чим менше l.
4πr2ψ2
n = 2 l = 0 2s
r
28/37
Принцип Гейзенберга |
Хвильова функцiя |
Рiвняння Шредингера |
Квантовi числа |
Екранування та проникнення |
Спiн електрона. Спiнове число
Спiн електрона. Ретельнi вимiри показують, що e¯ має не тiльки електростатичнi, але i магнiтнi властивостi.
Якщо пропустити через сильно змiнюване магнiтне поле потiк e¯, то початковий потiк розпадається на 2-а пучки.
Складається враження, що один пучок e¯ притягується, а другий вiдштовхується магнiтним полем. Ступiнь вiдхилення вказує на те, що кожний електрон веде себе як маленький магнiт.
Магнiтна взаємодiя квантується i iснує тiльки два можливих стани.
29/37
Принцип Гейзенберга |
Хвильова функцiя |
Рiвняння Шредингера |
Квантовi числа |
Екранування та проникнення |
Спiн електрона. Спiнове число
Чому це вiдбувається? Електрон обертається навколо своєї осi. Як кажуть має власний спiн. Це загальноприняте пояснення.
Для характеристики спiна e¯ вводиться 4-е квантове число ms- спiнове. Воно може мати тiльки два значення: +12,−12,
якi вiдрiзняються мiж собою як i другi квантовi числа на 1.
Таким чином, стан e¯в атомi може бути повнiстю охарактеризований з допомогою 4-х квантових чисел: n,l,ml,ms. Вони характеризують його спiн, енергiю e¯, об‘єм та форму простору, у якому вiрогiдно його перебування бiля ядра, орiєнтацiю електронної хмарки в просторi.
30/37
