
Вьюник. Лекция № 6
.pdf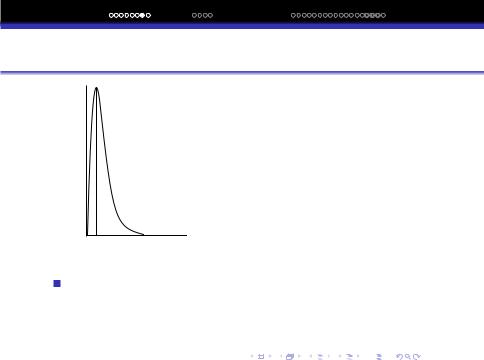
Принцип Гейзенберга |
Хвильова функцiя |
Рiвняння Шредингера |
Квантовi числа |
Екранування та проникнення |
Поняття про електронну хмаринку. Хвильова функцiя.
4πr2ψ2
n = 1
l = 0 1s
0.53 ºA |
r |
Залежнiсть w вiд r
Як видно з кривої радiального розподiлу електронної гу-
◦
стини, максимум вiдповiдає r1 = 0.53A. Така рiзниця в максимальному розподiлi електронної густини не є суперечливою.
11/37
Принцип Гейзенберга |
Хвильова функцiя |
Рiвняння Шредингера |
Квантовi числа |
Екранування та проникнення |
Поняття про електронну хмаринку. Хвильова функцiя.
Дiйсно e¯ може пiдходити на близьку вiдстань до ядра. Це можна пiдтвердити експериментально:
1Захват e¯ ядром (К-захват). Позитивний заряд ядра при цьому зменшується на 1.
2Ядерне магнiтне розщеплення. В сильному магнiтному полi електроннi магнiтики взаємодiють з ядрами-магнiтиками.
3 Спектральне розщеплення в спектрi атома H обумовлене тим, що e¯ деякий час проводить бiля ядра.
Хоча електронна густина поблизу ядра i максимальна, однак спочатку об‘єм сферичного шару r росте з ростом r швидше, нiж падає ймовiрнiсть розподiлу електронної густини, а
потiм навпаки, що i призводить до появи максимуму при
◦
r = 0.53A.
12/37

Принцип Гейзенберга |
Хвильова функцiя |
Рiвняння Шредингера |
Квантовi числа |
Екранування та проникнення |
Рiвняння Шредингера
Рiвняння Шредiнгера. Розрахунок w знаходження e¯ в данiй точцi атомного простору i його енергiї (E) – складна математична задача.
Вона розв‘язується з допомогою хвильового рiвняння Шредiнгера (1926, Австрiя). Це основне рiвняння квантової (хвильової) механiки.
Воно установлює зв‘язок мiж стацiонарними станами Бора та наявнiстю хвильових властивостей у e¯ по де-Бройлю.
Одержання цього рiвняння - великий крок у розвитку квантової механiки. Це одне iз важливих наукових досягнень, яке стоїть в ряду з внесками (вкладами) Галiлея, Ньютона i Максвела.
13/37
Принцип Гейзенберга |
Хвильова функцiя |
Рiвняння Шредингера |
Квантовi числа |
Екранування та проникнення |
Рiвняння Шредингера
При одержанi цього рiвняння Шредiнгер використав рiвняння стоячої хвилi, додавши до нього вiдоме спiввiдношення де-Бройля.
Для тривимiрного хвильового руху одного електрона в полi протона було одержано слiдуюче рiвняння:
|
8π2m |
|
|
|
|
|
|
|
|
e2 |
|||||
2ψ + |
|
|
(E − П)ψ = 0, де E = П+ К , П = − |
|
|
||||||||||
|
h2 |
r |
|||||||||||||
|
|
|
|
|
|
|
|
|
|
|
|
||||
K = |
mv2 |
, 2 |
|
∂2ψ ∂2 |
ψ ∂2ψ |
оператор Лапласа |
|||||||||
|
|
ψ = |
|
+ |
|
|
+ |
|
|||||||
2 |
∂x2 |
∂y2 |
∂z2 |
||||||||||||
|
|
|
|
|
|
|
|
|
|||||||
(лапласiан).
Оператор це вказiвка провести деяку математичну операцiю над деякою математичною величиною, x,y,z – координати, m-маса e¯, v- швидкiсть e¯.
14/37
Принцип Гейзенберга |
Хвильова функцiя |
Рiвняння Шредингера |
Квантовi числа |
Екранування та проникнення |
Рiвняння Шредингера
Рiвняння Шредiнгера є диференцiальним рiвнянням другого порядку в частинних похiдних.
Виявилося, що всi вiдомостi про поведiнку e¯ в атомi передає функцiя ψ. Знаходження ψ є розв‘язком рiвняння Шредiнгера.
Необхiдно вiдмiтити, що його розв‘язок можливий лише при вiдповiдних дискретних значеннях енергiї e¯. Таким чином пiдтверджується iдея квантування енергiї, висунена Бором в постулатi.
При розв‘язуванi хвильового рiвняння одержують двi величини: енергiю (E) i хвильову функцiю (ψ).
15/37
Принцип Гейзенберга Хвильова функцiя Рiвняння Шредингера Квантовi числа Екранування та проникнення
Рiвняння Шредингера
Обидвi цi величини залежать вiд цiлих чисел. Рiзним хвильовим функцiям (ψ1,ψ2,ψ3,....ψn) вiдповiдає своє значення енергiї (E1,E2,E3...En). Таким чином, квантування енергiї випливає iз розв‘язку хвильового рiвняння.
Хвильову функцiю, що є розв‘язком рiвняння Шредiнгера називають орбiталлю. Орбiталi описують просторовий розподiл електронної густини бiля ядра.
У зв‘зку з великими математичними труднощами точне рiшення рiвняння Шредiнгера можливе тiльки для найбiльш простого атома H.
Для атома HE потенцiальна енергiя мiстить 3-ри члена (2 притягання i 1-е вiдштовхування), у атома оксигену (O) 8 притягань та 28 вiдштовхувань.
16/37
Принцип Гейзенберга |
Хвильова функцiя |
Рiвняння Шредингера |
Квантовi числа |
Екранування та проникнення |
Квантовi числа
Це обумовлює зростання математичних труднощiв.
Хвильове рiвняння у випадку атома H описує e¯ як хвилю в 3-х вимiрах.
У зв‘язку з цим для повної характеристики стану e¯ в атомi необхiдно мати набiр iз 3-х цiлих чисел.
Цi числа називаються квантовими.
Кожний набiр квантових чисел вiдповiдає однiй iз можливих енергiй атома, а також картинi розподiлу ймовiрностi електронної густини, за якою є можливим судити про положення e¯ в атомi.
Квантовi числа визначають прийнятний розв‘язок рiвняння Шредiнгера (ψ -однозначна, безперервна, скiнчена, нормована R−+∞∞ ψ2dV = 1).
17/37
Принцип Гейзенберга |
Хвильова функцiя |
Рiвняння Шредингера |
Квантовi числа |
Екранування та проникнення |
Квантовi числа
Квантовi числа одержують при розв‘язуванi хвильового рiвняння. Три квантовi числа визначають конкретний розподiл ймовiрностi електронної густини (конкретну орбiталь), їх позначають латинськими лiтерами: n,l,m.
n – найбiльш важливе, називають головним квантовим числом. Воно приймає значення 1,2,3,...∞.
Енергiя e¯ атома H визначається формулою:
En = |
−2π2me4 1 |
, де n – є мiрою енергiї e¯ на якiй-небудь |
|||
|
|
· |
|
||
|
h2 |
n2 |
|||
орбiталi. |
|
|
|
|
|
Орбiталь з самим малим значенням n = 1 має саму низьку енергiю, тобто найбiльш вiд‘ємне значення.
18/37

Принцип Гейзенберга |
Хвильова функцiя |
Рiвняння Шредингера |
Квантовi числа |
Екранування та проникнення |
Квантовi числа
Це так званий нормальний стан для атома гiдрогену, енергетичнi ж рiвнi з n = 2,3, i т.д. є збудженими.
По мiрi зростання n зростають i енергiї орбiталей.
Вграничному станi n = ∞ ; E = 0, тобто e¯ не зв‘заний з ядром.
Внормальному (основному) станi атом може iснувати як завгодно довго, зв‘зок з ядром наймiцнiший.
Взбудженому станi атом перебуває 10−10 − 10−8сек. Збудження або промотування атома (нагрiвання, електричний розряд, дiя опромiнювання i т. iнш).
Енергiя промотування компенсується за рахунок утворення бiльш мiцних зв‘язкiв.
Поглинання енергiї: E1 −→ E2,E3 −→ E4 i т.iнш. Випромiнювання енергiї: E2 −→ E1,E3 −→ E1.
19/37
Принцип Гейзенберга |
Хвильова функцiя |
Рiвняння Шредингера |
Квантовi числа |
Екранування та проникнення |
Орбiтальне квантове число. Форма орбiталей.
Орбiтальне квантове число: Для характеристики форми електронної орбiталi, а також i форми електронної хмаринки вводиться орбiтальне квантове число l, яке приймає значення в залежностi вiд n: l = 0,1,2,3...(n − 1).
l вiдповiдає значенню орбiтального кутового моменту (M):
h p
M = 2π l(l + 1).
Орбiтальне квантове число зазвичай позначають малими латинськими лiтерами в залежностi вiд його значення:
Орбiтальне квантове число l |
0 |
1 |
2 |
3 |
4 |
5 |
Позначення енергетичного пiдрiвня |
s |
p |
d |
f |
g |
h |
|
|
|
|
|
|
|
20/37
