
- •Тематический план лабораторных и практических занятий по химии для студентов лечебного и педиатрического факультетов
- •Правила техники безопасности при работе в химической лаборатории
- •Меры первой помощи
- •Форма отчета
- •Занятие №1
- •Лабораторная работа №1
- •Занятие №4
- •Лабораторная работа №2
- •1. Приведите примеры буферных систем с рН больше или меньше 7 при равных концентрациях кислоты и сопряженного основания.
- •3. Какой из двух буферных растворов характеризуется меньшим значением рН:
- •Занятие №5
- •Лабораторная работа №3
- •Занятие № 6
- •Лабораторная работа №4
- •2. Объясните, почему литий образует малорастворимые в воде соли - фториды, фосфаты, карбонаты, в то время как соли других s-элементов металловI-а группы хорошо растворимы?
- •3. Какие связи (ионные, ковалентные) характерны в соединениях s-элементов с неметаллами?
- •Занятие №7
- •Лабораторная работа № 5
- •Занятие № 8
- •Лабораторная работа №6
- •Занятие № 9
- •Лабораторная работа №7
- •Занятие №10
- •Лабораторная работа № 8
- •Занятие №11
- •Лабораторная работа № 9
- •1. Напишите уравнение реакции катехина (1,2-дигидроксибензола) с ацетатом свинца
- •2. Напишите уравнение реакции окисления этанола бихроматом калия в кислой среде.
- •Занятие №14
- •Лабораторная работа № 10
- •1. Какое практическое значение имеет реакция -аминокислот с нингидрином?
- •5. Приведите химизм взаимодействия -аланина с хлороводородной кислотой и гидроксидом натрия.
- •7. Какие -аминокислоты в составе белка могут быть обнаружены с помощью ксантопротеиновой реакции?
- •Занятие №15
- •Лабораторная работа № 11
- •Занятие № 16
- •Лабораторная работа № 12
Занятие №11
Полифункциональные соединения (многоатомные спирты и фенолы, полиамины, двухосновные карбоновые кислоты)
Лабораторная работа № 9
Свойства одно- и многоатомных спиртов и фенолов
Опыт № 1. Окисление этилового спирта хромовой смесью
Реакция используется для экспрессного обнаружения следовых количеств этилового спирта в выдыхаемом воздухе.
Смешивают в пробирке 2 мл раствора бихромата калия, 1 мл концентрированной серной кислоты и 0,5 мл этилового спирта и осторожно нагревают смесь.
Химизм процесс: Течение реакции обнаруживается по изменению окраски раствора, а образование ацетальдегида - по характерному для него запаху яблок. Ацетальдегид в избытке бихромата калия в дальнейшем окисляется до уксусной кислоты.

Наблюдения.
____________________________________________________________________________________________________________________________________________________________________________________________________________________________________________________________________________________________________________________________________________________
Выводы._________________________________________________________________________________________________________________________________________________________________________________________________________________________________________________________________________________________________________________________________________________________________________________________________________________
Опыт №2.Образование иодоформа из спирта
Смешивают в пробирке 3-4 капли исследуемого спирта и 2-3 мл воды. Полученный раствор слегка нагревают (лучше всего на водяной бане при 60С), добавляют к нему 0,5 -1,0 мл растворя йода и затем приливают разбавленный раствор щелочи по каплям до исчезновения окраски. В случае образования иодоформа выделяется светло-желтая муть или осадок и появляется характерный запах.
Химизм процесса: В условиях опыта йод и щелочь вступают в обратимую реакцию:
![]()
Образующаяся соль иодноватистой кислоты является сильным окислителем и переводит первичные спирты в альдегиды:

Вторичные спирты окисляются до кетонов. Атомы водорода в группах -СО-СН3, -СО-СН2-, -СО-СН- легко замещаются галогенами, в частности йодом.
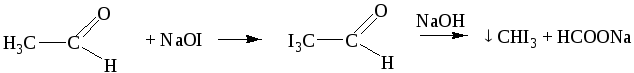
Ничтожно малая растворимость иодоформа в воде позволяет обнаружить по реакции его образования даже следы этилового спирта в водном растворе. Реакция широко используется в химико - токсикологическом анализе для установления алкоголя в желудке умерших людей.
Наблюдения.
_______________________________________________________________________________________________________________________________________________________________________________________________________________________________________________________________________________ Выводы._________________________________________________________________________________________________________________________________________________________________________________________________________________________________________________________________________
Опыт № 3Комплексообразование многоатомных спиртов
В пробирке получают гидроксид меди, для чего в разбавленный раствор сульфата меди вводят в небольшом избытке раствор едкой щелочи. Затем в пробирку добавляют 3-5 капель жидкого спирта (глицерина, этиленгликоля). Встряхнув пробирки, дают их содержимому отстояться и отмечают появление характерной окраски жидкости.
Химизм процесса: С увеличением числа гидроксильных групп в молекуле спирта кислотность спиртов возрастает, что определяет легкость образования с гидроксидом меди комплексных алкоголятов меди
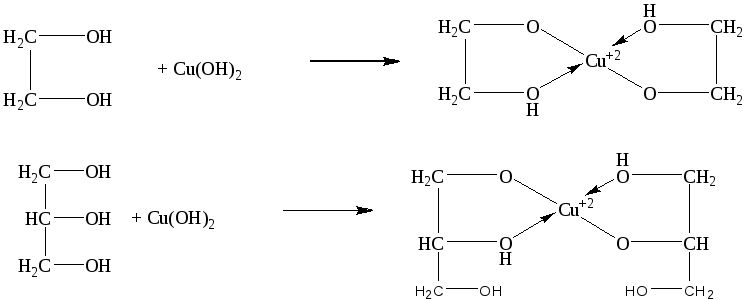
Наблюдения.
____________________________________________________________________________________________________________________________________________________________________________________________________________________________________________________________________________________________________________________________________________________
Выводы.
____________________________________________________________________________________________________________________________________________________________________________________________________________________________________________________________________________________________________________________________________________________
Опыт № 4Реакция фенолов с хлоридом железа
Многие одно- и многоатомные фенолы, содержащие в молекуле один или несколько фенольных гидроксила, дают с водным раствором хлорида железа интенсивное окрашивание того или иного цвета, характерное для данного фенола.
К 5-6 каплям 1% раствора фенола добавляют 3-5 капель раствора хлорида железа (III). Аналогично проводят реакцию с катехинами чая (витамин Р).
Химизм
процесса: Окрашивание появляется в
результате образования сильно
диссоциированных комплексных фенолятов,
образующихся по уравнению:
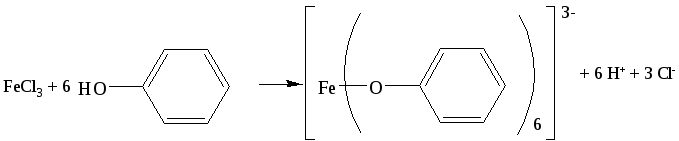
Хлорид железа способен также окислять фенолы до хинонов.
Наблюдения.
________________________________________________________________________________________________________________________________________________________________________________________________________________________________________________________________________________
Выводы. ____________________________________________________________________________________________________________________________________________________________________________________________________________________________________________________________________________________________________________________________________________________________________________________________________________________________________________________________________________________________
Опыт № 5.Обнаружение двухатомных фенолов
Двухатомные фенолы, флавоноиды, содержащие соседние гидроксильные группы, образуют с ацетатом свинца осадки, окрашенные в желто-оранжевый, красный или синий цвет.
К 1 мл спиртового 0,50% раствора кверцетина добавляют несколько капель 1% раствора ацетата свинца.
Химизм процесса:
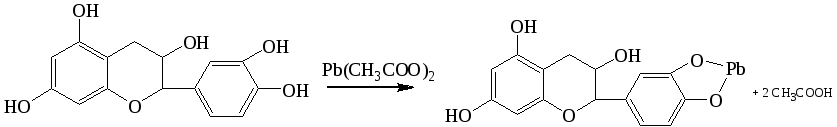
Наблюдения:
____________________________________________________________________________________________________________________________________________________________________________________________________________________________________________________________________________________________________________________________________________________
Выводы._____________________________________________________________________________________________________________________________________________________________________________________________________________________________________________________________________________________________________________________________________________
Опыт № 6Обнаружение токоферола (витамина Е)
Токоферол выделен в 1936 г из масла зародышей пшеницы. Это соединение является основным природным антиоксидантом.
К 1 мл спиртового 0,1% раствора -токоферола добавляют 2-3 капли 0,5% раствора хлорида железа в спирте и 2-3 капли 0,5% раствора 2,2-дипиридила.
Химизм процесса: Для идентификации токоферолов используют реакции окисления. При окислении токоферолов спиртовым раствором FeCl3происходит разрыв пиранового цикла с образованием-токоферилхинона желтого цвета по схеме:

-токоферол -токоферилхинон
Реакцию
ведут обычно в присутствии 2,2-дипиридила,
который с образовавшимсяFeCl2дает комплексное соединение, окрашенное
в интенсивно красный цвет.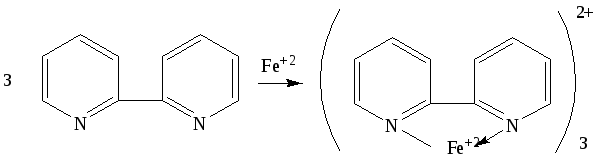
Наблюдения.
____________________________________________________________________________________________________________________________________________________________________________________________________________________________________________________________________________________________________________________________________________________
Выводы
____________________________________________________________________________________________________________________________________________________________________________________________________________________________________________________________________________________________________________________________________________________
Вопросы к защите работы.
