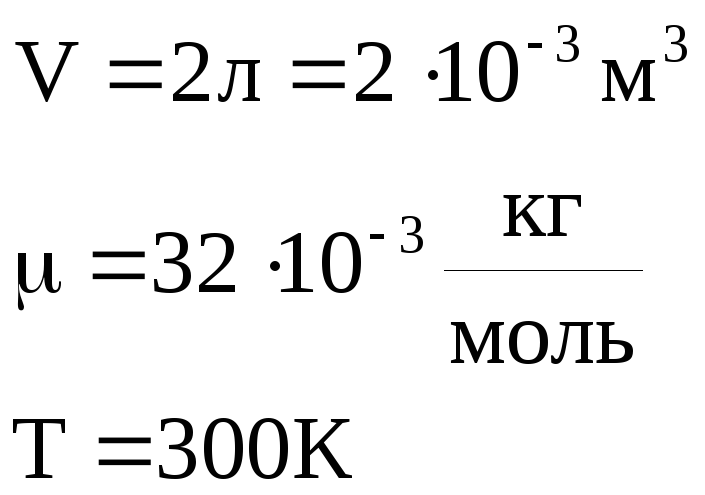- •Учебное пособие
- •Содержание
- •1. Физические основы механики
- •1.1. Основные формулы
- •1.2. Примеры решения задач к разделу «Механика»
- •1.3. Базовые задачи для самостоятельного решения
- •1.4. Контрольные вопросы
- •2. Основы молекулярной физики и термодинамики
- •2.1. Основные формулы
- •2.2. Примеры решения задач к разделу «Молекулярная физика и термодинамика»
- •2.3. Базовые задачи для самостоятельного решения
- •2.4. Контрольные вопросы
- •Библиографический список
- •Приложения
- •1. Основные физические постоянные (округленные значения)
- •2. Некоторые астрономические величины
2.2. Примеры решения задач к разделу «Молекулярная физика и термодинамика»
Пример
№ 1.
1 кг
двухатомного газа находится под давлением
р=8104
Па и имеет плотность
![]() .
Найти энергию теплового движения
молекул газа при этих условиях.
.
Найти энергию теплового движения
молекул газа при этих условиях.
|
Дано: m = 1 кг i = 5 р=8104 Па
|
Решение: Внутренняя энергия газовой системы определяется уравнением
U=
|
|
U - ?
|
Поскольку плотность
![]() ,
тогда p =
,
тогда p =![]() но
но![]() (2)
(2)
Таким образом из уравнений (1) и (2) имеем
U =
![]() . Подставив значения, получаем:
U =
. Подставив значения, получаем:
U =
![]() =
=![]() Дж
Дж
Проверка размерности
![]()
Ответ: U = 5 104 Дж.
Пример № 2. Чему равна наиболее вероятная скорость движения молекул кислорода при температуре Т = 273 К?
|
Дано: T = 273 K μ = 32 ∙10-3 кг/моль |
Решение:
Наиболее вероятная скорость молекул
определяется по формуле:
|
|
|
Подставим численные значения:
![]()
Ответ: ![]()
Пример № 3. Определить среднюю длину свободного пробега молекул и число соударений за 1 с, происходящих между всеми молекулами кислорода, находящегося в сосуде емкостью 2 л при температуре 27оС и давлении 100 кПа.
|
Дано:
|
Решение: Средняя длина свободного пробега молекул вычисляется по формуле:
где d – эффективный диаметр молекулы, n – концентрация, т.е. число молекул в единице объема. Давление связано с концентрацией:
|
|
<λ>, z - ? |
Выразим n:
![]() (2)
(2)
Подставим формулу (2) в (1) и получим:
![]() (3)
(3)
Число соударений, происходящих между всеми молекулами за 1 с равно:
![]() (4)
(4)
где N - число молекул в сосуде объемом V, < z > - среднее число соударений одной молекулы за 1 с.
Число молекул в сосуде равно:
![]() (5)
(5)
Среднее число соударений молекулы за 1 с:
![]() (6)
(6)
где < > – средняя арифметическая скорость молекулы, равная
![]() (7)
(7)
Подставим в формулу (4) выражения (5), (6), (7):
![]()
Учтем формулу (2):
![]()
Проверим справедливость формулы по размерности величин

Подставим числовые значения:
![]()
![]()
Ответ:
![]() ,
,![]() .
.
Пример № 4. Горячая вода некоторой массы отдает теплоту холодной воде такой же массы и температуры их становятся одинаковыми. Показать, что энтропия при этом увеличивается.
Решение: Обозначим температуру горячей воды Т1, холодной Т2, а температуру смеси Q. Определим температуру смеси, исходя из уравнения теплового баланса:
![]() ,
,
где с
– удельная теплоемкость, m – масса воды.
Тогда: ![]() .
.
Отсюда температура смеси равна:
![]() (1)
(1)
Изменение энтропии, происходящее при охлаждении горячей воды, равно:
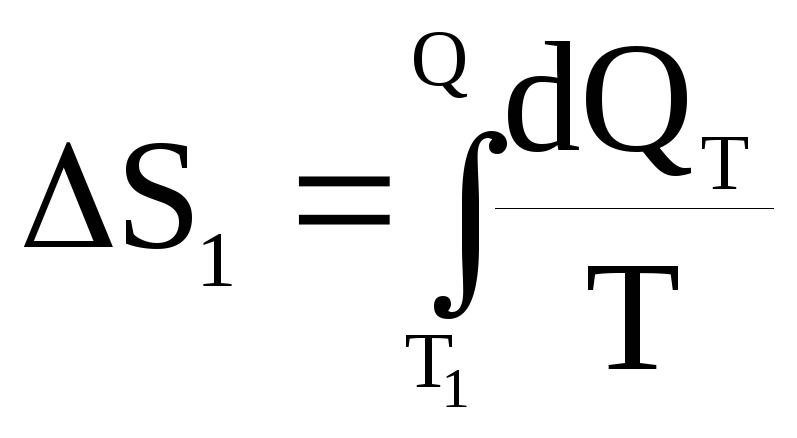 .
.
Элементарное количество теплоты равно:
![]() .
.
Тогда изменение энтропии, происходящее при охлаждении воды, равно:
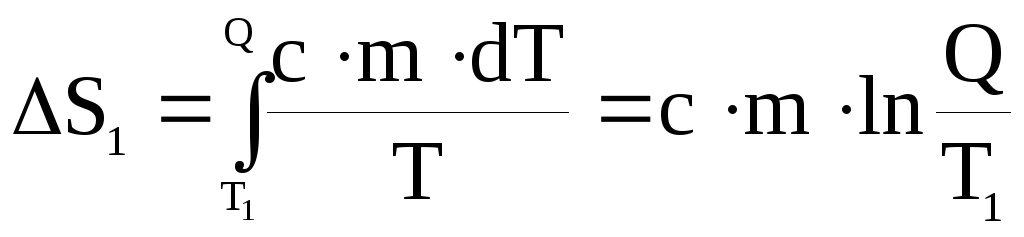 .
.
Изменение энтропии, происходящее при нагревании холодной воды, равно:
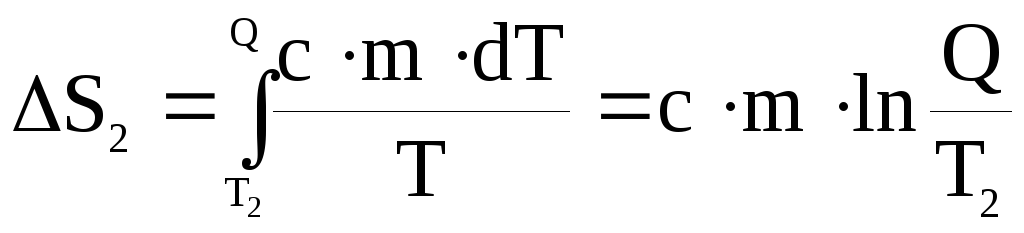 .
.
Изменение энтропии системы равно:
![]() .
.
С учетом (1) получим:
![]() .
.
Так
как
![]() ,
то
,
то![]() ,
следовательно:
,
следовательно:![]() и
и![]() .
Тогда
.
Тогда![]() ,
т.е. энтропия возрастает.
,
т.е. энтропия возрастает.
Ответ: энтропия возрастает.