
- •Отдельное спасибо ребятам со второго потока лечебного факультета 2012 г.
- •1)Мультиферментные комплексы и изоферменты. Кдз определения активности изоферментов. Энзимодиагностика. Ферментативные лекарственные препараты.
- •2) Окисление жирных кислот. Внутриклеточная локализация и биоэнергетика процесса. Особенности обмена жк с нечетным количеством углеродных атомов и ненасыщенных жк.
- •3) О каком заболевании следует думать, если моча новорожденного ребенка дает положительную реакцию на наличие фенилпирувата? Какой молекулярный блок лежит в основе данной патологии?
- •1)Классификация ферментов. Общая характеристика класса лиаз. Коферменты лиазных рекций.
- •2) Регуляция липидного обмена. Гормоны влияющие на обмен липидов. Патология липидного обмена : гиперлипидемия, атеросклероз, липоидозы, жировое перерождение печени, ожирение.
- •1)Классификация гормонов по локализации рецеторов. Вторичные посредники действия гормонов.
- •2) Гемоглобин, его структура, синтез, виды. Гемоглобинозы.
- •1)Белки плазмы крови, место их синтеза, биологическая роль. Изменение белкового спектра сыворотки при различных заболеваниях. Белки острой фазы.
- •2) Глюкоза крови. Пути ее поступления и использования. Гексокиназная реакция – клучевая реакция углеводного обмена. Пусти превращения глюкозо-6-фосфата.
- •1)Дыхательная цепь. Ферментные комплексы дыхательной цепи, их локализация. Редокс-потенциалы ферментных систем. Ингибиторы переноса электронов.
- •2) Адреналин и норадреналин, их синтез и влияние на обмен веществ.
- •1)Особенности обмена в эритроцитах. Эритроцитарные энзимопатии. Синтез гема. Порфирин.
- •3) Оцените состояние больного по следующим данным анализа крови и мочи: глюкоза крови – 10,0 ммоль/л, рН крови – 7,30, в моче обнаружены глюкоза, кетоновые тела.
- •1)Эндокринная система оргранизма. Классификация гормонов по химической структуре, их роль в регуляции обменных процессов. Причины эндокринных заболеваний. Механизм действия гормонов.
- •Причины заболеваний эндокринной системы.
- •1)Биологические мембраны, их структурные компоненты. Функции биологических мембран.
- •2) Патология углеводного обмена. Сахарный диабет. Нарушение углеводного и липидного обмена при этом заболевании.
- •1. Гипергликемия вызвана:
- •3) В крови больного повышена активность липазы, амилазы, трипсина. О какой патологии следует думать? Какие реакции катализируются данными ферментами?
- •1) Классификация ферментов. Общая характеристика класса трансфераз. Основные подклассы. Коферменты трансферазных реакций.
- •2)Напишите последовательность реакций превращения ацетил-КоА в мевалоновую кислоту в процессе синтеза холестерина. Укажите ферменты и коферменты.
- •3) Биохимический анализ нормальной и патологической мочи. Глюкозурия, протеинурия, кетонурия, билирубинурия.
- •2) Витамины, их классификация. Витамин в12 и фолиевая кислота, участие в обмене веществ и признаки витаминной недостаточности.
- •3) Какие изменения белкового спектра будут наблюдаться при остром воспалении? Что такое белки «острой фазы»? Диагностическое значение определения их концентрации в крови.
- •1)Роль воды в организме. Водный баланс, его регуляция и патология. Макроэлементы: натрий, калий, хлор, магний.
- •2) Биосинтез днк (репликация). Биосинтез рнк (транскрипция). Посттранскрипционный процессинг рнк. Основные положения аминокислотного кода. Обратная транскрипция.
- •2)Витамин в6, биотин, их химическая структура и признаки витаминной недостаточности. Участие в обмене веществ.
- •3)Будет ли протекать глюконеогенез, если в клетке цитратный цикл и дыхательная цепь полностью ингибированы. Ответ поясните.
- •1)Классификация и характеристика сложных белков (липопротеины, хромопротеины, гликопротеины, нуклеопротеины, фосфопротеины).
- •2) Вторичный липолиз триглицеридов. Окисление глицерина до конеч¬ных продуктов (со2 и н2о). Биоэнергетика процесса.
- •1)Структура гликогена, синтез и распад гликогена в печени и мышцах. Гликогенозы.
- •2) Изогидрия. Механизмы поддержания изогидрии. Ацидоз и алкалоз.
- •3) Сипмтомами авитаминоза в1 является расстройство нервной систе¬мы, потеря памяти, изменение психики. Почему к дефициту витамина в1 особо чув¬ствительна центральная нервная система?
- •1)Паратгормон и тиреокальцитонин. Влияние гормонов на обмен кальция и фосфора в организме человека
- •2) Сопряжение обмена углеводов и липидов. Сопряжение обмена углеводов и аминокислот. Пути превращения и образования пировиноградной кислоты.
- •1)Обмен и биологическое значение серосодержащих аминокислот (метионин и цистеин). Участие метионина в реакциях трансметилирования. Молекулярная патология обмена этих аминокислот.
- •2) Микроэлементы: селен, цинк, марганец, стронций, фтор, йод, молибден. Микроэлементозы.
- •3) Оценить состояние больного, если: рН крови - 7,31, рН мочи - 4,8. Общее содержание со2 в крови повышено. РСо2 - 80 мм рт ст. Титрометрическая кислотность мочи повышена.
- •1)Основные пути обмена аминокислот: декарбоксилирование, дезаминирование. Биологическая роль биогенных аминов.
- •2) Витамины р и с, их структура, признаки витаминной недостаточности, влияние на обмен веществ.
- •3) У больного после переливания крови развилась желтуха. Какой вид желтухи можно заподозрить? Как изменились показатели пигментного обмена в крови и моче?
- •1)Классификация ферментов. Общая характеристика класса оксидоредуктаз. Коферменты оксидоредуктазных реакций.
- •Характеристика фермента
- •2) Гормональная регуляция углеводного обмена. Гормоны, повышающие и понижающие уровень глюкозы в крови. Механизм их действия.
- •3) В крови снижено содержание мочевины. Нарушение какого метаболического пути можно предположить, каковы возможные причины этих нарушений?
- •1)Понятие об обмене веществ. Процессы анаболизма и катаболизма, их характеристика и взаимосвязь. Виды метаболических путей. Центральные метаболиты.
- •I . Подготовительная фаза.
- •II фаза. Превращение мономеров в простые соединения - центральные метаболиты (пвк, ацетилКоА)
- •III фаза. Цикл Кребса
- •2) Витамины рр и в2, структура, признаки витаминной недостаточности и участие в обмене веществ.
- •1)Обмен и биологическое значение глутаминовой и аспарагиновой аминокислот в организме человека.
- •2)Микроэлементы: железо, медь и кобальт. Их роль в организме. Понятие о микроэлементозах.
- •3) Пациенту в лечебных целях назначили диету с низким содержанием углеводов. Концентрация глюкозы в крови нормальная. За счет каких процессов преимущественно поддерживается уровень глюкозы в крови?
- •1) Основные пути промежуточного обмена аминокислот. Трансаминирование. Клиническое значение определения активности трансаминаз.
- •2) Антиоксидантная система организма. Неферментативные антиоксиданты. Антиоксидантные ферменты.
- •1)Гормоны передней доли гипофиза, их химическая структура и влияние на обмен веществ. Последствия изменений продукции соматотропного гормона в организме.
- •2)Глюконеогенез. Основные субстраты, ключевые ферменты процесса. Цикл Кори
- •3)Больной 50 лет поступил в клинику с жалобами на резкие боли в области сердца, слабость. Активность каких ферментов следует определить в крови больного для исключения инфаркта миокарда?
- •1)Холестерин, его биологическая роль, биосинтез. Гиперхолестеринемии. Атеросклероз.
- •2) Кровь, ее роль в организме. Химический состав плазмы. Калликреин-кининовая система.
- •3)Для лечения подагры применяется аллопуринол, структурный аналог гипоксантина. Объясните биохимический механизм действия данного лекарственного средства.
- •1)Кинетика ферментативных реакций. Зависимость скорости ферментативных реакции от концентрации субстрата и фермента, рН и температуры среды. Принципы количественного определения активности ферментов.
- •1. Зависимость скорости реакции от температуры
- •2. Зависимость скорости реакции от рН
- •3. Зависимость скорости реакции от концентрации субстрата
- •4. Зависимость от концентрации фермента
- •2) Синтез жирных кислот. Внутриклеточная локализация. Биосинтез триацилглицеролов.
- •1)Нуклеопротеины и нуклеиновые кислоты. Структурная организация молекул днк и рнк. Распад нуклеопротеинов в пищеварительном тракте. Нуклеотидный пул клеток, пути его пополнения и расходования.
- •2)Витамины а, е, к, влияние на обмен веществ, признаки витаминной недостаточности.
- •3)Оценить состояние больного по следующим данным анализа крови: активность креатинфосфокиназы повышена, общая активность лдг повышена, преимущественно за счет лдг1. Коэффициент де Ритиса - 1,90.
- •1)Биологическая роль печени. Роль печени в обмене углеводов, липидов, аминокислот и белков. Антитоксическая роль печени.
- •2)Биосинтез пуриновых и пиримидиновых нуклеотидов. Оротовая ацидурия.
- •1)Распад гемоглобина. Образование билирубина и продуктов его обмена. Характеристика прямого и непрямого билирубина. Диагностическое значиние их определения. Классификация желтух.
- •2)Глюкоза крови. Гипергликемия, гипогликемия, глюкозурия. Диагностическое значение определния глюкозы в крови и моче.
- •1)Гликолиз. Биологическая роль, химизм процесса, биоэнергетика, регуляция. Эффект Пастера.
- •2)Витамин d. Химическая природа витамина, гормонально-активные формы. Участие витамина в обмене веществ. Рахит.
- •3)Какова судьба гемоглобина, попавшего в плазму крови в результате гемолиза эритроцитов?
- •2. Регуляция и патология белкового обмена
- •3. Ответ. Поражение тканей печени. За счет изофермента лдг 4 и 5
- •1. 4,5 8,0 4,3
- •2. 6,1 14,0 10,0
- •2.Биохимия мышечной ткани
- •3. Ответ: 1 пациент – норма, 2 пациент – сахарный диабет.
- •1. Переваривание белков. Диагностическое значение биохимического анализа желудочного и дуоденального сока.
- •Условно заменимые аминокислоты ( могут образоваться из других кислот в организме )
- •Незаменимые аминокислоты ( нужно употреблять каждый день с пищей )
2) Витамины рр и в2, структура, признаки витаминной недостаточности и участие в обмене веществ.
B2 –Рибофлавин G2-2,5 мг/сут
Флавинмононуклеотид (ФМН) и флавинадениндинуклеотид (ФАД) являются производными
витамина В2 (диметилизоаллоксазинрибитола).
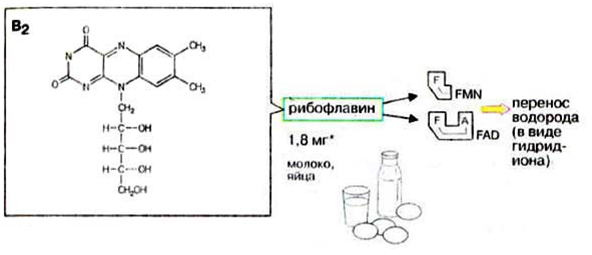
Пищевые источникивитамина В2: капуста, горох, яблоки, зеленая фасоль, помидоры, репа, дрожжи, яйца, печень, мясо, молоко.
Дефицит витамина В2:
-расстройство пищеварения и нервной системы,
-хронические гастриты и колиты,
-общая слабость,
-кожные заболевания,
-снижает сопротивляемость болезням.
Биофункция: Входит в состав дыхательных флавиновых ферментов (ФМФ и ФАД). Осуществляет переносH+иe–.
Авитоминоз/гипервитаминоз:
Поражение глаз, светобоязнь, поражение слизистой полости рта, глоссит, задержка роста.
PP Никотиновая кислота15-25 мг/сут Кофермент оксидоредуктаз
Биороль: Участвует в процессах клеточного дыхания (переносH+иe–). Регулирует секреторные и моторные функции желудочно-кишечного тракта и печени. Входит в состав НАД и НАДФ.
НАД и НАДФ:
Никотинамидадениндинуклеотид (НАД) и никотин-амидадениндинуклеотидфосфат (НАДФ) - производные витамина РР -никотинамида (антипеллагрического витамина).
Пищевые источники: Мясо, печень, почки, рыба, дрожжи.
Авитоминоз/гипервитаминоз: Воспаление кожи (пеллагра), расстройства желудочно-кишечного тракта.
Авитаминоз РР – пеллагра(болезнь трех Д):
-дерматит,
- деменция,
- диарея.
Симптомы пеллагры наиболее резко выражены у больных с недостаточным белковым питанием. Это объясняется недостатком триптофана, который является предшественником никотинамида.
3) В моче больного найдено значительное количество гомогентизиновой кислоты. Как образуется гомогентизиновая кислота в организме. Содержится ли она в моче здоровых людей? Назовите заболевание, обнаруженное у выше указанного больного и причину его возникновения?
Алкаптонурия.
Образование гомогентизиновой кислоты:
У животных является промежуточным соединением в процессе катаболизмааминокислотфенилаланинаитирозина:
Фенилаланин→Тирозин⇋ п-гидроксифенилпировиноградная кислота→ Гомогентизиновая кислота →Малеилацетоуксусная кислота→Фумарилацетоуксусная кислота→Фумаровая кислота+Ацетоуксусная кислота
Гомогентизиновая кислота является предшественником токоферолов,пластохинона.
Медицина
При наследственном заболевании алкаптонурия, выражающемся в нарушении обмена аминокислот из-за отсутствия оксидазы гомогентизиновой кислоты, метаболизм аминокислот останавливается на стадии образования гомогентизиновой кислоты, которая выводится с мочой.
Билет 20
1)Обмен и биологическое значение глутаминовой и аспарагиновой аминокислот в организме человека.
Глу и асп – первичные и заменимые АМК
Пути синтеза:
-восстановительное аминирование,
-трансаминирование
Глутамин синтезируется из глу под действием глутаминсинтетазы.
Аспарагин синтезируется из асп и глутамина.
Судьба Асп:
-Аспарагин
-Синтез пуриновых и пиримидиновых омнований
-В-аланин: КоАSH, Азотистые веществава мыщц: анзерин,карнозин
Судьба Глу:
-Фолиевая кислота
-Глутамин
-Пролин
-Глутатион
-Синтез Пуриновых нуклеотидов
Глутамин:
нетоксичен, свободно проходит через клеточную мембрану,
форма, в которой транспортируется аммиак, временное хранилище аммиака,
используется для синтеза белка, аминосахаров, пуриновых и пиримидиновых нуклеотидов, фолиевой кислоты, глу, три, гис, асн,
донор аммиака.
Образование амидов АМК:

Образование аммонийных солей:
глутамин используется почками в качестве источника аммиака, необходимого для нейтрализации кислых продуктов.
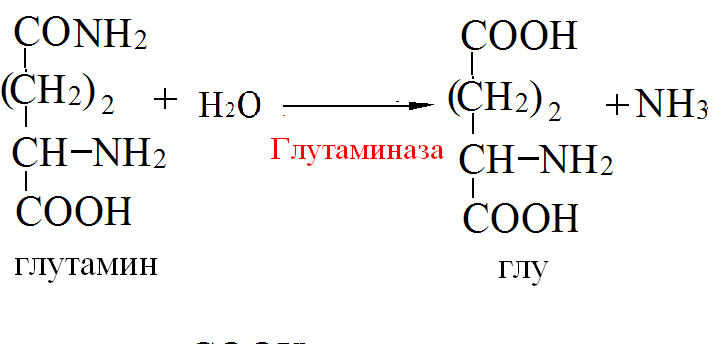
Аспарагиновая кислота(аминоянтарная кислота, аспартат, аминобутандиовая кислота) — алифатическая аминокислота, одна из 20 протеиногенных аминокислот организма. Встречается во всех организмах в свободном виде и в составе белков. Кроме того, выполняет роль нейромедиатора в ЦНС.
Аспарагиновая кислота:
- присутствует в организме в составе белков и в свободном виде
- играет важную роль в обмене азотистых веществ
- участвует в образовании пиримидиновых оснований и мочевины
Аспарагиновая кислота и аспарагинявляются критически важными для роста и размножения лейкозных клеток при некоторых видах лимфолейкоза.
Фермент микробного происхождения L-аспарагиназа, нарушающий превращение аспарагиновой кислоты в аспарагини наоборот, оказывает сильное специфическое цитостатическое действие при этих видах лейкозов.
Основные функции
Аспарагиновая кислота является прямым предшественником аспарагинаи участвует в синтезе незаменимых аминокислотметионинаитреонина, в синтезе пиримидиновых нуклеотидов. Она играет важную роль в обмене веществ, в деятельности ДНК и РНК, синтезе иммуноглобулинов, способствует удалению вредного аммиака из организма. Важный фактор предотвращения усталости.
Аспарагиновая кислота, будучи связывающим субстратом энергетического и пластического обмена, обладает способностью повышать основной обмен и участвует в передаче и модуляции межнейронных сигналов.
Используется в качестве биологически активной добавки в питании спортсменов.
Потребность
Cуточная потребность - 6 г.
Пищевые источники
Значительное количество аспарагиновой кислоты содержат проращенных семенах
Физиологич.роль:
-присутствует в организме в составе белков и в свободном виде
-играет важную роль в обмене азотистых веществ
-участвует в образовании пиримидиновыхоснований имочевины
-Аспарагиновая кислота и аспарагинявляются критически важными для роста и размножениялейкозныхклеток при некоторых видахлимфолейкоза.
-Ферментмикробногопроисхождения L-аспарагиназа, нарушающий превращение аспарагиновой кислоты в аспарагин и наоборот, оказывает сильное специфическоецитостатическоедействие при этих видах лейкозов.
