
- •Министерство здравоохранения Республики Беларусь
- •Введение
- •Химический эквивалент. Основы титриметрического метода анализа
- •Техника выполнения лабораторных работ и техника безопасности
- •Первая помощь при ожогах и отравлениях *
- •Фундаментальные единицы измерения
- •Лабораторная посуда
- •Методические указания к занятию № 2
- •Химический эквивалент
- •Молярная масса химического эквивалента
- •Количество вещества эквивалента
- •Молярная концентрация химического эквивалента
- •Закон эквивалентов
- •1. Примеры расчета молярной концентрации эквивалента (нормальной концентрации)
- •2. Контролирующие задания
- •3. Выполнение индивидуальных заданий
- •Методические указания к занятию № 3
- •Титриметрический анализ. Общая характеристика метода
- •Требования, предъявляемые к реакциям, которые используют в титриметрии
- •Способы титрования
- •Способы приготовления рабочих растворов
- •Правила работы с мерной посудой при проведении аналитических измерений
- •Мерные колбы
- •Пипетки
- •Бюретки
- •Проведение титрования
- •Методические указания к занятию № 4
- •Кислотно-основное титрование. Общая характеристика метода
- •Определение точки эквивалентности в кислотно-основном титровании. Кислотно-основные индикаторы
- •Подбор индикаторов при кислотно-основном титровании
- •Кривые титрования многоосновных (полипротонных) кислот, многокислотных оснований и их солей
- •Применение кислотно-основного титрования
- •Расчет: вычисляют средний объем (V) кислоты, пошедшей на титрование, с точностью до сотых мл
- •Методические указания к занятию № 5
- •Редоксиметрия. Общая характеристика и классификация методов
- •Кривые титрования в редоксиметрии
- •Способы определения точки эквивалентности
- •Перманганатометрия
- •Иодометрия
- •Расчет: вычисляют средний объем (V) kMnO4,, пошедшей на титрование с точностью до сотых мл
- •Тесты к теме: Закон эквивалентов. Титриметрия
- •Учение о растворах Методические указания к занятию № 6
- •1. Задачи для самостоятельного решения
- •Методические указания к занятию № 7
- •1. Задачи для самостоятельного решения
- •Тесты к теме: Растворы. Электролитическая диссоциация. Буферные растворы
- •Методические указания к занятию № 8
- •Лабораторная работа № 2: Прочность и разрушение комплексных ионов.
- •Тесты к теме: Комплексные соединения
- •Химическая кинетика и катализ Методические указания к занятию № 9
- •1. Задачи для самостоятельного решения
- •Тесты к теме: Скорость химических реакций
- •Методические указания к занятию № 10
- •Тесты к теме: Катализ
- •Электрохимия Методические указания к занятию № 11
- •Методические указания к занятию № 12
- •Тесты к теме: Электрохимия. Электропроводимость растворов
- •Поверхностные явления Методические указания к занятию № 13
- •Методические указания к занятию № 14
- •Тесты к теме: Поверхностные явления. Адсорбция
- •Физическая химия дисперсных систем Методические указания к занятию № 15
- •Методические указания к занятию № 16
- •Тесты к теме: Дисперсные системы. Коллоидные растворы
- •Методические указания к занятию № 17
- •Тесты к теме: Растворы биополимеров
- •Химия биогенных элементов Методические указания к занятию № 18
- •Общая характеристика биогенных элементов.
- •Общая характеристика групп элементов общая характеристика элементов VII а группы Нахождение в природе
- •Строение атомов галогенов, их физические и химические свойства
- •Общая характеристика элементов
- •VI а группы Нахождение в природе
- •Строение атомов, химические и физические свойства халькогенов
- •Общая характеристика элементов
- •V a группы Нахождение в природе
- •Строение атомов, физические и химические свойства пниктогенов
- •Общая харатеристика элементов
- •Ivа группы Нахождение в природе
- •Физические и химические свойства элементов iva группы
- •Общая характеристика элементов II а группы Нахождение в природе
- •Общая характеристика элементов iiа группы на основании строения их атомов и положения в таблице д.И. Менделеева
- •Общая харатеристика элементов
- •I а группы Нахождение в природе
- •Общая характеристика щелочных металлов на основании строения их атомов и положения в таблице д.И. Менделеева
- •Физические свойства простых веществ
- •Общая харатеристика d-элементов
- •Качественные реакции на важнейшие биогенные элементы
- •1. Химическая термодинамика
- •2. Строение атома, химическая связь
- •Тесты по темам кср Химическая термодинамика
- •Строение атома. Химическая связь
- •Вопросы для подготовки к экзамену по общей химии для лечебного и педиатрического факультетов
- •Вопросы для подготовки к экзамену по общей химии для медико-психологического факультета
- •Содержание
- •VI а группы 287
- •V a группы 290
- •Ivа группы 296
- •I а группы 303
- •Подписано в печать 20 .07.2011.
Бюретки
В титриметрии бюретки используются для постепенного прибавления с регулируемой скоростью одного раствора к другому с последующим измерением общего объёма расходованной при этом жидкости. Таким образом, с помощью бюреток непосредственно осуществляется сам процесс титрования.
Бюретка представляет собой узкую стеклянную трубку, на которую нанесена шкала делений (рис. 11).
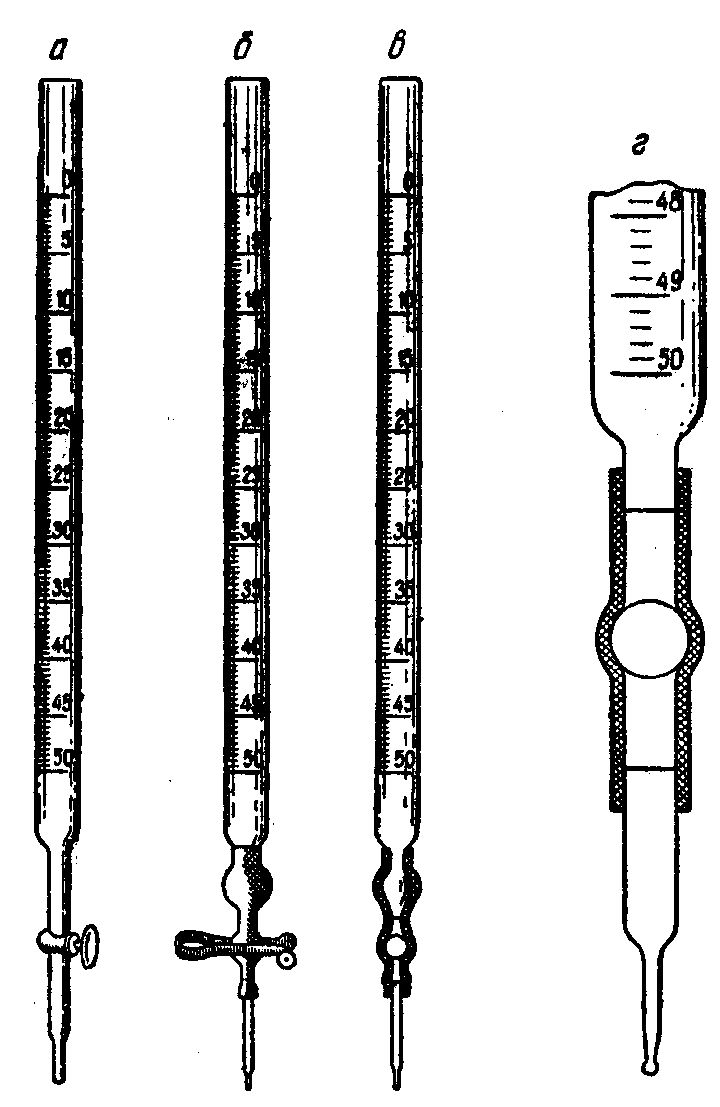
Рис. 11. Бюретки
В лабораторной практике обычно используются бюретки ёмкостью 25 – 50 мл (с ценой деления 0,1 мл). Для измерения малых объёмов жидкостей применяются бюретки емкостью от 1 до 5 мл (с ценой деления 0,01 мл). Такие бюретки называются микробюретками (рис. 12).
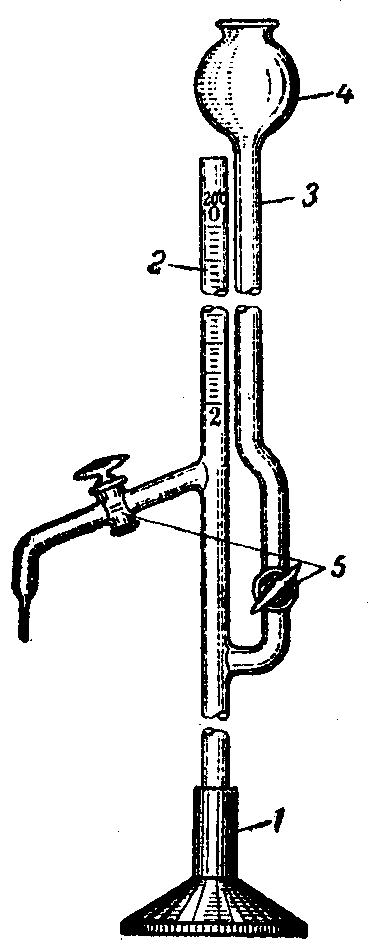
Рис. 12. Микробюретка с краном: 1 - деревянный штатив; 2 - микробюретка; 3 - трубка для заполнения бюретки жидкостью; 4 - воронка; 5 - краны.
На нижнем конце бюретки находится стеклянный пришлифованный кран (рис.11 а), или небольшое овальное расширение, на которое плотно надевается резиновая трубка со стеклянным, оттянутым в капилляр, концом. Резиновая трубка зажимается металлическим зажимом или стеклянной бусиной, представляющей собой стеклянный шарик с диаметром немного больше внутреннего диаметра резиновой трубки (рис.11 б, в). Шарик помещается внутри трубки между концом бюретки и оттянутым стеклянным концом. Нажимая большим и указательным пальцами резиновую трубку возле шарика, образуют внутри узкий просвет, через который жидкость вытекает из бюретки с большей или меньшей скоростью (рис. 11 г).
У бюреток, снабжённых краном, кран смазывают очень тонким слоем вазелина, следя за тем, чтобы вазелин не попал в канал крана.
Перед титрованием бюретку нужно подготовить в работе. Для этого её тщательно моют, ополаскивают несколько раз дистиллированной H2O, а затем раствором, которым она должна наполняться. Бюретку закрепляют в штативе в вертикальном положении, заполняют с помощью воронки нужным раствором до 2/3 её объёма. В кране или резиновой трубке и в наконечнике не должно оставаться пузырьков воздуха. Чтобы удалить их, нужно несколько раз быстро открыть и закрыть кран (зажим) и спустить жидкость сильной струёй.
В бюретках со стеклянным шариком для удаления воздуха отгибают вверх резиновую трубку с наконечником и нажимают на шарик. Жидкость выливается через загнутую кверху резиновую трубку и вытесняет из неё и наконечника весь воздух (рис. 13).
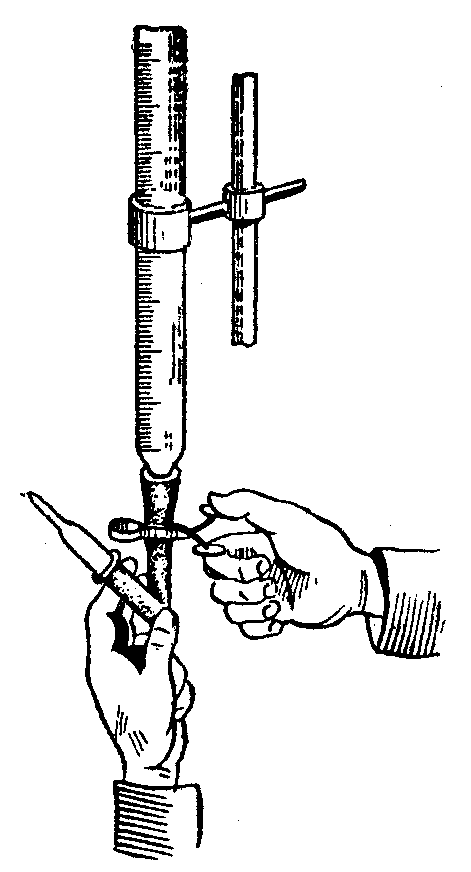
Рис. 13. Удаление воздуха из кончика бюретки
Убедившись в полном удалении воздуха, бюретку снова заполняют жидкостью – сначала выше нулевого деления, а затем, открыв кран либо зажим или надавив на шарик, точно до нулевого деления.
Отсчёты уровня светлых жидкостей производят по их нижнему мениску, а тёмных – по верхнему. При выполнении нескольких измерений в каждом из них все отсчёты делают аналогичным образом.
Проведение титрования
С помощью пипетки отмеряют, а затем переносят в колбу для титрования соответствующий объём раствора. Если титрование осуществляют в присутствии индикатора, то в колбу для титрования добавляют несколько его капель (как правило, 1-2 капли). Приготовленную таким образом колбу помещают на листе белой бумаги под носиком бюретки (рис. 14).
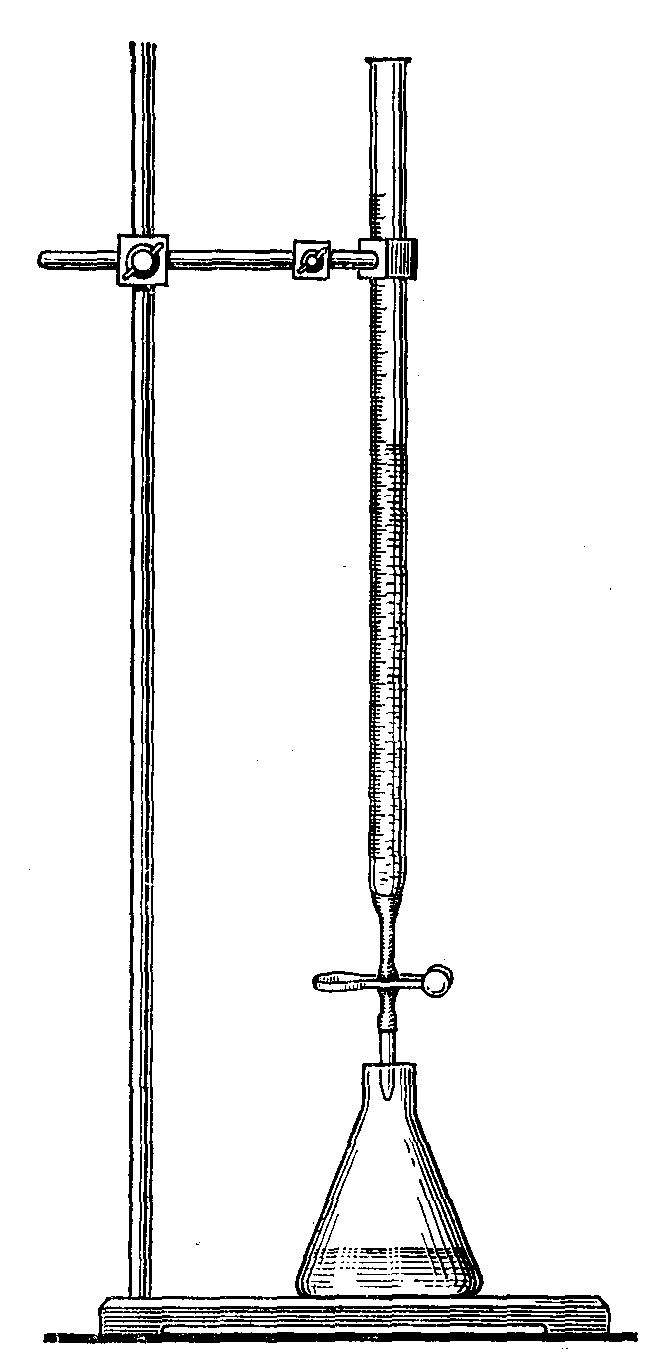
Рис. 14. Положение колбы и бюретки при титровании
Нажимая большим и указательным пальцами левой руки на шарик бюретки, добавляют в колбу небольшими порциями второй раствор. При этом правой рукой осторожно встряхивают колбу для быстрого перемешивания раствора.
Вблизи точки эквивалентности раствор в колбе в месте падения капли раствора из бюретки на некоторое время приобретает окраску, характерную для точки эквивалентности. Это может служить признаком приближающегося конца реакции титрования. В этом случае раствор из бюретки начинают прибавлять по одной капле, каждый раз внимательно наблюдая окраску смеси в колбе.
После стойкого (неисчезающего) изменения окраски титрование прекращают и записывают показание объема жидкости в бюретке.
Первое титрование служит для ориентировочного установления объёма и при расчётах не используется. Титрование с тем же исходным объёмом раствора в колбе проводят ещё не менее трёх раз. Перед началом каждого нового опыта уровень жидкости в бюретке снова доводят до нулевой отметки.
Первую порцию жидкости при повторном титровании спускают из бюретки одномоментно (объём её должен быть немного меньше 0,5-1 мл) результата первого титрования. После этого дотитровывают раствор по каплям до наступления точки эквивалентности. По результатам нескольких измерений рассчитывают средний объём раствора, пошедшего на титрование.
Практическая часть занятия
1. Определить цену деления пипетки.
2. При помощи градуированной пипетки отмерить:
а) 5 мл дистиллированной воды;
б) 8,7 мл дистиллированной воды;
в) 0, 4 мл дистиллированной воды.
3. Определить цену деления бюретки.
4. Заполнить бюретку дистиллированной водой и отмерить:
3 мл дистиллированной воды;
6,2 мл дистиллированной воды;
0,8 мл дистиллированной воды.
Вывод: ________________________________________________________________________________________________________________________________________________________________________________________________________________________________________________________________________________________
________________________________________________________
________________________________________________________________________________________________________________________________________________________________________
Дата ___________ Подпись преподавателя___________
