
Активный транспорт
Активный транспорт — энергозависимый трансмембранный переноспротивэлектрохимическогоградиента. Различают первичный и вторичный активный транспорт. Первичный активный транспорт осуществляютнасосы(различные АТФазы), вторичный —симпортёры(сочетанный однонаправленный транспорт) иантипортёры(встречный разнонаправленный транспорт).
Первичныйактивныйтранспорт. Движущая сила трансмембранного переноса возникает при ферментативном гидролизе макроэргических связей АТФ. Родовой термин для таких АТФаз (например, Na+,K+-, H+,K+-, Ca2+‑АТФазы) —насосы.
Вторичныйактивныйтранспорт. Движущая сила для трансмембранного переноса одного вещества (или ионов)противэлектрохимическогоградиентавозникает за счёт потенциальной энергии, запасённой за счёт сочетанного переноса ионов (как правило, Na+)поэлектрохимическомуградиенту. В большинстве случаев поступление Na+в цитозоль из межклеточного пространства и обеспечивает вторичный активный транспорт разных ионов и веществ. Известно 2 типа вторичного активного переноса —симпортиантипорт(рис. 2–6).
· Первичныйактивныйтранспортобеспечивают следующие насосы — натрий, калиевые АТФазы, протонные и калиевые АТФазы, Са2+-транспортирующие АТФазы, митохондриальные АТФазы, лизосомальные протонные насосы и др.
Натрий,калиеваяАТФаза(рис. 2–11) регулирует трансмембранные потоки основных катионов (Na+, K+) и опосредованно — воды (что поддерживает постоянный объём клетки), обеспечивает Na+–связанный трансмембранный перенос (симпорт и антипорт) множества органических и неорганических молекул, участвует в создании МП покоя и генерации ПД нервных и мышечных элементов.
Электрогенность. При каждом цикле гидролиза АТФ 3 иона Na+выбрасываются из клетки, а 2 иона K+поступают в цитозоль, суммарный эффект — выброс из клетки одного катиона. Другими словами, Na+,K+‑насос обладает электрогенностью: его работа приводит к поддержанию положительного заряда наружной (внеклеточной) поверхности мембраны.
Сердечныегликозиды(например, уабаин и дигоксин) блокируют работу Na+,K+–насоса, конкурентно с K+взаимодействуя с участком связывания K+на наружной поверхности мембраны. В результате при гипокалиемии (низкий [K+] плазмы крови) увеличивается токсичность сердечных гликозидов.
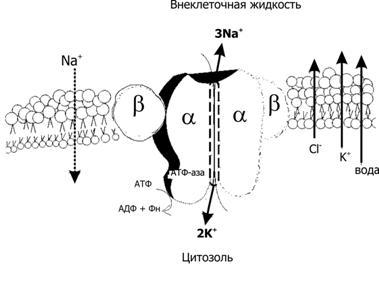
Рис.2–11.Na+,K+–насос [7]. Модель Na+,K+–АТФазы, встроенной в плазматическую мембрану. Na+,K+–насос — интегральный мембранный белок, состоящий из 4 СЕ (формирующие канал 2 каталитические субъединицы a и 2 гликопротеина b). Na+,K+‑насос осуществляет транспорт катионов против электрохимического градиента (mX) — транспортирует Na+из клетки в обмен на K+ (при гидролизе одной молекулы АТФ 3 иона Na+выкачиваютсяиз клетки, и 2 иона K+закачиваютсяв неё). Слева и справа от насоса при помощи стрелок показаны направления трансмембранного потока ионов и воды в клетку (Na+) и из клетки (K+, Cl–и вода) в силу различий их DmX. АДФ — аденозиндифосфат, Фн — неорганический фосфат.
ПротоннаяикалиеваяАТФаза(H+,K+‑насос). При помощи этого фермента париетальные клетки желёз слизистой оболочки желудка участвуют в образовании соляной кислоты (электронейтральный обмен 2 внеклеточных ионов K+на 2 внутриклеточных иона H+при гидролизе одной молекулы АТФ).
H+,K+‑АТФаза — гетеродимер (2 высокомолекулярных a‑СЕ и 2 меньшей мол. массы и сильно гликозилированной b‑СЕ).
b‑СЕ — главный Аг, к которому при некоторых заболеваниях (например, при витамин B12–анемиях и атрофическом гастрите) в крови циркулируют АТ.
Са2+-транспортирующиеАТФазы(Са2+‑АТФазы)выкачиваютионыкальцияизцитоплазмывобменнапротоныпротив значительного электрохимического градиента Са2+.
Са2+‑АТФазыплазмолеммыпереносят ионы кальция из цитоплазмы во внеклеточное пространство в обмен на протоны (1 H+в обмен на 1 Ca2+при гидролизе 1 молекулы АТФ).
Са2+‑АТФазысаркоплазматическогоретикулума. Как и Са2+‑АТФазы плазмолеммы, Са2+-транспортирующие АТФазы саркоплазматического ретикулумаоткачиваютионыкальцияизцитоплазмы(2 H+в обмен на 2 Ca2+при гидролизе 1 молекулы АТФ), но не во внеклеточное пространство, а вовнутриклеточныедепокальция(в замкнутые межмембранные объёмы гладкой эндоплазматической сети, именуемой в скелетных МВ и кардиомиоцитах — саркоплазматический ретикулум). Недостаточность Са2+‑АТФазы саркоплазматического ретикулума проявляется симптомами мышечной усталости (миопатия) при физической нагрузке.
МитохондриальнаяАТФазатипа F (F0F1) — АТФ–синтаза внутренней мембраны митохондрий — катализируют конечный этап синтеза АТФ (рис. 2–12). Кристы митохондрий содержат АТФ-синтазу, сопрягающую окисление в циклеКребса и фосфорилирование АДФ до АТФ. АТФ синтезируется при обратном токе протонов в матрикс через канал в АТФ-синтезирующем комплексе.
Хемиосмотическоесопряжение. Сопряжение переноса электронов и синтеза АТФ (механизм предложилПитер Митчеллв 1961 г.) обеспечивает протонный градиент. Внутренняя мембрана непроницаема для анионов и катионов. Но при прохождении электронов по дыхательной цепи ионы H+ откачиваются из матрикса митохондрий в межмембранное пространство (рис. 2–12). Эта энергия электрохимического протонного градиента и используется для синтеза АТФ и транспорта метаболитов и неорганических ионов в матрикс.

Рис.2–12.МеханизмхемиосмотическогосопряженияприобразованииАТФвмитохондриях[11]. При транспорте электронов по дыхательной цепи из матрикса через внутреннюю мембрану в межмембранное пространство митохондрий поступает H+. Созданный таким образом электрохимический градиент (DmH) позволяет АТФ-синтазе катализировать реакцию АДФ + неорганический фосфат (Фн) ® АТФ.
Лизосомальныепротонныенасосы(H+‑АТФазы типа V [от Vesicular]), встроенные в мембраны, окружающие лизосомы (также комплексГольджии секреторные пузырьки), транспортируют H+из цитозоля в эти мембранные органеллы. В результате в них понижается значение pH, что оптимизирует функции этих структур.
ТранспортёрыABC(отATP-BindingCassette — АТФ-связывающая последовательность) — либо гидролизующие АТФ насосы для активного транспорта разных ионов и молекул, либо ионные каналы или регуляторы ионных каналов. Так, генCFTR(от cystic fibrosis transmembrane regulator — трансмембранный регулятор кистозного фиброза) кодирует структуру хлорного канала (одновременно регулятор функционирования других каналов), мутации которого приводят к развитию муковисцидоза (кистозного фиброза).
· Вторичныйактивныйтранспорт. Известны 2 формы активного вторичного транспорта: сочетанный (симпорт) и встречный (антипорт) (см. рис. 2–6).
Симпорт— сочетанный перенос (котранспорт, сочетанный транспорт) — движение двух веществ сквозь мембрану при помощи одного и того же переносчика (симпортёра).
Антипорт— одновременное трансмембранное перемещение двух веществ, но в противоположном направлении (встречный транспорт) при помощи одного и того же переносчика (антипортёра, обменника).
Симпортреализуют интегральные мембранные белки. Перенос вещества Х против его электрохимического градиента (mХ) в большинстве случаев происходит за счёт поступления в цитозоль из межклеточного пространства по градиенту диффузии ионов натрия (т.е. за счёт DmNa), а в ряде случаев — за счёт поступления в цитозоль из межклеточного пространства по градиенту диффузии протонов (т.е. за счёт DmH). В итоге и ионы (Na+или H+), и вещество Х (например, глюкоза, аминокислоты, неорганические анионы, ионы калия и хлора) перемещаются из межклеточного вещества в цитозоль.
Всасываниеглюкозыпроисходит через верхушечные поверхности клеток, окаймляющих просвет проксимальных извитых канальцев почки и тонкого кишечника при помощи сочетанного транспорта с ионами Na+. Разные изоформы транспортёра переносят Na+и глюкозу в соотношении 1:1 или 2:1. Расчёты показывают, что максимальная концентрация глюкозы в клетке может в 100 или в 104раз превышать её концентрацию в плазме крови.
При стехиометрии 1:1 движущая сила равна сумме разностей электрохимического потенциала для Na+(DmNa) и химического потенциала для глюкозы (Dmглюкоза). Равновесие достигается, когда DmNaв одном направлении становится равным Dmглюкозав противоположном направлении:
Уравнение2–5
–DmNa= Dmглюкоза
Выражая «DmNa» через концентрации Na+снаружи (сн) и изнутри (вн) мембраны и МП (Vm), а «Dmглюкоза» через концентрации глюкозы снаружи (сн) и изнутри (вн) мембраны, можно вычислить максимально возможный трансмембранный градиент концентрации глюкозы:
Уравнение2–6
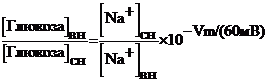
Для эпителиальной клетки градиент концентрации Na+десятикратен (это соответствует десятикратному градиенту концентрации глюкозы), а значение МП для внутренней поверхности мембраны –60мВ (это соответствует ещё десятикратному градиенту концентрации глюкозы).
При стехиометрии 2:1:
Уравнение2–7
2DmNa = –Dmглюкоза
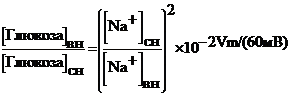
получаем максимальный теоретический трансмембранный градиент концентрации глюкозы в 104.
Всасываниеаминокислотэпителиальными клетками проксимальных извитых канальцев нефрона и энтероцитами тонкого кишечника происходит при сочетанном транспорте вместе с Na+.
Неорганическиеанионы(фосфаты, сульфаты, бикарбонаты) транспортируют разные переносчики в сочетании с транспортом Na+.
Калийихлор. Известно несколько Na+‑котранспортёров K+и Cl–. В частности, в плазмолемму свободной поверхности эпителия восходящего отдела петлиХенлевстроены ингибируемые фуросемидом (петлевой диуретик) переносчики (все 3 иона транспортируются в цитозоль). В то же время выход K+и Cl–из клетки осуществляет не зависящий от Na+K+,Cl–‑котранспортёр.
Разныепротонныекотранспортёрыосуществляют одновременный с H+перенос в цитозоль олигопептидов (эпителий проксимальных извитых канальцев почки), лактата и пирувата (многие клетки), дивалентных металлов (например, Fе2+ в канальцах нефрона и тонком кишечнике).
Антипорт(встречный, или обменный транспорт), как правило, перемещает анионы в обмен на анионы и катионы в обмен на катионы. Движущая сила обменника формируется за счёт поступления в клетку Na+.
Na+-Ca2+-обменниквмонтирован в плазмолемму всех клеток и вместе с Ca2+‑насосом плазмолеммы приводит к практически полному удаление Ca2+из цитозоля (в обмен на поступление в цитозоль 3 ионов натрия). Эта стехиометрия обмена (3:1) обеспечивает трансмембранную разницу (DmCa) на 4 порядка величин.
Na+-H+-обменникосуществляет обмен внеклеточного Na+на внутриклеточный H+в соотношений 1:1, что важно для поддержания внутриклеточного pH, объёма клеток, секреции кислот (H+) и абсорбции Na+.
Na+-Cl–-HCO–3-обменникэлектронейтрален и сочетает однонаправленный вход в клетку 1 Na+и 2 HCO–3и транспорт из клетки 1 Cl–. Как и Na+-H+-обменник, этот транспортёр сдвигает значение внутриклеточного pH в щёлочную сторону.
Cl–-HCO–3-обменник(обменник анионов) функционирует независимо от потока Na+. Направленный внутрь клетки градиент Cl–одновременно транспортирует НСО–3из клетки. Этот анионный обменник важен для обеспечения функции дыхания: через обменник в лёгких НСО–3поступает в эритроциты, тогда как в тканях НСО–3выходит из эритроцитов. Потоки НСО–3важны для регуляции внутриклеточного pH, а потоки Cl–для регуляции клеточного объёма.
Обменникиорганическиханионовобеспечивают поглощение гепатоцитами билирубина и жёлчных кислот, различными клетками — простаноидов (ПгE2, ПгF2a,тромбоксанаB2), клетками почечных канальцев — органических анионов, антибиотиков, парааминогиппуровой кислоты.
