
ЗАНЯТИЕ № 7
ТЕМА: МИКРОБИОЛОГИЧЕСКИЕ ОСНОВЫ ХИМИОТЕРАПИИ БАКТЕРИАЛЬНЫХ ИНФЕКЦИЙ. АНТИСЕПТИКА.
ПЕРЕЧЕНЬ КОНТРОЛЬНЫХ ВОПРОСОВ
-
Противомикробные мероприятия. Влияние экологических факторов на микробы. Действие физических факторов (температуры, высушивания, излучений, ультразвука, осмотического давления). Действие химических факторов.
-
Цели, способы, средства и объекты стерилизации и дезинфекции в медицинской и микробиологической практике. Контроль качества дезинфекции. Контроль стерилизации и стерильности. Способы проведения.
-
Антисептика. Определение. Антисептические средства, требования, происхождение, свойства, группы, механизмы действия на микробы. Типы антисептики. Терапевтическая антисептика. Профилактическая антисептика.
-
Химиотерапевтические препараты. Свойства. Основные группы химиопрепаратов. Механизмы действия на бактерии. Понятие об избирательности и "мишенях" действия.
-
Органические и неорганические соединения металлов и металлоидов. Сульфаниламидные препараты. Препараты нитрофуранового ряда. Противогрибковые, противовирусные, противопаразитарные химиопрепараты.
-
Антибиотики. Определение. Продуценты антибиотиков. Синтетические и полусинтетические антибиотики.
-
Основные группы антибиотиков по химической структуре. Бета-лактамные антибиотики Тетрациклины. Аминогликозиды. Макролиды и азолиды. Анзамицины (рифампицины). Левомицетин. Фторхинолоновые антибиотики. Линкомицин. Полимиксины. Гликопептиды
-
Классификация антибиотиков про механизму действия на бактериальную клетку.
-
Механизмы устойчивости микроорганизмов к антибактериальным препаратам.
-
Методы определения чувствительности бактерий к антибиотикам и другим химиопрепаратам. Техника постановки, учета и оценки чувствительности методом дисков, Е-теста, серийных разведений.
ЛАБОРАТОРНАЯ РАБОТА
1► Впишите в таблицу возможные способы и режимы стерилизации указанных объектов:
|
Стерилизуемые объекты |
Способы и режимы стерилизации |
|
Бактериологические петли |
Стерилизация пламенем мгновенно |
|
Перевязочный материал (марля, вата, бинт) |
Стерилизация паром под давлением 2 атм (132ºС) 20 минут |
|
Резиновые, пластиковые изделия |
Стерилизация паром под давлением 1 атм (121ºС) 45 минут, газовая стерилизация (окись этилена), |
|
Стеклянные изделия |
Стерилизация сухим жаром 180ºС 1 час |
|
Основные питательные среды (МПА, МПБ) |
Стерилизация паром под давлением 1 атм (121ºС) 20 минут |
|
Питательные среды, содержащие белок |
Дробная стерилизация (тиндализация) 56ºС в течение часа 5-6 суток подряд |
|
Растворы, содержащие вещества, которые инактивируются при температуре свыше 60оС |
Стерилизация фильтрованием, Ɣ излучением |
Методы определения чувствительности микроорганизмов к антибиотикам
Диско-диффузионный метод
Н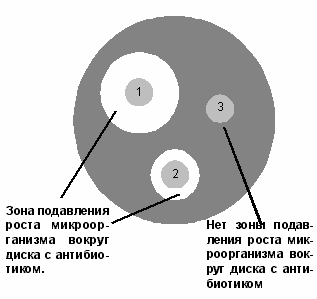 а
поверхность плотной питательной среды,
засеянной сплошным газоном исследуемой
культурой, накладывают не более 6 дисков,
пропитанных антибиотиками, на расстоянии
не менее 2 см друг от друга. Регистрация
результатов проводится через 18-24 часов
инкубирования в термостате по диаметру
зоны отсутствия роста вокруг дисков с
антибиотиками. Наличие роста вокруг
диска свидетельствует о нечувствительности
данного микроба к антибиотику. Для
интерпретации результатов используются
специальные таблицы.
а
поверхность плотной питательной среды,
засеянной сплошным газоном исследуемой
культурой, накладывают не более 6 дисков,
пропитанных антибиотиками, на расстоянии
не менее 2 см друг от друга. Регистрация
результатов проводится через 18-24 часов
инкубирования в термостате по диаметру
зоны отсутствия роста вокруг дисков с
антибиотиками. Наличие роста вокруг
диска свидетельствует о нечувствительности
данного микроба к антибиотику. Для
интерпретации результатов используются
специальные таблицы.
Рисунок 1. Определение чувствительности
микроорганизмов диско-диффузионным методом:
1 – микроорганизм чувствителен к антибиотику;
2 – микроорганизм умеренно резистентен к антибиотику;
3 – микроорганизм устойчив к антибиотику.
Метод Е-тестов Принцип метода. Определение чувствительности микроорганизма проводится аналогично тестированию диско-диффузионным методом. Отличие состоит в том, что вместо диска с антибиотиком используют полоску Е-теста, содержащую градиент концентраций антибиотика от максимальной к минимальной. В месте пересечения эллипсовидной зоны подавления роста с полоской Е-теста получают значение минимальной подавляющей концентрации (МПК).
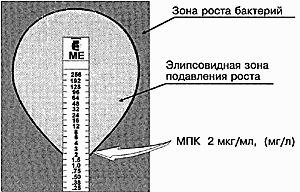
Рисунок 2. Определение чувствительности микроорганизмов с помощью Е-тестов
Метод серийных разведений в бульонной среде Берут 9 пробирок, содержащих 1 мл бульона Мюллер-Хинтона. Одна из них служит контролем роста бактерий, а в остальных готовят двукратные серийные разведения антибактериального препарата. Например, 32 мг/л – 1-я, 16 мг/л – 2-я, 8 мг/л – 3-я, 4 мг/л – 4-я и т.д. Затем в каждую пробирку вносят 0,1 мл испытуемой бактериальной суспензии. Посевы инкубируют при 37°С в течение 18-24 ч., отсутствие помутнения среды свидетельствует о задержке роста бактерий в присутствии данной концентрации препарата.
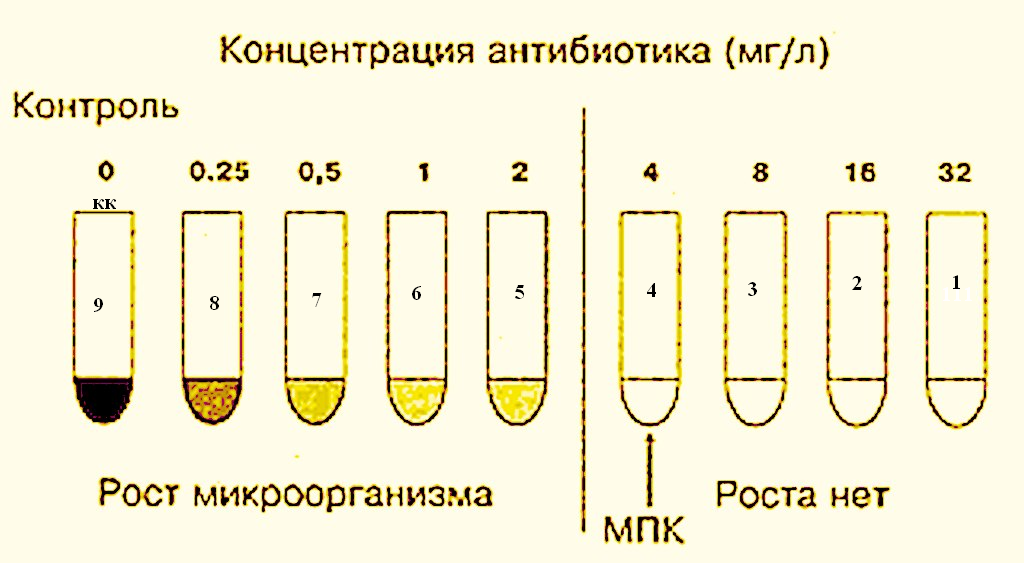
Рисунок 3. Определение значения МПК методом разведения в жидкой питательной среде
Минимальная подавляющая концентрация (МПК) – наименьшая концентрация антибиотика (в мкг/мл или мг/л), которая in vitro полностью подавляет видимый рост бактерий.
2► Определение чувствительности разных штаммов стафилококков к антибиотикам методом стандартных дисков
|
Антибиотик |
Зона подавления роста, мм |
Характеристика штамма |
|
1. Оксациллин |
|
|
|
2. Ко-тримоксазол |
|
|
|
3. Рифампицин |
|
|
|
4. Эритромицин |
|
|
|
5. Ванкомицин |
|
|
|
6. Ципрофлоксацин |
|
|
Исследуемая культура является чувствительной (S), умеренно устойчивой к (I), устойчивой (R) _.
Достоинства метода: Легко воспроизводимый метод Недостатки метода: качественный метод, не позволяет определить МПК препарата./
3►Определение минимальной подавляющей концентрации (МПК) пенициллина методом серийных разведений.
Вывод: МПК пенициллина для исследуемого штамма составляет (см . рисунок № 3) 4 мг/мл
Достоинства метода: количественный , позволяет определить МПК препарата
Недостатки метода: трудновоспроизводимый метод
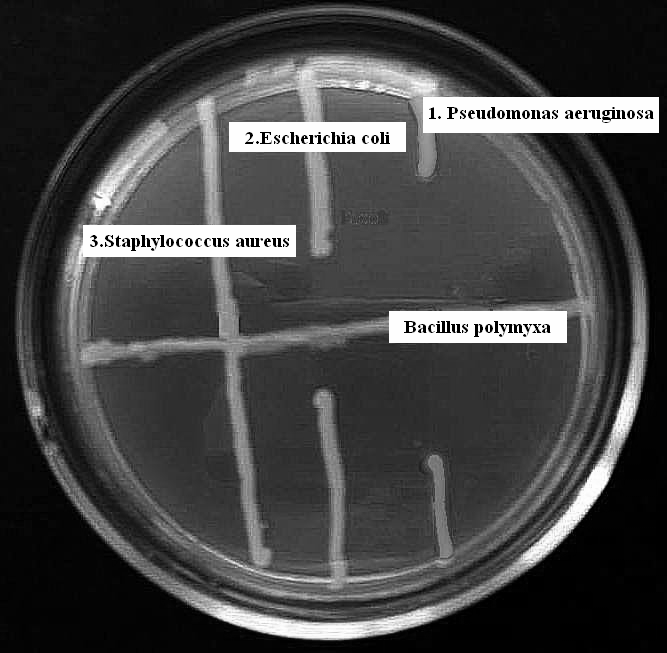
4►Выявление и регистрация антагонистического действия разных видов бактерий.
На чашку с МПА штрихом по диаметру засевается микроб-антагонист и перпендикулярно к нему тест-штаммы. Учет результатов проводится через сутки после посева. Наличие и степень антагонистического действия определяют по величине зон задержки роста тест-культур.
Штриховой посев Васillus polymyxa
Вывод: наибольшее антагонистическое действие выявлено к тест-штаммам (укажите виды)
P.aeruginosae, E.coli, нет антагонизма к S. aureus
