
HT_kur_lek
.pdfвибухонебезпечними. Бажано, щоб вони були дешевими та доступними. Нині використовують газоподібні, рідкі, тверді та змішані охолодні середовища.
3.1. Газоподібні середовища
До газоподібних охолодних середовищ належать атмосферне повітря та газові суміші – регульовані (РГС), модифіковані (МГС) та ін.
Найширше використовується атмосферне повітря. Його перевагами є доступність і дешевизна, а також менший вміст домішок, що можуть змінити смакові якості продукту. Крім того, повітря, як і всі газоподібні середовища, контактує з усією поверхнею продукту, рівномірно охолоджуючи її. Недоліками повітря як охолодного середовища є малий коефіцієнт тепловіддачі до поверхні, мала питома теплоємність, а отже, великі витрати.
Повітря холодильних камер містить пил, краплини води, мікроорганізми тощо. Пил разом з мікроорганізмами, що містяться на його поверхні, осідає на стіни камери, обладнання та продукти. Тому для зменшення бактеріального забруднення продуктів повітря слід фільтрувати.
Вологе повітря можна розглядати як бінарну суміш сухого повітря та водяної пари. До складу сухого повітря входять азот (78 %), кисень (21 %), аргон (0,9 %), вуглекислий газ (0,02–0,03 %), неон, гелій, водень та інші гази у невеликих
концентраціях. Вміст водяної пари характеризується різними показниками: |
|
||||||
Вологовміст повітря – це масовий вміст водяної пари у 1 кг сухого повітря: |
|
||||||
d = |
mпар |
= 0,622 |
pпар |
= 0,622 |
pпар |
, |
(6) |
mпов |
|
|
|||||
|
|
pпов |
B - pпар |
|
|||
де mпар, mпов – маси відповідно водяної пари та сухого повітря, кг, В – барометричний тиск, Па; рпар, pпов – парціальні тиски відповідно водяної пари та сухого повітря, Па.
Відносна вологість повітря – відношенням парціального тиску водяної пари у повітрі до тиску насичення водяної пари за даної температури.
|
|
|
|
f = |
pпар |
|
|
|
|
|
|
|
|
||||
|
|
|
|
|
. |
|
|
|
|
|
|
|
(7) |
||||
|
|
|
|
¢¢ |
|
|
|
|
|
|
|
||||||
|
|
|
|
|
|
|
|
pпар |
|
|
|
|
|
|
|
|
|
Густина вологого повітря визначається як сума мас сухого повітря та водяної |
|||||||||||||||||
пари у 1 м3 суміші: |
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
B |
æ |
|
|
1+ d |
ö |
|
æ |
|
|
1+ d |
ö |
|
||
r |
в.п |
= |
|
ç |
|
|
÷ |
= r |
ç |
|
|
÷. |
(8) |
||||
|
|
|
|
|
|
|
|
|
|||||||||
|
|
|
ç |
1 |
+1,61d |
÷ |
|
пов ç |
1 |
+1,61d |
÷ |
|
|||||
|
|
|
0,287T è |
ø |
|
è |
ø |
|
|||||||||
Питома теплоємність вологого повітря – це кількість теплоти, яку необхідно підвести до 1 кг сухого повітря, що еквівалентно (1+d) кг вологого повітря, для
нагрівання його на 1 К за сталого вологовмісту: |
|
свп = спов+ dспар = 1,006+1,87·d |
(9) |
де спар, спов – питомі теплоємності відповідно водяної пари та сухого повітря, кДж/(кг·К).
Питома ентальпія – кількість теплоти, що міститься у повітрі, віднесена до 1
21
кг сухого повітря. За початкову точку відліку приймають питому ентальпію сухого повітря при 0 °С. Питому ентальпію вологого повітря визначають за формулою
h = cповt+(r + cпарt)d = 1,006t + (2501+1,87t)d |
(10) |
Теплопровідність вологого повітря за температур –50...50 °С (d<0,04 кг/кг):
l = 0,024 + 0,8·10–4t |
(11) |
Для малих вологовмістів, характерних холодильній технології, |
динамічну |
в’язкість вологого повітря вважають такою самою, як і сухого і визначають з рівняння Созерленда:
m ×10 |
5 |
=1,72 |
397 |
æ |
T |
ö1,5 |
(12) |
|
|
ç |
|
÷ |
|||
|
T +124 |
273 |
|||||
|
|
|
è |
ø |
|
Для аналізу процесів оброблення вологого повітря використовують h–d- діаграму вологого повітря, що є графічною інтерпретацією рівняння (10). За нею можна визначити всі параметри повітря за будь-якими двома відомими.
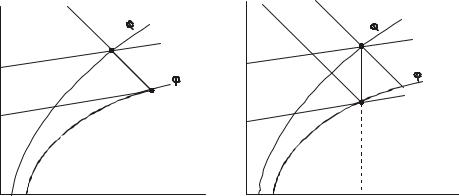
Під час випаровування води з вологої поверхні поглинається теплота випаровування r. Ця теплота відводитиметься від поверхні, тому у разі відсутності теплонадходжень волога поверхня матиме нижчу температуру, ніж суха, що перебуває у таких самих умовах теплообміну. Температура вологої поверхні називається температурою мокрого термометра. Різниця між температурою повітря та температурою мокрого термометра називається психрометричною різницею. Вона залежить від інтенсивності випаровування вологи і зростає у міру осушення повітря. Для визначення температури мокрого термометра користуються h–d-діаграмою (рис. 4, а). З точки 1, що характеризує початковий стан повітря слід провести ізоентальпу до перетину з лінією насичення. Температура у точці перетину (точка 2) буде температурою мокрого термометра.
Також можемо визначити для вологого повітря точку роси, тобто температуру, при якій повітря даного вологовмісту стане насиченим вологою (рис. 4, б). Для цього з точки 1, що характеризує початковий стан повітря, слід провести вертикальну пряму до перетину з лінією насичення. Температура у точці перетину (точка 2) буде температурою точки роси.
h |
h |
h |
|
1 |
1 |
|
|
|
|
t |
1 |
|
|
|
|
1 |
|
|
|
=100% |
|
t |
2 |
|
мт |
|
|
|
d |
|
|
а |
|
|
h |
|
|
|
|
1 |
|
|
|
h |
1 |
1 |
|
|
2 |
|
|
|
t |
|
|
|
|
|
|
|
|
|
1 |
|
|
|
|
|
|
|
|
0% |
|
|
|
0 |
|
|
|
|
=1 |
|
t |
|
2 |
|
|
р |
|
|
|
|
|
|
|
|
|
|
|
d1 |
|
d |
|
|
б |
|
|
Рис. 4. Визначення температури мокрого термометра (а) та температури точки роси (б) за h–d-діаграмою
22
Для зображення процесу нагрівання чи охолодження повітря за сталого вологовмісту слід провести вертикальну пряму до перетину з ізотермою кінцевої температури процесу.
Під час холодильного оброблення продуктів проходить багато вологообмінних процесів: дифузія вологи у повітрі, випаровування вологи з поверхні продуктів та її конденсація з вологого повітря, сублімація, взаємодія повітря з розсолом тощо. Для холодильної технології одним із найважливіших процесів вологообміну є всихання – випаровування води у вологе повітря з поверхні продукту. Витрату води, що випаровується, визначають за формулою
mп=β(pпр – p′′повϕпов)Fτ (13)
де β – коефіцієнт масовіддачі, віднесений до одиниці тиску, кг/(Па·м2·с); pпр – парціальний тиск водяної пари над поверхнею продукту, Па; p′′пов – тиск насичення водяної пари у повітрі, Па; ϕпов – відносна вологість повітря; F – площа поверхні, м2; τ – час, с.
Залежно від співвідношення між температурою продукту, що надходить до камери, та станом повітря у ній волога випаровуватиметься з поверхні продуктів (наприклад під час надходження продуктів у камеру охолодження) чи конденсуватиметься на ній (наприклад під час перенесення замороженого продукту до камери зберігання чи до теплішого приміщення, коли температура поверхні продукту нижча за температуру точки роси). На кількість вологи, що випаровується (конденсується), впливають величина вільної поверхні продуктів, способи їх укладання у штабелі, наявність упаковки.
До камери постійно надходить волога: за рахунок випаровування з продуктів, з навколишнього повітря, від людей. З іншого боку волога постійно конденсується чи десублімується на поверхні охолоджувальних пристроїв, температура яких нижча за температуру повітря. У камерах зберігання, як правило, конденсація вологи на приладах охолодження перевищує вологонадходження, тому для підтримання вологісного режиму слід зволожувати повітря у камері. Для цього у камеру подають тонко розпилену воду чи водяну пару. Оптимальна температура та відносна вологість повітря, що тісно пов’язані між собою, підтримуються за допомогою їх автоматичного регулювання. Можливий зворотний варіант – надходження вологи перевищує відведення. Тоді зайву вологу слід видаляти з камери, щоб не зростав вологовміст повітря.
Крім повітря використовують також інші гази та газові середовища. Вуглекислий газ (CO2) –застосовують за всіх методів холодильного оброблен-
ня, а також у поєднанні з іншими методами консервування. Він пригнічує розвиток мікроорганізмів (плісняви, бактерій). CO2 добре розчиняється у жирах та, не реагуючи з ними, витісняє кисень, уповільнюючи окиснення жирів. Після переміщення продукту до атмосферного повітря CO2 легко десорбується. CO2 використовують для охолодження та заморожування свіжого м’яса та м’ясопродуктів, птиці.
Газоподібний азот (N2) – утворюється після випаровування скрапленого азоту. Він так само, як і вуглекислий газ, витісняє з продукту кисень, уповільнює
23
окиснення та пригнічує життєдіяльність мікроорганізмів. Незважаючи на порівняно високу вартість, його застосовують у холодильному транспорті, а також для створення газових середовищ.
Регульовані газові середовища (РГС, за міжнародною термінологією СА – сontrolled atmosphere) – це газові суміші з різною концентрацією кисню, вуглекислого газу й азоту, склад яких підтримується сталим шляхом регулювання. Їх основу становить азот, концентрація якого в суміші 79–97%. РГС найчастіше використовується для зберігання фруктів та овочів.
Модифіковані газові середовища (МГС, попередньо приготовані, за міжнародною термінологією МА – modified atmosphere) – за складом подібні до РГС. Їх створюють всередині герметичної упаковки одноразово під час пакування, а. впродовж зберігання їх склад не змінюють. Такі середовища застосовують для короткотермінового зберігання м’ясних і молочних продуктів, хлібобулочних виробів найчастіше у роздрібному продажі.
Саморегульовані газові середовища (СГС, за міжнародною термінологією SCА
– self-controlled atmosphere) – створюються завдяки процесам життєдіяльності продуктів, зокрема диханню. Для цього використовують газоселективні мембрани, зокрема полімерні плівки. Такі середовища використовують для зберігання насамперед плодоовочевої продукції, а також сирів. У вітчизняній практиці через мале поширення попередньо приготованих модифікованих газових середовищ саморегульовані газові середовища також називають модифікованими (МГС).
3.2. Рідкі середовища
До рідких охолодних середовищ належать вода, водні розчини солей натрію, кальцію та магнію, гліколі, фреони, скраплені гази (насамперед азот). Їх основними перевагами порівняно з газовими середовищами є вищі теплоємність і теплопровідність, вищий коефіцієнт тепловіддачі до поверхні продукту. Охолодження здійснюється способом занурення чи зрошування.
Для охолодження найчастіше використовують льодяну воду (з температурою 0–1°С), охолоджену у спеціальних холодильних установках – чіллерах. Перевагами води є велика теплоємність (4,19 кДж/(кг·К)), дешевизна, менша, ніж у розчинів, корозійна активність, відсутність шкідливого впливу на більшість продуктів. Проте зниження температури нижче 0 °С призводить до замерзання води зі збільшенням її об’єму, через що можливе руйнування обладнання. Тому воду використовують лише при додатних температурах.
Льодоводяні суміші готують із води та подрібненого льоду. Перевагою льодоводяної суміші є те, що її температура (0 °С) не змінюється доти, доки не розплавиться лід. Таким чином забезпечується вища швидкість охолодження порівняно з водою. Лід для суміші виготовляють за допомогою льодогенераторів заздалегідь (акумулювання холоду) чи виморожують з потоку води (розсолу) та сколюють лід назад у потік. На шляху до теплообмінного апарата льодяна вода (розсіл) буде охолоджена до необхідних температур за рахунок танення льоду. Так можна ефективно охолодити молоко, пиво, сік тощо до температур 2–3°С і нижчих.
24
Суттєвих переваг можна досягти, якщо через канал теплообмінника рухається двофазна суміш “вода (розсіл) – лускоподібний лід”. При цьому з боку такої суміші коефіцієнт тепловіддачі становить 2000–4000 Вт/(м2·К) – значення, характерні для процесів безпосереднього кипіння холодоагентів. Крім того, температура холодоносія в теплообміннику залишається сталою. Недоліком такої системи є можливість утворення льодяних пробок у трубопроводах та теплообмінних каналах.
В охолоджених водних розчинах нижче від температури початку кристалізації води утворюються мікроскопічні кристали льоду, що не заважають транспортуванню двофазної льодорідинної суспензії трубопроводами. Такий холодоносій, що найчастіше називають айссларрі (ice-slurry), одержують із морської води, водних розчинів солей, гліколів, спиртів. Рідка фаза розділяє кристали льоду, що дає можливість уникнути утворення сніжних грудок і перекачувати суспензії, що містять до 60 % (за масою) льоду у вигляді кристалів розміром від 10 до 450 мкм. Частка льоду та розмір кристалів залежать від багатьох факторів, насамперед від конструкції льодогенератора, швидкості течії розчину, концентрації розчинених речовин, тривалості перебування кристалів у розчині, умов теплообміну тощо. За розрахунками теплопровідність і в'язкість айссларрі при частці льоду близько 15 % вищі від значень тих самих властивостей для однофазного розчину на 50%.
З використанням айссларрі як охолодного середовища чи холодоносія можна забезпечити у 3–5 разів більшу холодопродуктивність, ніж з використанням води чи розчинів, до 50 % зменшити діаметри відповідних трубопроводів, зменшити кількість холодоносія у холодильній системі, створити більш стабільні температурні режими холодопостачання. Такі середовища дають можливість підтримувати більш рівномірне температурне поле порівняно з грудковим льодом.
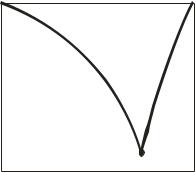
Для від’ємних температур використовують розчини солей (розсоли), що є подвійними системами, бо складаються з води та розчиненої солі. Їх стан визначається діаграмами стану (рис. 5).
t, оС 0
−10
−20
−30
−40
−50
−60
К |
р |
|
|
і |
|
|
|
л |
|
|
и |
|
о |
|
|
|
в |
|
|
|
|
а |
|
с |
|
|
в |
|
|
|
|
|
я |
|
|
|
и |
|
|
|
|
д |
|
н |
|
|
і |
|
|
|
|
л |
|
н |
|
|
е |
|
|
|
|
н |
|
е |
|
|
|
л |
|
|
|
н |
|
|
|
|
|
і |
|
|
|
я |
|
|
|
|
л |
|
д |
|
|
|
|
и |
|
|
ь |
|
в |
|
|
о |
|
а |
|
|
у |
||
|
|
д |
в |
|
|
|
|
||
|
|
|
и |
|
|
|
|
р |
|
|
|
К |
|
|
|
|
Кріогідратна точка |
||
0 |
10 |
20 |
30 |
40 |
50 |
60 |
|
Масовий вміст CaCl2 у воді, % |
|||||
Рис. 5. Діаграма стану розчину CaCl2
Під час охолодження розчину певної концентрації при досягненні температури, що відповідає кривій виділення льоду чи солі, з розчину починається виділення відповідного компонента. При цьому змінюватиметься концентрація
25
розчину. Якщо заморожувати розчин з концентрацією, нижчою за евтектичну, спочатку почнеться виділення льоду, при цьому концентрація рідкої фази розчину зростатиме, відповідно температура її кристалізації знижуватиметься. У разі заморожування розчину з концентрацією, вищою за евтектичну, з розчину виділятиметься сіль за рахунок зниження її розчинності, а концентрація рідкої фази зменшуватиметься. З досягненням температури кріогідратної точки відбудеться замерзання розчину у вигляді однорідної суміші обох компонентів, що називається евтектикою. Концентрацію у цій точці називають евтектичною, а розчин такої концентрації – евтектичним.
Для холодильного оброблення харчових продуктів використовують розчини солей, наведені у табл. 5.
Таблиця 5
Параметри евтектичних розчинів солей
Назва показника |
|
Розчин |
|
|
NaCl |
CaCl2 |
MgCl2 |
||
|
||||
Евтектична концентрація, % |
22,4 |
29,8 |
21,6 |
|
Температура замерзання, °С |
–21,2 |
–55 |
–33,6 |
Розчини є електролітами, тому мають високу корозійну активність, особливо на межі “метал–повітря–розсіл”. При цьому меншу корозійну активність мають розчини, приготовлені на основі дистильованої води, ніж на основі водопровідної (у декілька разів). Наявність аніонів хлору в присутності катіонів заліза, міді надає розсолам корозійних властивостей, при яких псуються деталі, виготовлені з міді, латуні і навіть із неіржавіючої сталі. Металеві поверхні піддаються точковій і виразковій корозії, швидкість якої може сягати 1,5 мм/рік, причому часто трапляється нерівномірність корозії трубопроводів, теплообмінного обладнання, особливо за виразкової корозії. Великої шкоди завдає електрохімічна корозія, зокрема за наявності електропровідного контакту системи циркуляції розсолу з ґрунтами під підприємством, де утворюються сильні, нерівномірні електричні поля та блукаючі електричні струми. Внаслідок дії різних видів корозії термін експлуатації окремих елементів холодильної установки зменшується. Для пригнічення корозійної активності в розсоли, крім основної солі, додають антикорозійні речовини – інгібітори, пасиватори (силікат натрію, хромова суміш та ін.). При цьому швидкість корозії зменшується до 0,1 мм/рік і менше.
Розсоли та антикорозійні добавки в них можуть бути токсичні чи небезпечні для довкілля. Для контролю витікання розсолів у довкілля до них додають різні барвники, частіше синтетичного походження. Слід контролювати чистоту солі, що закуповується для приготування розчину-холодоносія.
У разі контакту з продуктом, що має вищу температуру, ніж розчин, шар розсолу поблизу поверхні продукту відхиляється від кривої початку замерзання і відбувається дифузія солі у поверхневий шар продукту, що спричиняє погіршання смакових якостей продукту. Для уникнення цього продукт ізолюють від середовища
26
за допомогою металевих форм чи герметичної полімерної тари.
Гліколі – це жирні спирти, водні розчини яких мають низьку температуру замерзання. Вони менш агресивні до металів, але мають вищу в’язкість і нижчу теплопровідність. Розчини гліколів використовуються у системах швидкого заморожування упакованих продуктів.
Етиленгліколь – слабкоотруйна речовина, без запаху, змішується з водою у будь-яких співвідношеннях, температура замерзання чистого етиленгліколю – 17,5 °С, а його 70%-го розчину у воді –67,2 °С.
Пропіленгліколь – безбарвна густа рідина зі слабким характерним запахом, змішується з водою та етиловим спиртом, має гігроскопічні властивості, нетоксичний, використовується як харчова добавка (Е1520). Пропіленгліколь у водних розчинах не взаємодіє з металами. Водні розчини пропіленгліколю використовують у температурному діапазоні –50...–1 °С. У харчових виробництвах цей холодоносій виявився найбільш конкурентоспроможним у діапазоні температур –20...–1 °С. Пропіленгліколь є поверхнево-активною речовиною, сприяє вимиванню відкладень на стінках обладнання в розчин.
Для швидкого заморожування особливо цінних продуктів застосовують скраплені гази (кріорідини), найчастіше азот. Замороження здійснюють зрошуванням або зануренням у кріогенних швидкоморозильних апаратах. Низькі температури кипіння кріорідин та інтенсивна тепловіддача при цьому дають можливість швидко заморозити продукт з мінімальною втратою його якості. Проте значним недоліком кріорідин є їх висока вартість.
3.3. Тверді середовища.
Найчастіше у харчовій промисловості використовують водяний лід. Температура його плавлення за атмосферного тиску становить 0 °С, питома теплота плавлення – 335 кДж/кг, густина – 917 кг/м3, питома теплоємність – 2,1 кДж/(кг×К), теплопровідність – 2,3 Вт/(м·К). При замерзанні води її об’єм зростає на 9 %.
Природний лід заготовлюють шляхом випилювання великих блоків із водойм, наморожування на горизонтальних майданчиках, вирощування сталактитів. Його зберігають у льодосховищах з постійною чи тимчасовою теплоізоляцією. Штучний лід одержують за допомогою льодогенераторів, у яких заморожують очищену воду.
Форма, розмір, якість і спосіб отримання льоду залежать від його призначення. Матовий лід, приготований з питної води без оброблення, містить дрібні бульбашки повітря, що утворилися в процесі замерзання внаслідок десорбції з води. Прозорий лід (для охолодження напоїв) не містить бульбашок повітря. Під час його виготовлення форма продувається стисненим повітрям, що виділяє розчинене повітря з води і виносить з собою. Для охолодження птиці, риби, м’яса використовують лід з додаванням бактерицидних речовин, що зменшують обсіменіння продукту мікроорганізмами. У льодогенераторах виготовляють різні види льоду.
Трубчастий лід виготовляють у кожухотрубних льодогенераторах, у міжтрубному просторі яких кипить аміак, а до вертикальних труб через насадки подається вода, що плівкою стікає донизу і частково замерзає. Вода, що не замерзла, поверта-
27
ється до верхнього резервуара. Завдяки безперервній циркуляції з води видаляється повітря і лід утворюється у вигляді прозорих циліндрів з товщиною стінки 4–8 мм, які після відтанення сповзають донизу. Їх розрізають на куски потрібної довжини.
Лускоподібний лід виготовляють у барабанних льодогенераторах. Вони являють собою охолоджуваний барабан, що обертається, на який розпилюється вода. На поверхні барабана швидко утворюється шар тонкого льоду, який зрізається ножем. Такий лід, що має вигляд тонких пластинок, використовують для охолодження риби, м’яса, ковбасних виробів, деяких плодів та овочів.
Сніговий лід виготовляють розпилюванням води у посудині, при низькій температурі. Його використовують у тих самих випадках, що й лускоподібний.
Льодосоляні суміші давно використовують для одержання температур нижче 0 °С. Змішуванням водяного льоду та солей (NaCl, CaCl2) у певних співвідношеннях можна досягти температур плавлення суміші аж до кріогідратної точки. Під час контакту льодосоляної суміші з неупакованим продуктом поверхневі шари продукту просолюються, що змінює його смак і стимулює окиснення жирів. Для уникнення цього використовують заморожені евтектичні розчини у металевих формах. Їх розміщують у охолоджуваному об’ємі, а після танення льоду та отеплення знову заморожують.
Сухий лід – це твердий діоксид вуглецю. Температура його сублімації за атмосферного тиску становить –78,9°С; теплота сублімації 574 кДж/кг , а густина 1400–1500 кг/м3. За тиску нижче 0,528 МПа він може перебувати лише у твердому та газоподібному станах. Під час підведення теплоти до сухого льоду за атмосферного тиску йде процес його переходу одразу до газоподібного стану (сублімація). Сухий лід найчастіше отримують шляхом дроселювання газоподібного СО2 з тиску 2–3 МПа до атмосферного. Кристали сухого льоду з температурою – 79 °С відділяють від газу і пресують у вигляді блоків.
Одиниця об’єму сухого льоду дає втричі більшу холодопродуктивність, ніж водяного, що дає можливість ефективніше використовувати об’єм охолоджуваних приміщень чи тари. Інші його переваги перед водним льодом: можливість досягнення нижчої температури, відсутність рідкої фази в процесі холодильного оброблення, підвищення вмісту СО2 у атмосфері камери, що пригнічує життєдіяльність мікроорганізмів і уповільнює окиснення продукту. Сухий лід кладуть зверху та між упаковками продукту під час зберігання, перевезення та продажу морозива, ягід, фруктів. У безмашинних системах охолодження використовують металеві контейнери, наповнені сухим льодом, причому газоподібний СО2, що утворюється, відводять до камери, пригнічуючи діяльність мікроорганізмів.
У швидкоморозильних апаратах використовують металеві плити, всередині яких циркулює холодоагент. Найчастіше використовують сталь, чавун, алюміній та його сплави, мідь. Перевагами металів, як охолодних середовищ, є високі коефіцієнти теплота температуропровідності, хімічна стійкість щодо продуктів, легкість механічного оброблення. Основний недолік – складність забезпечення рівномірного контакту з усією поверхнею продукту.
Під час заморожування ягід, овочів, напівфабрикатів у киплячому шарі як
28
охолодне середовище іноді використовують дрібнодисперсні середовища: подрібнений лід, дрібні полімерні кульки, а також спеціальні суміші (наприклад, суміш манної крупи, цукру, солі та подрібненого льоду). Таке середовище під впливом потоку повітря, що з певною швидкістю продувається крізь нього знизу догори, переходить у завислий стан і утворює киплячий шар, крізь який рухається продукт. У цьому шарі теплообмін відбувається значно інтенсивніше, ніж у повітрі.
3.4. Прилади для вимірювання та контролю параметрів охолодних середовищ і продуктів
Для контролю температури охолодного середовища та продуктів застосовують рідинні, металеві, електричні та електронні термометри, а також термометри на рідких кристалах. Для реєстрації температури впродовж зберігання чи транспортування використовують термографи та термоіндикатори.
Термографи застосовують для безперервної графічної реєстрації температури у камерах зберігання. Вони складаються з термометра (датчика) та реєстраційного пристрою. Термоіндикатори призначені лише для фіксації факту підвищення температури понад заданий рівень (наприклад під час транспортування).
Відносна вологість повітря вимірюється психрометрами та гігрометрами. Психрометричний метод ґрунтується на залежності швидкості випаровування
води з поверхні від відносної вологості повітря. Психрометр складається з сухого та мокрого термометрів. У мокрого термометра кулька обмотана змоченою у воді тканиною (марля, батист). У разі зниження відносної вологості за рахунок прискорення випаровування води та інтенсивнішого відведення теплоти від кульки термометр показуватиме нижчу температуру. За температурою сухого термометра та різницею показань двох термометрів за таблицями визначають відносну вологість повітря. Психрометри використовують при температурах вище –5 °С. Для прискорення вимірювань використовують психрометр з примусовою циркуляцією повітря
– аспіраційний психрометр Ассмана, у якому кульки термометра обдуваються повітрям за допомогою вентилятора з пружинним чи електричним приводом.
Гігрометричний метод дає змогу визначити відносну вологість повітря у інтервалі температур –60...+40 °С. У сорбційних гігрометрах чутливий елемент змінює свої властивості (наприклад знежирена волосина подовжується або сіль змінює електричний опір) у разі зміни вологовмісту за рахунок сорбування вологи з повітря. Інтенсивність сорбування залежить від відносної вологості повітря. Зміна властивостей фіксується безпосередньо (волосяні гігрометри) або перетворюється на електричний сигнал і виводиться на шкалу, проградуйовану в одиницях відносної вологості. Для безперервної реєстрації відносної вологості у камерах зберігання використовують гігрографи, у яких наявний реєструвальний пристрій.
Для вимірювання швидкості руху повітря 1–50 м/с призначені чашкові анемометри, а крильчасті – 0,1–4 м/с. Принцип їх дії подібний: вимірюється частота обертання крильчатки потоком повітря, що пропорційна швидкості руху повітря.
Для дистанційного контролю використовують електроанемометри. Принцип їх дії ґрунтується на охолодженні потоком повітря провідника, що нагрівається
29
сталим електричним струмом. Температуру провідника вимірюють за допомогою термопари чи визначають за його опором. Вона знижуватиметься зі зростанням швидкості руху повітря.
Переносні напівпровідникові електротермоанемометри, у яких роль датчика відіграє напівпровідниковий термоопір, дають змогу швидко та з високою точністю визначити температуру та малі швидкості руху повітря.
3.5. Допоміжні засоби для холодильного оброблення та зберігання
Для збереження якості, зниження втрат і збільшення терміну зберігання продуктів застосовують допоміжні засоби: ультрафіолетове та іонізуюче опромінення, зниження тиску, харчові покриття, упаковку та ін.
Ультрафіолетове опромінення значно подовжує терміни зберігання охолоджених продуктів (м’яса, яєць, напівкопчених і копчених ковбасних виробів, сирів, цитрусових плодів та ін.). Під його впливом зростання мікрофлори різко сповільнюється (бактеріостатичний ефект), що залежить від дози опромінення та стану середовища. Зі зниженням температури тривалість цього ефекту зростає.
Іонізуюче опромінення завдяки високій енергії здатне викликати іонізацію атомів і молекул. При цьому в продуктах виникають хімічні перетворення, пов’язані насамперед з іонізацією води, утворенням вільних радикалів з високою хімічною активністю, що призводять до змін у клітинах. За певної дози ІВ пригнічує життєдіяльність мікроорганізмів.
Антисептики пригнічують мікроорганізми. Надходячи до клітини, вони взаємодіють з білками протоплазми, що призводить до загибелі клітини. Важливо, щоб антисептики були нешкідливими для людини і мінімально змінювали споживчі властивості продуктів. Використовують сорбінову та бензойну кислоти, перекис водню, діоксид сірки та ін.
Озон (О3) завдяки високій хімічній активності окиснює ароматичні речовини та призводить до загибелі мікроорганізмів. Оброблення озоном застосовують для дезінфекції та дезодорації повітря (знищення неприємних запахів), сухої, холодної дезінфекції технологічних приміщень, складів, холодильних камер, технологічного обладнання (місткостей і трубопроводів), знищення плісняви. У разі дезінфекції озонуванням приблизно в п’ять разів скорочується тривалість простоювання камер порівняно з “мокрою” дезінфекцією, скорочується трудомісткість. Озонування не потребує розморожування холодильних камер, застосування хлоровмісних засобів.
Надзвичайно важливу роль у процесі зберігання відіграє упаковка продукту. Її наявність дає можливість усунути або зменшити контакт продукту з навколишнім повітрям. Упаковка є основним джерелом інформації про продукт для споживача. Упакований продукт має кращий вигляд, зручніший для перевезень і продажу.
Різноманітність харчових продуктів спричиняє різноманітність видів упаковки та різні вимоги до неї. Для упакування охолоджених і заморожених продуктів широко використовують папір і картон або лотки з пресованої целюлози (для яєць, деяких фруктів). Папір легко обробляти та утилізувати, наносити інформацію, упаковка має привабливий зовнішній вигляд та низьку вартість. Папір як
30
