
- •1.1. Еволюція хімії лікарських засобів
- •1.2. Предмет та об’єкти дисципліни «Органічний синтез лікарських засобів»
- •2.1. Сучасні вимоги до лікарських препаратів
- •2.2. Стратегія органічного синтезу ЛР
- •2.3. Загальні принципи комп’ютерного пошуку та конструювання ЛЗ
- •2.4. Схема розробки нового лікарського препарату
- •2.5. Особливості органічного синтезу лікарських субстанцій
- •3.1 Вплив функціональних груп на біологічну активність молекули
- •3.1.1. Вплив алкільних груп
- •3.1.2. Ефект галогенів
- •3.1.3. Вплив гідроксильних груп
- •3.1.5. Вплив аміногруп.
- •3.1.6. Дія кислотних угруповань
- •3.1.7. Вплив ненасичених зв’язків
- •5.1.1. Галогенпохідні в якості засобів для наркозу
- •5.1.2. Дихлороетиламінний фармакофор та його роль в створенні протипухлинних засобів
- •Етери та естери
- •5.3. Альдегіди та кислоти. Вітаміни F и В15
- •6.2. Пептиди
- •6.4. Похідні γ-аміномасляної кислоти.
- •6.5. Інші амінокислоти у фармацевтичних препаратах
- •7.1. Заміщені циклогексани
- •7.2. Камфора
- •7.3. Похідні адамантану
- •7.4. Стероїди з циклопентафенантреновою структурою. Вітамін D
- •8.1. Антисептики фенольного ряду
- •8.2. Аміноспирти ароматичного ряду
- •8.2.1. Аміноалкілбензени, похідні амфетаміну
- •8.2.2. Синтез адреноблокаторів фенольного ряду (анаприлін)
- •8.2.3. Похідні п-амінофенолу
- •8.3. Похідні бензенової та саліцилової кислот
- •8.4. Похідні п-амінобензенових кислот
- •8.4.1. Протитуберкульозні засоби – похідні п-амінобензенової кислоти
- •8.4.2. Анестетики на основі п-амінобензенової кислоти
- •8.5. Похідні сульфанілової кислоти
- •8.6. Антигістамінні препарати ряду діарилметану
- •8.7. Оксопохідні нафталену
- •9.1.1. Синтез протипухлинних речовин групи азирідину та оксирану
- •9.1.2. Антибіотики, що містять чотиричленне азетидинове ядро
- •9.2. Лікарські речовини на основі п'ятичленних гетероциклів
- •9.2.1. Аскорбінова кислота
- •9.2.2. Антибактеріальні нітрофурани
- •9.2.3. Противиразкові препарати з фурановим фрагментом (ранітидин, лупітидин)
- •9.2.4. Похідні піролу та індолу
- •9.2.5. Похідні піролідину в якості ноотропних та антигіпертензивних засобів
- •9.2.6. Похідні імідазолу та бензімідазолу
- •9.2.7. Похідні піразолу
- •9.2.8. Похідні тіазолу. Вітамін В1
- •9.3. Похідні шестичленних гетероциклів
- •9.3.1. Похідні бензопірану
- •9.3.2. Токофероли (вітамини групи Е)
- •9.3.3. Похідні піридину, хіноліну та ізохіноліну
- •9.3.4. Похідні піримідину
- •Похідні піримідинів з антивірусною (антиСНІД-овою) активністю
- •9.3.5. Похідні бензотіазинів.
- •9.3.6. Пуринові основи
- •9.4. Синтез лікарських засобів з семичленним гетероциклом. Похідні дибензодіазепінового ряду
- •9.5. Лікарські засоби – похідних біциклооктану.

23
За останні 30 років в біохімії відбулися події, які змінили уявлення про функціонування самих різних біологічних систем. Було виявлено, що оксид нітрогену (ІІ) – NO є одним з універсальних і необхідних регуляторів функцій метаболізму в організмі людини, а також унікальною сигнальною молекулою, за допомогою якої клітини можуть обмінюватися інформацією. Оксид нітрогену (ІІ) бере участь у регуляції тонусу кровоносних судин, пригнічує
агрегацію |
тромбоцитів та |
їх адгезію на |
стінках, функціонуєсудин |
в |
центральній |
і вегетативній |
нервовій системах, регулює діяльність органів |
||
дихання, шлунково-кишкового тракту та сечостатевої системи. NO бере участь у деструкції та метаболізмі ферментів, які містять залізо, кобальт, марганець, цинк.
Широта біологічної активності оксиду нітрогену(ІІ) дуже велика. В 1992 році в журналі«Science» NO було названо молекулою року, а в 1998 році американські фармакологи Ф. Мюрад, Л. Ж. Ігнарро і .Р Фарчготт були удостоєні Нобелівської премії в галузі медицини та фізіології за з'ясування ролі NO у функціонуванні кровоносної системи. Кількість оглядових і оригінальних
публікацій, присвячених ролі моноксиду нітрогену в організмі зростає
лавиноподібно. |
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
Щодо сполук з нітрота |
нітрозогрупами, зазначимо, що аліфатичні |
|
||||||||||||||||||||
нітрити та нітрати викликають розширення судин, і тому застосовуються для |
|
|||||||||||||||||||||
зниження кров'яного тиску. Цей ефект послаблюється разом зі зменшенням |
|
|||||||||||||||||||||
довжини вуглецевого ланцюга від амілнітриту до метилнітриту. Всі нітрити |
|
|||||||||||||||||||||
діють однаково; при цьому вторинні і третинні нітрити діють сильніше, ніж |
|
|||||||||||||||||||||
первинні, ймовірно, внаслідок |
того, що |
вони |
легше |
гідролізуються |
з |
|||||||||||||||||
утворенням спирту і нітратної кислоти. Аналогічно діють |
також |
естери |
|
|||||||||||||||||||
нітратної кислоти: нітрогліцерин, нітросорбіт, та ін. |
|
|
|
|
|
|
||||||||||||||||
Введення |
нітрогрупи в |
ароматичні сполуки зазвичай підвищує їх |
||||||||||||||||||||
токсичність: наприклад, нітробензен, нітронафтол і нітротіофен токсичніші, ніж |
|
|||||||||||||||||||||
вихідні сполуки, що не містять нітрогрупи. |
|
|
|
|
|
|
|
|
|
|
|
|
|
|||||||||
3.1.5. Вплив аміногруп. |
|
|
|
|
|
|
|
|
|
|
|
|
|
|
||||||||
Дослідженню |
|
впливу |
аміногрупи, введеної |
|
|
в |
бензенове |
або |
||||||||||||||
гетероциклічне ядро присвячено багато робіт. Це пов’язано |
з тим, що ці |
|
||||||||||||||||||||
сполуки створили |
основу |
для одержання цілих класів жарознижуючих |
||||||||||||||||||||
(фенацетин, парацетамол), антибактеріальних (сульфаніламідні |
препарати) |
та |
|
|||||||||||||||||||
знеболювальних |
ЛП (місцеві |
анестетики – похідні |
|
пара-амінобензенової |
|
|||||||||||||||||
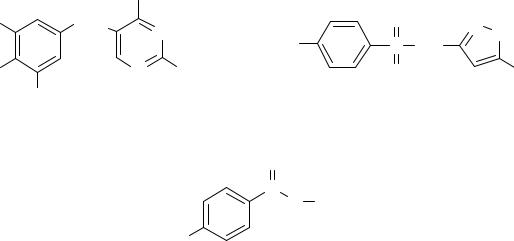
кислоти, анестезин, новокаїн, тощо): |
|
|
|
|
|
|
|
|
|
|
|
|
|
|||||||||
C2H5 |
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
||
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
||
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
||
O |
|
|
|
|
|
|
|
NHCOCH3 |
HO |
|
|
|
|
NHCOCH |
|
|
||||||
|
|
|
|
|
|
|
|
|
||||||||||||||
|
|
|
|
|
|
|
|
|
|
|
|
|||||||||||
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
3 |
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
||||||||
|
Фенацетин |
|
|
Парацетамол |
|
|
|
|||||||||||||||
|
|
|
|
|
24 |
CH3O |
NH2 |
O |
|
|
|
CH2 |
N |
N |
O |
||
|
|
H2N |
S |
NH |
|
CH3O |
N |
NH2 |
O |
|
CH3 |
|
OCH3 |
|
|
|
|
|
Триметоприм |
|
Сульфоксазол |
|
|
O
C
O CH3
H2N
Анестезин
Введення другої аміногрупи в ароматичне кільце, як правило, веде до значного зростання токсичності.
Речовини, що містять у своїй молекулі третинний атом Нітрогену, часто є малотоксичними або зовсім нетоксичними. Цікаво, що в багатьох випадках при
перетворенні |
третинного |
атома |
Нітрогену |
у |
вторинний |
утворюють |
високоактивні |
сполуки. А |
при перетворенні сполук з |
третинним |
атомом |
||
Нітрогену в четвертинні амонієві основи у них з'являються курареподібні властивості.
3.1.6. Дія кислотних угруповань
Введення в молекулу кислотних угруповань часто викликає зменшення, або повне зникнення токсичності, інколи ця закономірність стосується і біологічної активності загалом. Фенол С6Н5ОН отруйний, але фенілсульфатна
кислота СН ОSО ОН майже нешкідлива. Морфін володіє дуже високою
6 5 2
біологічною активністю, морфінсульфатна кислота абсолютно позбавлена активності. Анілін, токсичність якого вища, ніж у бензену, стає практично
нешкідливим |
при |
приєднанні |
до |
нього |
карбоксильної; парагрупи- |
||
амінобензенова |
кислота |
добре |
переноситься |
організмом, є |
ендогенною |
||
сполукою. Присутність карбоксильної групи в молекулі бензену знижує токсичність. Препарати бензенової кислоти, зокрема її натрієва сіль, мають низьку токсичність і застосовуються в якості лікарського засобу.
3.1.7. Вплив ненасичених зв’язків
Ненасичені сполуки зазвичай бувають більш токсичними, ніж їх насичені аналоги, що пов’язано з їх більш високою хімічною реакційною здатністю.
Наприклад, пропіловий спирт СНСН СН ОН виявляє слабку наркотичну дію,
3 2 2
але в помірних дозах він не отруйний. У той же час аліловий спирт СН2=СНСН2ОН є дуже токсичною речовиною, що не виявляє наркотичної дії взагалі. Необхідно відзначити, що висока фунгіцидна активність ненасичених
25
спиртів використовується в антимікотичних препаратах, які здатні руйнувати цитоплазматичні мембрани грибків.
3.2. Зв'язок між будовою і біологічною активністю
Підбиваючи підсумок, можна зробити висновок, що широкі узагальнення щодо впливу будови речовини на її біологічну активність виявилися корисними при синтезі багатьох ЛЗ, і, безсумнівно, виявляться корисними в майбутньому для передбачення очікуваного характеру активності синтезованих сполук. З іншого боку, не можна заперечувати існування багатьох виключень з наведених
залежностей, що |
пов'язують |
біологічну |
активність |
з |
хімічною будовою |
||||
молекул. |
|
|
|
|
|
|
|
|
|
На |
сьогодні |
виявлено |
ряд фармакофорних , |
групвведення |
яких |
в |
|||
молекулу потенційного лікарського засобу«прищеплює» йому потрібний вид |
|
||||||||
активності. |
Наприклад, наявність фенольного |
угруповання |
може |
надавати |
|||||
речовині антисептичну властивість. Введення карбамідного фрагмента сприяє |
|
||||||||
прояву снодійного ефекту, тощо. |
|
|
|
|
|
|
|
||
Особливістю |
біологічних |
систем |
є , |
щоте вони |
не |
розрізняють |
в |
||
синтетичних ЛЗ ароматичні та гетероциклічні кільця. Таким чином, заміна одного плаского ядра на інше(наприклад бензенового на піридинове, або фуранового на тіофенове або пірольне мало позначається на корисній дії). Тому подібні заміни можуть бути частиною стратегії при дизайні синтетичних
лікарських |
речовин. Наприклад, для |
зміни |
полярності |
молекули, введення |
|
|||
різних замісників в ароматичне кільце(ця задача полегшується |
у |
випадку |
||||||
заміни бензенового кільця на гетероцикл), з метою |
посилення |
взаємодії |
||||||
лікарської речовини зі специфічним рецептором, поліпшення фармакологічної |
|
|||||||
дії препарату, тощо. |
|
|
|
|
|
|
|
|
Зауважимо, що |
застосування |
виявлених |
закономірностей |
не |
||||
абсолютним |
і часто не |
може забезпечити |
очікуваного |
ефекту. Тим |
не |
менш, |
|
|
спрямований синтез лікарських препаратів із заданими властивостями є на сьогоднішній день одним з найбільш пріоритетних напрямків сучасної теоретичної та синтетичної органічної хімії.
3.3. Залежність фармакологічної дії ЛЗ від хімічних та фізичних властивостей
На сьогоднішній день не виникає сумнівів, що саме хімічна просторова будова речовини визначає наявність у неї біологічної активності. Проте, хімічна структура молекули не є єдиним фактором, що визначає фармацевтичну активність ЛЗ. Дуже важливо, щоб лікарська речовина потрапила до місця дії в організмі. Більшість лікарських речовин повинні добре розчинятися у ,воді тому, що вони переносяться в організмі, головним чином, током крові. Також важливою є висока ліпофільність(розчинність в жирах) і здатність проникати
через клітинні мембрани, щоб впливати на біохімічні |
процеси метаболізму. |
Препарати, що діють на центральну нервову |
систему, повинні вільно |
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
26 |
|
переходити з крові в спинномозкову |
рідину |
та, |
тобтомозок |
долати |
|
|||||||||||||||
гематоенцефалічний бар'єр, що захищає мозок від проникнення в нього |
|
|||||||||||||||||||
чужорідних речовин, розчинних у крові. Іншим бар'єром для проникнення |
|
|||||||||||||||||||
лікарських речовин з крові до тканин органу-мішені є стінки капілярів. Для |
|
|||||||||||||||||||
більшості лікарських речовин не дуже високої молекулярної маси цей бар'єр |
|
|||||||||||||||||||
переборний. Існує ще один бар'єр– плацентарний, що відокремлює організм |
|
|||||||||||||||||||
матері від плоду. Він, зазвичай, легко проникний для лікарських речовин, а це |
|
|||||||||||||||||||
небезпечно. |
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
||
|
В |
цілому, |
лікарська |
молекула, |
крім основної |
фармакофорної |
групи, |
|
||||||||||||
повинна |
містити гідрофільні та(або) ліпофільні фрагменти, |
|
що |
сприяють |
|
|||||||||||||||
перенесенню її до відповідної системиорганізму. Розчинність має суттєвий |
|
|||||||||||||||||||
вплив на процес всмоктування ЛЗ. Досліджено загальні закономірності впливу |
|
|||||||||||||||||||
різних радикалів на гідрота ліпофільність молекул ЛЗ. Відомо, що розчинність |
|
|||||||||||||||||||
у |
воді |
|
зменшується |
в |
наступному |
ряду |
|
в |
|
залежності |
від |
н |
||||||||
функціональних |
груп: карбоксильна > гідроксильна > карбонільна > аміно- |
> |
|
|||||||||||||||||
амідо- > |
нижчі |
алкіли > |
вищі алкіли > |
феніл-. Так, |
|
введення в |
структуру |
|
||||||||||||
фенольних |
угруповань, |
карбоксильних |
чи |
сульфогрупп, основного |
|
або |
|
|||||||||||||
амонійного |
атома |
Нітрогену(четвертинна |
сіль) |
покращує |
розчинність |
|
||||||||||||||
органічної молекули у воді, змінює її основність або кислотність, і, як наслідок, |
|
|||||||||||||||||||
підсилює |
її |
дію. Наявність н-алкільних |
ланцюгів, їх |
подовження, |
а |
також |
|
|||||||||||||
введення |
галогенів, навпаки, підвищує |
ліпофильность |
лікарських |
речовин |
|
|||||||||||||||
(розчинність в жирових тканинах, які можуть служити лікарським депо), |
|
|||||||||||||||||||
полегшує їх проходження через біологічні мембрани організму. Розгалужені |
|
|||||||||||||||||||
алкільні |
замісники та наявність атомів галогенів ускладнюють метаболізм |
|
||||||||||||||||||
(зокрема |
біоокиснення) |
лікарських |
речовин. |
Циклоалкільні |
угруповання |
|
||||||||||||||
покращують зв’язок з біорецептором за рахунок Ван-дер-ваальсових сил. |
|
|
|
|||||||||||||||||
|
Використання лікарських речовин з спиртовими або карбоксильними |
|
||||||||||||||||||
групами у вигляді етерів або естерів змінює полярність молекули лікарської |
|
|||||||||||||||||||
речовини, |
покращує |
|
прояв |
фармакологічної |
активності |
та |
уповільнює |
|||||||||||||
біодекарбоксилювання. |
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
||||
|
Ще |
|
одним |
з |
|
факторів |
впливу |
на |
|
фармакологічну |
|
активність |
||||||||
молекулярна маса речовини. Відомо, що аліфатичні спирти, вуглеводні та деякі |
|
|||||||||||||||||||
інші сполуки знижують свою активність зі збільшенням молекулярної маси. |
|
|
||||||||||||||||||
|
При виготовленні ЛЗ зважають також на дисперсність речовин, а також |
|
||||||||||||||||||
на природу допоміжних речовин у препараті |
|
|
|
|
|
|
|
|
|
|
||||||||||
|
Сучасні методи дослідження дозволяють врахувати наведені вище факти |
|
||||||||||||||||||
при |
конструюванні лікарського |
препарату, |
вводячи |
відповідні |
хімічні |
|
||||||||||||||
угрупування в потенційну лікарську речовину. |
|
|
|
|
|
|
|
|
|
|
||||||||||
|
3.4. Вплив оптичної активності на фармакологічну активність |
|
|
|
||||||||||||||||
|
Однією з причин різної фармакологічної активності є оптична |
ізомерія |
|
|||||||||||||||||
ЛЗ. Приблизно 40%-ів синтетичних лікарських речовин мають хоч би один |
|
|||||||||||||||||||
хіральний атом Карбону, проте, лише 15%-ів з них застосовуються в формі |
|
|||||||||||||||||||
одного |
енантіомера (інші |
у |
вигляді |
рацематів |
|
або |
діастереомерів). Що |
|
||||||||||||
|
|
|
|
|
|
|
|
|
|
|
27 |
|
стосується природних ЛР, майже всі вони використовуються у вигляді одного |
|
|||||||||||
енантіомера. |
|
|
|
|
|
|
|
|
|
|
|
|
В більшості випадків, енантіомери мають різну біологічну активність. Це |
|
|||||||||||
пояснюється тим, що кожен рецептор та молекула ЛР повинні відповідати один |
|
|||||||||||
одному |
за |
просторовою структурою(принцип |
ключ – замок). Відомо, що |
|
||||||||
L-амінокислоти при дії стереоспецифічних транспортних мембранних систем |
|
|||||||||||
можуть потрапити у внутрішню частину клітин. Їх концентрація в клітині при |
|
|||||||||||
цьому у 500 |
разів перевищує |
концентрацію |
у |
навколишньому |
середовищі. |
|
||||||
D-Амінокислоти не транспортуються цими системами. Лише L-амінокислоти є |
|
|||||||||||
поживними речовинами, в той час як їх D-антиподи такої властивості не мають. |
|
|||||||||||
Тому в якості ЛЗ використовують самеL-ізомери амінокислот. Наприклад, |
|
|||||||||||
лише L(-)-ізомер засобу Метилдопа має гіпотензивний ефект. Така сама |
|
|||||||||||
закономірність притаманна й |
іншим |
синтетичним. |
УЛЗ протиракового |
|
||||||||
препарата |
сарколізину |
активною |
є |
тільки |
одна |
лівообертаюча, |
форм |
|||||
правообертаюча лікувальної дії не має. |
|
|
|
|
|
|
|
|
||||
Анальгетик морфін існує у вигляді16 оптичних ізомерів. Усі вони були |
|
|||||||||||
одержані |
у |
чистому |
вигляді |
та досліджені. Виявилось, |
що |
морфін, який |
|
|||||
міститься у рослинній сировині, є одним з лівообертаючих ізомерів. Одержаний |
|
|||||||||||
синтетично |
правообертаючий |
морфін |
не |
мав |
жодних |
лікувальних |
||||||
наркотичних властивостей. Алкалоїд D-тубокурарин має сильну знеболювальну |
|
|||||||||||
дію, в той час як L-форма малоактивна. |
|
|
|
|
|
|
|
|
||||
Наприкінці 1960-х років виявилось, що застосування снодійного засобу |
|
|||||||||||
талідоміду вагітними жінками викликало каліцтва у їх новонароджених дітей. |
|
|||||||||||
Пізніше було з’ясовано, що препарат застосовувався в рацемічній формі, в якій один енантіомер мав снодійну дію та не мав токсичності по відношенню до плода, а інший мав тератогенну токсичність (викликав каліцтва у плода).
При створенні нових лікарських речовин, що мають хіральні центри, слід мати на увазі, що різні енантіомери можуть мати різну і навіть протилежну біологічну активність. Використання сучасних технологій синтезу оптично активних речовин дозволить отримати препарати, що мають найбільшу ефективність при найменшій токсичності.
Контрольні запитання та завдання
1.Що таке функціональна група? Яку роль виконують функціональні групи у створенні ЛЗ?
2.Як змінюється біологічна активність молекули при введенні до неї атомів галогену? Окремо охарактеризуйте вплив атому флуору.
3.Як впливає наявність гідроксильних груп в молекулі на її біологічну активність?
4.Як впливає наявність нітрота нітрозо-груп в молекулі на її біологічну активність? Які функції виконує оксид нітрогену (ІІ) в організмі?
5.Як впливає наявність аміногруп в молекулі на її біологічну активність? Як змінюється токсичність молекули при введені аміногрупи?
6.Наведіть приклади, що доводять вплив оптичної активності на біологічну активність молекул.
28
4. КЛАСИФІКАЦІЯ ЛІКАРСЬКИХ ПРЕПАРАТІВ. ОСНОВНІ ГРУПИ ЛІКАРСЬКИХ ПРЕПАРАТІВ
Проблема класифікації ліків є дуже |
важлив, оскількию |
створення |
||||||
порядку |
в |
такому |
різноманітті |
ліків |
необхідно |
як |
для |
раціональн |
застосування існуючих, |
так і створення нових лікарських засобів. |
|
|
|
||||
Існує три основних типи класифікації лікарських речовин: |
|
|
|
|||||
1)за лікувальною дією;
2)за джерелами отримання;
3)за хімічною будовою.
За лікувальною дією лікарські речовини поділяють на три групи– хіміотерапевтичні, нейрофармакологічні та регуляторні.
До хіміотерапевтичних відносять протиінфекційні лікарські речовини: антивірусні, антимікробні (антибіотики, антисептики), антитуберкульозні, антималярійні, фунгіцидні, протипухлинні, антигельмінтні препарати.
До нейрофармакологічної групи включають лікарські речовини, що діють на центральну нервову систему (наркотичні знеболюючі засоби, снодійні та інші психотропні препарати) і речовини, що діють на периферійну нервову систему (наприклад, місцеві анестетики).
Група регуляторних лікарських речовин включає вітаміни, гормони,
метаболіти |
та |
антиметаболіти(речовини, |
що |
регулюють |
активність |
||||||||
ферментних, гормональних, імунних і генних систем). |
|
|
|
|
|
||||||||
За джерелами отримання лікарські речовини поділяють |
на синтетичні |
||||||||||||
(складають |
близько 70%-ів |
усіх |
лікарських |
речовин), апівсинтетичні |
|||||||||
(отримують з природних речовин шляхом їх хімічної модифікації, наприклад, |
|||||||||||||
антибіотики |
цефалоспоринового |
та |
пеніцилінового ) |
рядів природні |
|||||||||
(наприклад, алкалоїди, вітаміни, гормональні речовини та ін.). |
|
|
|
|
|||||||||
За |
хімічною |
будовою лікарські речовини |
поділяють |
на |
неорганічні |
||||||||
(кислоти, основи, солі, оксиди, комплексні сполуки) та органічні речовини. В |
|||||||||||||
свою чергу, органічні |
речовини |
класифікують |
на |
похідні |
аліфатичного, |
||||||||
аліциклічного, ароматичного та гетероциклічного рядів. У рядах ЛР діляться на |
|||||||||||||
класи, ґрунтуючись на наявності тих чи інших функціональних |
груп та |
||||||||||||
замісників. Гетероциклічні сполуки поділяють в залежності від типу основного |
|||||||||||||
гетероциклу (наприклад, сполуки ряду азирідину, оксирану, азетидину, фурану, |
|||||||||||||
хіноліну |
та |
.ін). Хоча |
така |
класифікація |
не |
завжди |
дозволяє |
однозначно |
|||||
віднести |
ЛЗ |
до |
|
певного |
класу(деякі |
з |
них |
мають |
декілька |
різних |
|||
функціональних груп або гетероциклів), в процесі вивчення курсу ми будемо намагатися розглядати та поділяти їх на класи саме за хімічною будовою.
5. СИНТЕЗ ЛІКАРСЬКИХ РЕЧОВИН АЛІФАТИЧНОГО РЯДУ
Серед незаміщених насичених |
вуглеводнів аліфатичного ряду лише |
окремі речовини застосування в якості лікарських препаратів. Зупинимось на |
|
деяких з них. Вазелін – суміш рідких та |
твердих, головним чином насичених |
