
- •1.1. Еволюція хімії лікарських засобів
- •1.2. Предмет та об’єкти дисципліни «Органічний синтез лікарських засобів»
- •2.1. Сучасні вимоги до лікарських препаратів
- •2.2. Стратегія органічного синтезу ЛР
- •2.3. Загальні принципи комп’ютерного пошуку та конструювання ЛЗ
- •2.4. Схема розробки нового лікарського препарату
- •2.5. Особливості органічного синтезу лікарських субстанцій
- •3.1 Вплив функціональних груп на біологічну активність молекули
- •3.1.1. Вплив алкільних груп
- •3.1.2. Ефект галогенів
- •3.1.3. Вплив гідроксильних груп
- •3.1.5. Вплив аміногруп.
- •3.1.6. Дія кислотних угруповань
- •3.1.7. Вплив ненасичених зв’язків
- •5.1.1. Галогенпохідні в якості засобів для наркозу
- •5.1.2. Дихлороетиламінний фармакофор та його роль в створенні протипухлинних засобів
- •Етери та естери
- •5.3. Альдегіди та кислоти. Вітаміни F и В15
- •6.2. Пептиди
- •6.4. Похідні γ-аміномасляної кислоти.
- •6.5. Інші амінокислоти у фармацевтичних препаратах
- •7.1. Заміщені циклогексани
- •7.2. Камфора
- •7.3. Похідні адамантану
- •7.4. Стероїди з циклопентафенантреновою структурою. Вітамін D
- •8.1. Антисептики фенольного ряду
- •8.2. Аміноспирти ароматичного ряду
- •8.2.1. Аміноалкілбензени, похідні амфетаміну
- •8.2.2. Синтез адреноблокаторів фенольного ряду (анаприлін)
- •8.2.3. Похідні п-амінофенолу
- •8.3. Похідні бензенової та саліцилової кислот
- •8.4. Похідні п-амінобензенових кислот
- •8.4.1. Протитуберкульозні засоби – похідні п-амінобензенової кислоти
- •8.4.2. Анестетики на основі п-амінобензенової кислоти
- •8.5. Похідні сульфанілової кислоти
- •8.6. Антигістамінні препарати ряду діарилметану
- •8.7. Оксопохідні нафталену
- •9.1.1. Синтез протипухлинних речовин групи азирідину та оксирану
- •9.1.2. Антибіотики, що містять чотиричленне азетидинове ядро
- •9.2. Лікарські речовини на основі п'ятичленних гетероциклів
- •9.2.1. Аскорбінова кислота
- •9.2.2. Антибактеріальні нітрофурани
- •9.2.3. Противиразкові препарати з фурановим фрагментом (ранітидин, лупітидин)
- •9.2.4. Похідні піролу та індолу
- •9.2.5. Похідні піролідину в якості ноотропних та антигіпертензивних засобів
- •9.2.6. Похідні імідазолу та бензімідазолу
- •9.2.7. Похідні піразолу
- •9.2.8. Похідні тіазолу. Вітамін В1
- •9.3. Похідні шестичленних гетероциклів
- •9.3.1. Похідні бензопірану
- •9.3.2. Токофероли (вітамини групи Е)
- •9.3.3. Похідні піридину, хіноліну та ізохіноліну
- •9.3.4. Похідні піримідину
- •Похідні піримідинів з антивірусною (антиСНІД-овою) активністю
- •9.3.5. Похідні бензотіазинів.
- •9.3.6. Пуринові основи
- •9.4. Синтез лікарських засобів з семичленним гетероциклом. Похідні дибензодіазепінового ряду
- •9.5. Лікарські засоби – похідних біциклооктану.
52
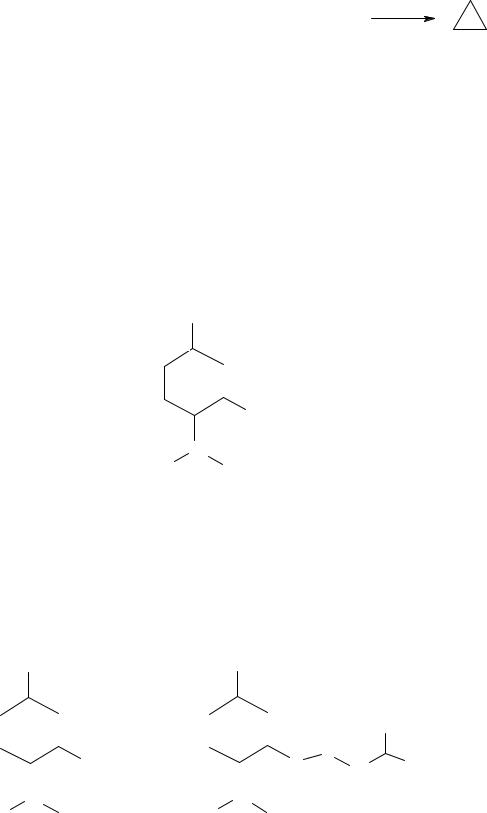
алілхлориду приєднують бромоводень з утворенням1-бром-3-хлоропропану. На наступній стадії його дегалогенують цинковим пилом у спирті за наявності йодиду натрію (NaI) з одержанням циклопропану:
Zn
Cl-CH2-CH=CH2 + HBr  Cl-CH2-CH2-CH2-Br
Cl-CH2-CH2-CH2-Br
-ZnBrCl
7.1. Заміщені циклогексани
Ментол – це L-2-ізопропіл-5-метил-циклогексанол-1. Оскільки ментол має три асиметричні атоми Карбону(помічені зірочками), він існує у вигляді восьми оптичних ізомерів та чотирьох рацематів. L-Ментол міститься в природних ефірних оліях (м’ятній та геранієвій). Добувають його з м’ятної олії виморожуванням за температури від-15°С до -20°С. Крім того, L-ментол добувають відновленням металічним натріємL-ментолу, який міститься (до 20%-ів) у м’ятній олії. Стереохімія в значній мірі ускладнює технологію одержання синтетичного ментолу, внаслідок необхідності виділення лише одного енантіомера.
CH3
*

 *
*
OH
*
CH
H3C CH3
Ментол Ментол входить до складу багатьох комбінованих препаратів, тому
потреба в ньому велика. Застосовують ментол як зовнішній болезаспокійливий засіб і як антисептик при запальних захворюваннях верхніх дихальних шляхів. Розповсюджений препарат валідол складається з суміші25%-ів ментолу та 75%-ів ментилового естеру ізовалеріанової кислоти. Валідол має заспокійливу дію на ЦНС, допомагає при легких приступах стенокардії.
|
|
CH3 |
|
CH3 |
|
O |
|
|
CH3 |
|||||
|
|
|
|
|
|
|
|
|
|
|
||||
|
|
|
|
|
|
|
|
|
|
|
||||
|
|
|
|
|
|
|
|
|
|
|
|
|
||
|
|
|
|
OH |
|
|
|
O |
C |
CH |
|
CH3 |
||
|
|
|
|
|
|
|
|
|
|
|
||||
|
|
|
|
|
|
|
|
|
|
|
|
2 |
|
|
|
|
|
CH |
|
|
CH |
|
|
|
|
|
|
|
|
H3C |
|
|
CH3 |
H3C |
CH3 |
|
|
|
|
|
|
|||
|
|
25% |
Валідол |
75% |
|
|
|
|
|
|
||||
|
|
|
|
|
|
|
|
|
|
|
|
|||
53
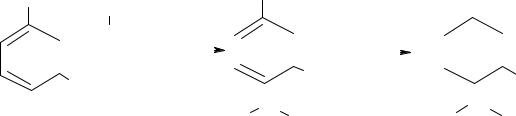
Ментол має м'ятний запах та приємний смак, що холодить, тому його використовують також для ароматизації ,ЛЗхарчових продуктів та зубної пасти. Рацемічний синтетичний ментол одержують в промисловості реакцією алкілювання м-крезолу 2-хлорпропаном за наявності каталізатора– кислот Льюіса:
|
CH3 |
|
|
|
|
|
CH3 |
|
|
|
CH |
||||||||||||
|
CH3 |
|
|
|
|
|
H2, Ni |
|
|
3 |
|
||||||||||||
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|||||||||
|
|
|
Cl |
|
CH |
|
CH3 (AlCl3) |
|
|
|
|
|
|
|
|
|
|
|
|
||||
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|||||||
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|||||||||
|
|
|
|
|
|
- HCl |
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
||
|
|
|
OH |
|
|
|
|
OH |
|
|
|
|
|
|
|
OH |
|||||||
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
||||||
|
|
|
|
|
|
|
|
|
|
|
|
||||||||||||
|
|
|
|
|
|
|
|
|
H3C CH CH3 |
|
H3C |
|
CH |
||||||||||
|
|
|
|
|
|
|
|
|
|
|
|
|
|
CH3 |
|||||||||
|
|
|
|
|
|
|
|
|
|
Тимол |
|
|
Ментол |
||||||||||
Ізопропільна група, головним чином, заміщує Гідроген, що знаходиться в орто-положенні до гідроксильної групи. Тимол, який при цьому утворюється, гідрують на нікелевому каталізаторі під тиском водню за температури120 – 180°С. Суміш ізомерів, що одержали при відновленні тимолу, розділяють на ізомери.
Ще одна важлива сполука цього ряду– ретинол (вітамін А), що був відкритий в 1913 році двома незалежними групами вчених (Е. Мак-Коллут та К. Осборн). Це перший з відкритих вітамінів, у зв'язку з чим й отримав літеру «A».
У 1921 році Д. Стинбок описав авітамінозА, для якого були характерні затримка росту, захворювання очей, а також підвищена схильність до різних інфекцій.
Структурна формула ретинолу була визначена у1931 році швейцарським
хіміком П. Каррером та |
шведським |
біохіміком. |
ЕйлерХ-Хельпиним. |
В |
|||
подальшому були численні спроби синтезу даного вітаміну, проте, тільки в |
|||||||
1942 році |
Бакстером |
та |
його |
співробітниками |
було отримано перший |
||
кристалічний |
вітамін А. |
В |
1946 |
році |
Іслером був здійснений |
перший |
|
крупномасштабний промисловий синтез цього вітаміну. |
|
|
|||||
Ретинол |
належить |
до |
тетраєнових |
похідних |
циклогексену й |
включає |
|
чотири ізопренових фрагменти. Вітамін А містить ряд близьких за стуктурою сполук: ретинол (вітамін A1), дегідроретинол (вітамін А2), ретиналь (альдегід вітаміну A1), ретиноєву кислоту, естери цих речовин. Каротини (α-, β-, γ-), що є провітамінами вітаміну А, в організмі людини перетворюються на ретинол, ретиналь та ретиноєву кислоту.
Найбільш розповсюдженим та біологічно активнимβ-каротинє. Ферментативний гідроліз однієї його молекули приводить до двох молекул ретинолу, а гідроліз α- та γ-ізомерів – лише до однієї молекули.

54
H C CH |
CH3 |
CH3 |
3 |
3 |
R |
|
|
CH3
R=CH2OH – ретинол (вітамін А1)
R=CHO – ретиналь
R=COOH – ретиноєва кислота (вітамін А2)
Жир печінки риб містить велику кількість вітамінуА. Рослини багаті провітаміном, головним з яких є β-каротин(морква, салат, зелена цибуля). Каротин в організмі піддається окисному ферментативному розщепленню з утворенням ретиналю, який відновлюється в ретинол, а останній у вигляді естерів вищих жирних кислот депонується в печінці.
Виробляється й використовується цей вітамін у вигляді ретинолу ацетату
та ретинолу пальмітату. Необхідний для зору та кісток, здоров'я |
шкіри |
і |
||||
волосся, нормальної роботи імунної системи, тощо. |
|
|
|
|||
Раніше вітамін А добували |
екстракцією з |
печінки морських |
риб, але |
в |
||
наш час цей метод поступився синтетичному методу добування. Це складний |
||||||
багатостадійний |
синтез, що |
ґрунтується |
на |
поступовому |
нарощуванні |
|
карбонового ланцюга. Синтез починається конденсацією ацетилену та ацетону та має більше десяти стадій.
Існує також біотехнологічний шлях виробництва ретинолу з β-каротину з застосуванням ферменту каротиндегідрогенази.
7.2. Камфора
Камфора відноситься |
до похідних біциклогептену. Цей терпеноїд |
|||||
міститься |
у D-формі у |
камфорному |
дереві(Китай, Японія) |
та камфорному |
||
базиліку, звідки його й одержують перегонкою з водяною парою, |
потім |
|||||
очищують |
сублімацією. |
У |
медицині |
застосовують як |
природну |
оптично |
активну камфору, так і синтетичну рацемічну.
Рацемічну камфору синтезують з α-пінену через відповідний форміат:
H3C |
CH3 |
H3C |
CH3 |
H3C CH3 |
H3C |
HCOOH |
O |
CH3 |
CH3 |
|
||||
|
|
H C O |
|
O C |
α-Пінен |
|
|
Камфора |
|

|
|
|
|
|
|
|
55 |
|
|
|
|
H3C |
CH3 |
|
|
|
|
|
Br2 |
O |
CH3 |
|
|
|
|
|
|
|
|
|
|
|
|||
|
|
|
C |
|
|
|
|
|
|
-HBr |
|
|
|
|
|
||
|
Br |
|
|
|
|
|
||
|
|
|
|
|
|
|
|
|
|
|
|
Бромкамфора |
|
|
|
|
|
|
Камфора збуджує ЦНС, стимулює дихання та обмінні процеси в міокарді. |
|
||||||
Введення атому Брому в α-положення до кетонної групи |
різко |
зміню |
||||||
фармакологічні |
властивості |
камфори. Бромкамфора |
покращує |
серцеву |
||||
діяльність, має седативні властивості, заспокоює центральну нервову систему. |
|
|||||||
Одержують бромкамфору при нагріванні камфори з бромом |
в |
розчин |
||||||
хлороформу або тетрахлорометану. |
|
|
|
|
||||
7.3. Похідні адамантану
Адамантан – родоначальник гомологічного ряду каркасних вуглеводів алмазоподібної будови. На його основі з’явилась нова галузь органічної хімії, що активно розвивається– хімія поліедранів. Похідні адамантану знайшли практичне застосування в якості ЛЗ з противірусною та антипаркинсонічною
активністю |
|
1-Аміноадамантан (мідантан, амантадін) – перший |
синтетичний |
антигрипозний засіб. Його почали застосовувати у1967 році. Пізніше було відкрито його антипаркинсонічний ефект.
Вихідною сполукою для синтезу похідних є сам адамантан. Найлегшим шляхом функціоналізації якого є одержання галогенопохідних. В залежності від умов, при бромуванні можна одержати моно-, ди-, трибромоадамантани.
1-Аміноадамантан одержують за наступною схемою: на першій стадії адамантан бромують молекулярним бромом за температури80 – 100°С. Для того, щоб одержати монобромопохідну(1-бромоадамантан) бром не повинен містити домішок заліза або інших можливих кислот каталізаторів– кислот Льюіса, тому його попередньо переганяють. Далі дією формаміду 1-бромоадамантан формулюють. На останній стадії під дією хлоридної кислоти
здійснюється гідроліз, що |
й приводить до |
бажаного1-аміноадамантану |
||
(амантадину). |
|
|
|
|
|
|
O |
|
|
Br |
C |
H |
NH2 |
. HCl |
HN |
||||
Br2 |
HCONH2 |
HCl, H2O |
|
|
|
|
-HCOH |
|
|
Амантадин
