
- •Isbn 5-225-02710-5 © X. А. Мусалатов, 1998
- •Глава 1. Общая характеристика катастроф и чрезвычайных ситуаций
- •1.1. Виды катастроф
- •Классификация катастроф
- •1.1.2. Искусственные катастрофы
- •1.2. Характеристика чрезвычайных ситуаций
- •Глава 2. Содержание и основы оказания хирургической помощи при катастрофах
- •2.1. Служба медицины катастроф России
- •2.2. Общие принципы оказания хирургической помощи пораженным
- •2.3. Виды медицинской помощи при ликвидации последствий чрезвычайных ситуаций
- •1. Неотложные мероприятия (первой очереди):
- •2. Мероприятия, выполнение которых может быть вынужденно отложено (второй очереди):
- •2.4. Медицинская сортировка и эвакуация пораженных
- •2.4.1. Проведение медицинской сортировки
- •До месту жительства {легкопирнженные)
- •Ilih до окончителвнога нсъодл
- •Медицинская сортировка при оказании первой врачебной помощи
- •2.4.2. Эвакуация пораженных
- •Глава 3. Организационные, медицинские и деонтологические особенности работы медицинского персонала в условиях чрезвычайных ситуаций
- •3.1. Особенности организации работы при чрезвычайных ситуациях
- •3.2. Особенности оказания неотложной медицинской помощи в чрезвычайных ситуациях
- •Глава 4. Угрожающие жизни состояния 4.1. Шок
- •4.1.1. Этиология и основы патогенеза шока
- •4.1.2. Патофизиология шока
- •4.1.3. Клинические проявления травматического шока
- •4.1.4. Диагностика, определение тяжести и прогноза течения шока
- •4.1.5. Некоторые особенности течения шока
- •4.1.6. Лечебные мероприятия при шоке
- •4.2. Острая дыхательная недостаточность
- •4.2.1. Этиология и патогенез
- •4.2.2. Клинические проявления острой дыхательной недостаточности
- •4.2.3. Принципы лечения пострадавших с острой дыхательной недостаточностью при травмах
- •4.3. Кома
- •4.4. Оказание медицинской помощи пострадавшим с угрожающими жизни состояниями
- •1. Противошоковые мероприятия должны быть начаты как можно раньше и произведены в максимально возможном объеме.
- •4.4.1. Первая медицинская помощь
- •4.4.2. Доврачебная помощь
- •4.4.3. Первая врачебная помощь
- •4.4.4. Квалифицированная медицинская помощь
- •4.4.5. Специализированная медицинская помощь
- •Глава 5. Реанимационные мероприятия при катастрофах 5.1. Терминальные состояния
- •5.2. Проведение реанимационных мероприятий пострадавшим в катастрофах
- •5.2.1. Первая медицинская и доврачебная помощь
- •5.2.2. Первая врачебная помощь
- •5.2.3. Квалифицированная медицинская помощь
- •Глава 6. Кровотечение. Кровопотеря. Компенсация кровопотери при ликвидации последствий чрезвычайных ситуаций
- •6.1. Виды кровотечений
- •6.2. Тяжесть кровопотери
- •6.3. Инфузионно-трансфузионные среды, применяемые для коррекции острой кровопотери
- •6.4. Оказание помощи пострадавшим с кровотечениями и кровопотерей при катастрофах
- •Задачи при оказании различных видов медицинской помощи пострадавшим с кровотечением и острой кровопотерей
- •6.4.1. Первая медицинская помощь
- •Окончательная остановка наружного и внутреннего кровотечения
- •6.4.2. Доврачебная помощь
- •6.4.3. Первая врачебная помощь
- •При оказании первой врачебной помощи обязательно производится ревизия жгута.
- •5E:I помощи жгута!
- •Mvmtipur-jiniir чип ктрал * пот о сосуда;
- •6.4.4. Квалифицированная медицинская помощь
- •6.4.5. Специализированная медицинская помощь
- •Глава 7. Методы и средства обезболивания при оказании помощи пострадавшим
- •7.1. Виды анестезии
- •7.1.1. Местная и регионарная анестезия
- •7.1.2. Центральная и общая анестезия
- •7.2. Проведение обезболивания у пострадавших при катастрофах
- •7.2.1. Первая медицинская и доврачебная помощь
- •7.2.2. Первая врачебная помощь
- •1. Место вкола иглы должно быть в стороне от проекции сосу
- •7.2.3. Квалифицированная медицинская помощь
- •7.2.4. Специализированная медицинская помощь
- •Глава 8. Иммобилизация при повреждениях конечностей
- •8.1. Транспортная иммобилизация
- •8. В зимнее время иммобилизованную конечность необходимо дополнительно утеплить.
- •8.2. Лечебная иммобилизация
- •8.2.1. Гипсовые повязки
- •8.2.2. Вытяжение
- •8.3. Проведение иммобилизации пострадавшим с повреждениями конечностей
- •Иммобилизация при оказании медицинской помощи пострадавшим
- •Глава 9. Раны мягких тканей
- •9.1. Классификация, характеристика ран мягких тканей
- •9.1.1. Раны неогнестрельного происхождения
- •9.1.2. Огнестрельные раны
- •9.1.3. Взрывная травма
- •9.2. Клинические проявления и особенности течения раневого процесса
- •9.3. Хирургическая обработка ран
- •9.4. Оказание медицинской помощи пострадавшим с ранениями мягких тканей
- •9.4.1. Первая медицинская и доврачебная помощь
- •9.4.2. Первая врачебная помощь
- •9.4.3. Квалифицированная медицинская помощь
- •9.4.4. Специализированная медицинская помощь
- •Глава 10. Раневая инфекция
- •10.1. Этиология, патогенез, клинические проявления раневой инфекции
- •10.2. Общие принципы профилактики и лечения гнойных осложнений ран
- •10.3. Особые виды раневой инфекции
- •10.3.1. Столбняк
- •10.3.2. Анаэробная газовая инфекция
- •10.3.3. Гнилостная инфекция
- •10.4. Особенности оказания медицинской помощи пострадавшим с инфекционными осложнениями ран
- •Глава 11. Закрытые повреждения костей и суставов конечностей
- •11.2. Закрытые травматические вывихи
- •11.3. Оказание медицинской помощи пострадавшим с закрытыми повреждениями костей и суставов
- •11.3.1. Первая медицинская и доврачебная помощь
- •11.3.2. Первая врачебная помощь
- •11.3.3. Квалифицированная медицинская помощь
- •Медицинская сортировка пострадавших с закрытыми повреждениями костей и суставов конечностей и оказание им первой врачебной и квалифицированной медицинской помощи
- •Сортировка в эавненмоп'н от тяжести ию» Прн
- •Эвакуация
- •Госпитальная
- •11.3.4. Специализированная медицинская помощь
- •Глава 12. Открытые повреждения костей и суставов
- •12.1. Характеристика открытых повреждений костей и суставов
- •12.1.1. Открытые переломы
- •12.1.2. Открытые повреждения суставов
- •12.2. Оказание помощи пострадавшим с открытыми повреждениями костей и суставов
- •12.2.1. Первая медицинская и доврачебная помощь
- •12.2.2. Первая врачебная помощь
- •12.2.3. Квалифицированная медицинская помощь
- •Медицинская сортировка пострадавших с открытыми повреждениями костей и суставов и оказание им квалифицированной медицинской помощи
- •Госпитальная
- •- Гдофмлпгткл
- •12.2.4. Специализированная медицинская помощь
- •Глава 13. Повреждения позвоночника
- •13.1. Классификация и механизм повреждений позвоночника и спинного
- •13.2. Диагностика повреждений позвоночника и спинного мозга
- •13.2.1. Неосложненные повреждения позвоночника
- •13.2.2. Осложненные повреждения позвоночника
- •13.3. Оказание медицинской помощи пострадавшим с повреждениями позво-
- •13.3.1. Первая медицинская и доврачебная помощь
- •13.3.2. Первая врачебная помощь
- •13.3.3. Квалифицированная медицинская помощь
- •13.3.4. Специализированная медицинская помощь
- •Глава 14. Повреждения таза и тазовых органов
- •14.1. Классификация и клиническая картина повреждений таза
- •14.2. Повреждения тазовых органов
- •14.3. Оказание медицинской помощи пострадавшим с повреждениями таза и тазовых органов
- •14.3.1. Первая медицинская и доврачебная помощь
- •14.3.2. Первая врачебная помощь
- •14.3.3. Квалифицированная медицинская помощь
- •14.3.4. Специализированная медицинская помощь
- •Глава 15. Повреждения груди
- •15.1. Классификация, диагностика повреждений груди
- •15.2. Особенности оказания медицинской помощи пострадавшим с травмой
- •15.2.1. Первая медицинская и доврачебная помощь
- •15.2.2. Первая врачебная помощь
- •Эвакуация
- •15.2.3. Квалифицированная медицинская помощь
- •15.2.4. Специализированная медицинская помощь
- •Глава 16. Повреждения живота
- •16.1. Классификация повреждений живота
- •Без повреждения внутренних органом
- •16.2. Клиническая картина, диагностика повреждений живота
- •16.3. Оказание медицинской помощи пострадавшим
- •16.3.1. Первая медицинская и доврачебная помощь
- •16.3.2. Первая врачебная помощь
- •16.3.3. Квалифицированная медицинская помощь
- •V операнда)
- •Кроватей ашя; - ревизия органов брюншеи полости: перанчния кнруршчеиг.Ш
- •16.3.4. Специализированная медицинская помощь
- •Глава 17. Черепно-мозговая травма
- •17.1. Классификация черепно-мозговой травмы
- •17.2. Клиническая картина и диагностика
- •17.3. Оказание медицинской помощи пострадавшим с черепно-мозговой травмой
- •17.3.1. Первая медицинская и доврачебная помощь
- •17.3.2. Первая врачебная помощь
- •17.3.3. Квалифицированная медицинская помощь
- •17.3.4. Специализированная медицинская помощь
- •Глава 18. Повреждения лица и шеи
- •18.1. Классификация, диагностика повреждений лица и шеи
- •18.1.1. Ранения мягких тканей лица
- •18.1.2. Повреждения лор-органов
- •18.1.3. Переломы костей лицевого черепа
- •18.1.4. Повреждения глаз
- •18.2. Оказание медицинской помощи пострадавшим с повреждениями лица и
- •18.2.1. Первая медицинская и доврачебная помощь
- •18.2.2. Первая врачебная помощь
- •18.2.3. Квалифицированная медицинская помощь
- •18.2.4. Специализированная медицинская помощь
- •Глава 19. Термические ожоги
- •19.1. Местные изменения при ожогах
- •19.2. Ожоговая болезнь
- •19.3. Оказание помощи пострадавшим при термических ожогах
- •19.3.1. Первая медицинская и доврачебная помощь
- •19.3.2. Первая врачебная помощь
- •Медицинская сортировка пострадавших с термическими ожогами и оказание им первой врачебной и квалифицированной медицинской помощи
- •Площадка
- •Гсямптоматнчесхая терапия)
- •Госпитальное отделение
- •19.3.3. Квалифицированная медицинская помощь
- •19.3.4. Специализированная медицинская помощь
- •Глава 20. Холодовая травма
- •20.1. Виды холодовой травмы
- •20.1.1. Отморожение
- •20.1.2. Общее охлаждение (замерзание)
- •20.2. Осложнения холодовой травмы
- •20.3. Оказание помощи пострадавшим при холодовой травме
- •20.3.1. Первая медицинская и доврачебная помощь
- •20.3.2. Первая врачебная помощь
- •20.3.3. Квалифицированная медицинская помощь
- •Медицинская сортировка пострадавших с холодовой травмой и оказание им первой врачебной и квалифицированной медицинской помощи
- •Площадка
- •Гершшм)
- •1 Периую очередь
- •20.3.4. Специализированная медицинская помощь
- •Глава 21. Синдром длительного сдавления мягких тканей конечностей
- •21.1. Терминология
- •21.2. Патогенез синдрома длительного сдавления
- •21.3. Клинические проявления синдрома длительного сдавления
- •21.4. Оказание помощи пострадавшим с сдс
- •21.4.1. Первая медицинская и доврачебная помощь
- •21.4.2. Первая врачебная помощь
- •21.4.3. Квалифицированная медицинская помощь
- •21.4.4. Специализированная медицинская помощь
- •Глава 22. Политравма. Особенности оказания помощи пострадавшим при катастрофах
- •22.1. Терминология, классификация, клинические проявления
- •22.2. Особенности клинического течения комбинированных поражений
- •22.2.1. Комбинированные радиационные поражения
- •22.2.2. Комбинированные химические поражения
- •22.3. Особенности оказания помощи пострадавшим с политравмой
- •22.3.1. Первая медицинская и доврачебная помощь
- •22.3.2. Первая врачебная помощь
- •22.3.3. Квалифицированная медицинская помощь
- •22.3.4. Специализированная медицинская помощь
- •Глава 2. 1 - б; 2 - в, д; 3 - б, в; 4 - б, в; 5 - а, в, г, д; 6 - в, г; 7 - г.
Пусковым
механизмом в развитии шока при травмах
является острая кровопотеря, в результате
которой развивается синдром малого
выброса. Шок развивается, как правило,
не только в связи с уменьшением объема
циркулирующей крови (ОЦК) и его
компонентов, сколько в результате
интенсивности кровопотери. Острая
потеря 50 /о крови у молодого здорового
пациента приводит к острой циркуляторной
недостаточности и развитию картины
глубокого шока. Тяжелые стадии шока
развиваются в условиях абсолютной
гиповолемии (уменьшение ОЦК за счет
кровопотери) в сочетании с относительной
гиповолемией (увеличение емкости
сосудистого русла в результате мощного
болевого воздействия влияния метаболитов
и токсемии). Возникновение этой
«вторичной гиповолемии» и степень ее
выраженности зависят от того, как давно
организм получил тяжкие повреждения.
I
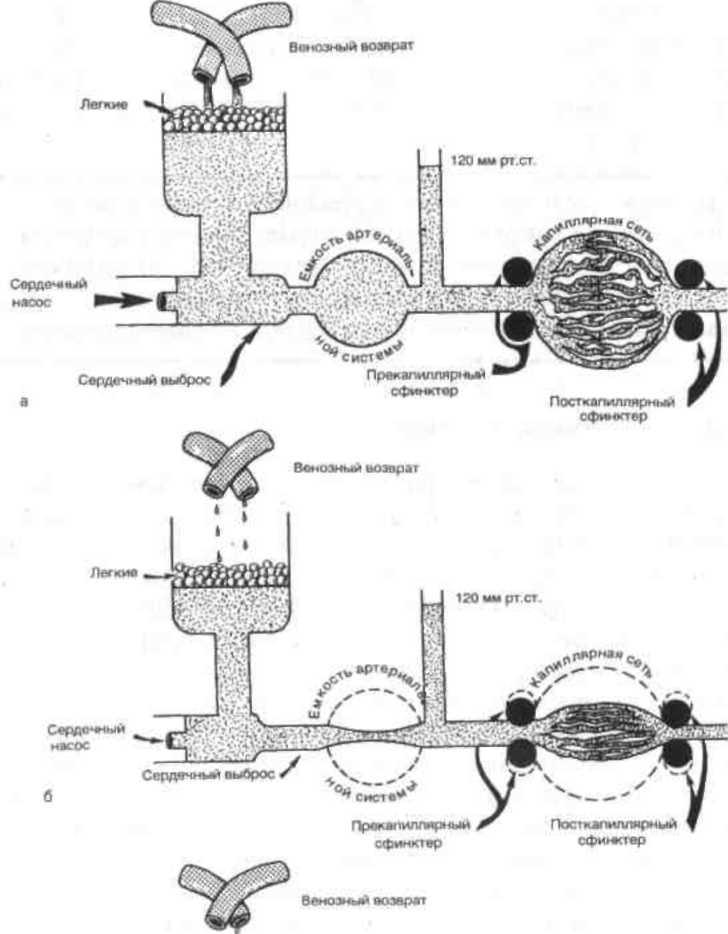
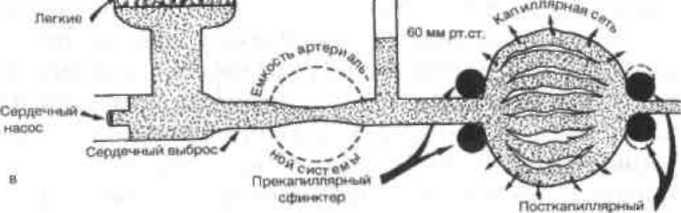
Рис.
4.1.
Развитие синдрома малого выброса при
шоке (схема).
а
— кровообращение при нормальном объеме
крови; б — кровообращение при
компенсированном шока; в — кровообращение
при декомпененрованном шоке.
Так
как основной емкостью для крови является
«система малого давления», т. е. венозная
система, принимающая на себя до 75 %
объема крови, то кровопотеря отражается
прежде всего на объеме крови в венах.
Венозные сосуды обладают хорошо развитым
веномоторным меха-4.1.2. Патофизиология шока
низмом,
позволяющим быстро приспосабливать
емкость системы к изменившемуся объему
крови. До тех пор пока действует этот
адаптационный механизм, центральное
венозное давление (ЦВД) остается в
прежних пределах, и венозный возврат
не меняется. Однако эти возможности
ограничены и исчерпываются уже при
потере 5-10 % ОЦК. С истощением веномоторного
адаптационного механизма ЦВД уменьшается
и венозный возврат снижается. Это ведет
к уменьшению сердечного выброса. Однако
организм стремится компенсировать
недостаточный венозный возврат
нарастающей тахикардией. Поскольку
диастолический период и длительность
наполнения полостей сердца при тахикардии
укорочены, ударный объем уменьшается.
Минутный объем сердца при этом может
довольно долго оставаться на прежнем
уровне или даже повышаться. При истощении
этого механизма, которое наступает с
уменьшением венозного возврата на
25—30 %, начинает снижаться сердечный
выброс — развивается синдром малого
выброса (рис. 4.1).
Как
известно, адаптационные и компенсаторные
реакции организма при любых условиях
снижения объемного кровотока направлены
прежде всего на сохранение адекватного
кровообращения в жизненно важных
органах (мозг, сердце, печень и почки).
При невозможности поддержания
кровотока развивается следующий этап
компенсации — периферическая
вазоконстрикция, обеспечивающая
поддержание артериального давления
на уровне выше критического. Этот
феномен известен под названием
«централизация кровообращения», т.е.
поддержание кровотока в мозге, коронарных
сосудах и крупных сосудистых магистралях
за счет уменьшения перфузии мезентериальных
сосудов, сосудов почек, печени, подкожной
клетчатки и т.д. Возрастает
нейроэндокринная стимуляция.
Активизируется ренин-ангиотензиновая
система, в кровь выбрасывается
альдостерон, который задерживает в
организме натрий, что в свою очередь
ведет к увеличению продукции
антидиуретического гормона и таким
образом увеличивает реабсорбцию воды,
концентрацию АКТГ, глюкокортикоидов,
а главное — катехоламинов, которые
в основном и обеспечивают централизацию
кровообращения. Организм в порядке
«скорой помощи» пытается привести
объем сосудистого русла в соответствие
с уменьшением ОЦК путем сужения сосудов.
Эта реакция становится тем менее
целесообразной, чем длительнее она
существует. С каждой минутой нарастает
депонирование крови в венулах и
капиллярах; происходит своеобразное
«кровотечение в собственные сосуды».
Вследствие
гипоксии в отключенных от адекватной
перфузии при централизации кровообращения
тканях в условиях активной стимуляции
катехоламинами анаэробного обмена в
крови начинает нарастать количество
промежуточных недоокисленных продуктов
обмена, в частности молочной кислоты
(лактата). Возникает метаболический
ацидоз. При концентрации лактата более
8,8 мкмоль/л развивается отек эндотелия
капилляров, мембран форменных элементов
крови (эритроцитов, тромбоцитов,
лейкоцитов). Медленно движущиеся в
капиллярах форменные элементы
склеиваются в «монетные столбики», или
агрегаты (сладж-синдром). При этом же
уровне лактата начинается отек нейроглии
мозга, поражаются ретикулоэндотелиальная
система и проводящая система сердца.
Депонирование крови нарастает, из-за
чего венозный приток, сердечный
выброс и артериальное давление
прогрессивно уменьшаются, усугубляя
тем самым нарушения микроциркуляции.
В 2— 4 раза возрастает разница насыщения
кислородом артериальной и венозной
крови, что связано с уменьшением объемной
скорости кровотока: ткани успевают
«выбрать» почти весь кислород. В венозной
крови содержание кислорода снижается
с 14—15 до 4—5 об. %. К тканям доставляется
все меньше кислорода, так как в целом
количество крови в организме уменьшается,
и растет артериальная гипоксия. Общее
потребление кислорода резко падает,
ткани испытывают тяжелое кислородное
голодание. В этой ситуации большое
значение приобретает гликолиз, а
следовательно, все больше увеличивается
содержание лакта-та. Легочная вентиляция
поддерживается путем перевозбуждения
респираторного центра, который
включает в дыхательный акт дополнительные
мышцы. Количество кислорода, уходящее
на работу дыхательных мышц, возрастает
с 3—5 до 40—50 %, что неминуемо требует
повышения минутного объема сердца, а
это в подобной ситуации практически
неосуществимо. В частности, поэтому
гиперпноэ может достаточно быстро
смениться гипопноэ и альвеолярной
гиповенти-ляцией.
