
- •Учебно-методические разработки для самостоятельной работы студентов по курсу «Теоретические основы защиты окружающей среды»
- •Часть I
- •Обезвоживание и методы очистки сточных вод
- •Введение
- •Глава 1. Основные законы термодинамики. Понятие энтропии как функции обесценивания энергии и стремления системы к хаосу
- •1.1 Понятие «энтропия». Принцип существования и возрастания энтропии
- •1.2. Энергоэнтропийная концепция аварийности и травматизма
- •1.3. Воздействие промышленного производства на природу. Ресурсосберегающая технология. Материальный баланс производства
- •1.4. Классификация основных процессов
- •1.5. Общие принципы анализа и расчета процессов и аппаратов
- •1.5.1. Материальный баланс
- •1.5.2. Энергетический баланс
- •1.5.3. Интенсивность процессов и аппаратов
- •1.5.4. Определение основных размеров аппаратов
- •1.5.5. Моделирование и оптимизация процессов и аппаратов
- •Контрольные вопросы
- •Глава 2. Классификация двухфазных систем
- •2.1. Методы обезвоживания
- •2.2. Формы связи воды с твердым телом. Энергия связи различных форм воды с твердым телом
- •2.3. Влагоудерживающая способность твердых тел. Влияние основных факторов на степень обезвоживания
- •Контрольные вопросы
- •Глава 3. Отделение жидкости под действием механических методов
- •3.1. Обезвоживание кускового материала дренированием
- •3.1.1. Гидродинамика течения жидкости под влиянием собственного веса в порах осадка
- •3.2. Отстаивание под действием силы тяжести
- •3.2.1. Основные понятия. Классификация суспензий
- •3.2.2. Способы выражения и расчета концентрации твердого в пульпе
- •3.2.3. Исследование скорости расслоения суспензий I-го и II-го классов методом длинной трубки
- •3.2.4. Качественное описание процесса расслоения суспензий III и IV классов
- •3.2.5. Расчет удельной поверхности сгущения по методу Коу и Клевенжера
- •3.2.6. Расчет удельной поверхности по методу Кинча
- •3.2.7. Определение высоты сгустителя
- •3.2.8. Пример расчета сгустителя по методу Кинча
- •Контрольные вопросы
- •Глава 4. Применение центробежной силы при обезвоживании
- •4.1. Основные понятия
- •4.2. Особенности применения гидроциклонов для обезвоживания
- •Порядок расчета гидроциклона.
- •4.3. Особенности применения центрифуг для сгущения суспензий
- •4.4. Основные закономерности разделения суспензий в осадительных центрифугах. Индекс производительности
- •4.5. Физические основы разделения суспензий в фильтрующих центрифугах
- •Контрольные вопросы
- •Глава 5. Фильтрование
- •5.1. Основные понятия. Классификация
- •5.2. Физические основы фильтрации с образованием осадка. Гидродинамика течения жидкости через пористые и зернистые слои
- •5.3. Основное уравнение фильтрации
- •5.4. Определение оптимальных условий работы фильтров. Экономически выгодный цикл фильтрации
- •5.5. Применение уравнения фильтрации. Определение удельного сопротивления осадка и его сжимаемости
- •5.6. Фильтровальные перегородки
- •5.7. Конструкции фильтров. Периодически и непрерывно действующие. Классификация. Фильтры, работающие под давлением. Вакуум-фильтры. Способы снятия осадка
- •5.8. Выбор и расчет фильтров
- •5.9. Схемы подсоединения вакуум-фильтров
- •Контрольные вопросы
- •Глава 6. Агрегирование
- •6.1. Теория процесса агрегирования. Механизмы встреч частиц друг с другом. Понятие о расклинивающем давлении Теория процесса агрегации
- •Два механизма соударения или встречи частиц
- •6.2. Три слагающие поверхностных сил (расклинивающего давления). Двучленный закон взаимодействия
- •6.3. Силы Ван-дер-Ваальса. Слагающие сил Ван-дер-Ваальса. Ван-дер-ваальсово взаимодействие между молекулами и конденсированными фазами Силы Ван-дер-Ваальса
- •Электромагнитная теория взаимодействия конденсированных фаз
- •6.4. Природа ионно-электростатических сил. Закономерность изменения их вглубь раствора
- •6.5. Гидратационная слагаемая поверхностных сил (расклинивающего давления)
- •6.6. Три механизма агрегирования: коагуляция, флокуляция, мостиковая флокуляция
- •6.7. Основные принципы селективной агрегации частиц
- •6.8. Характеристика применяемых высокомолекулярных синтетических флокулянтов
- •Контрольные вопросы
- •Глава 7. Абсорбция
- •7.1. Общие сведения
- •7.2. Равновесие при абсорбции
- •7.3. Материальный и тепловой балансы процесса
- •7.4. Скорость процесса
- •Контрольные вопросы
- •Глава 8. Адсорбция
- •8.1. Общие сведения
- •8.2. Характеристики адсорбентов и их виды
- •8.3. Равновесие при адсорбции
- •8.4. Кинетика адсорбции
- •8.5. Десорбция
- •Контрольные вопросы
- •Глава 9. Флотация
- •9.1. Общие сведения
- •9.2. Теоретические основы процесса флотации
- •9.3.Флотационные реагенты и их классификация
- •9.4. Механизм действия собирателей
- •9.5. Реагенты-депрессоры
- •9.6.Реагенты-активаторы
- •9.7. Реагенты-регуляторы среды
- •9.8. Реагенты-пенообразователи
- •Контрольные вопросы
- •Глава 10. Экстракция
- •10.1 Процессы экстракции в системах жидкость-жидкость
- •10.1.1. Общие сведения
- •10.1.2. Равновесие в системах жидкость - жидкость
- •10.1.3. Методы экстракции
- •10.2. Процессы растворения и экстракции в системах твердое тело - жидкость
- •10.2.1. Общие сведения
- •10.2.2. Равновесие и скорость выщелачивания
- •Контрольные вопросы
- •Глава 11. Сушка
- •11.1. Основные понятия. Параметры, подлежащие расчету
- •11.2. Равновесное содержание влаги при сушке. Кинетика сушки. Понятие о напряжении объема сушилки
- •11.3. Основные параметры влажного воздуха
- •11.5. Изображение процессов изменения состояния воздуха на j - X на диаграмме
- •11.6. Материальный и тепловой балансы сушки
- •11.7. Расчет удельных расходов воздуха и тепла на сушку
- •11.8. Расчет сушилки в случае частичной рециркуляции обработанного воздуха
- •11.9. Сушка топочными газами
- •11.10. Конструкции сушилок
- •Контрольные вопросы
- •Литература
- •Оглавление
- •Глава 1. Основные законы термодинамики. Понятие энтропии как функции обесценивания энергии и стремления системы к хаосу 6
- •Глава 2. Классификация двухфазных систем 41
- •Глава 3. Отделение жидкости под действием механических методов 50
- •Глава 4. Применение центробежной силы при обезвоживании 75
- •Глава 5. Фильтрование 86
- •Глава 6. Агрегирование 117
- •Глава 7. Абсорбция 144
Электромагнитная теория взаимодействия конденсированных фаз
В настоящее время Лившицем, Питаевским и Даглошанским развивается более общий подход к рассмотрению взаимодействия конденсированных фаз. Они рассматривают взаимодействие твердых тел, как обмен квантами энергии электромагнитного излучения, наподобие обменных валентных сил, с той разницей, что электромагнитное поле носит случайный характер, вызванный флуктуацией энергии, а квант энергии h имеет малое абсолютное значение.
В
Рис.6.4.
Зависимость
энергии притяжения двух параллельных
плоскостей от статической
диэлектрической постоянной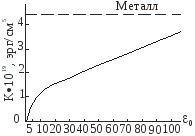
Этот подход позволяет представить универсальную зависимость энергии взаимодействия двух тел (в виде кубиков с площадью 1 см2) от величины статистической диэлектрической постоянной (рис. 6.4). У твердых диэлектриков в большинстве случаев 0 изменяется от 2 до 10. Таким образом их энергия взаимодействия не превышает 1·10-19 эрг/см3.
Максимальная сила притяжения должна быть для металлов, так как для них 0 можно считать равной бесконечности.
Экспериментально этот факт подтверждается. Металлы наиболее гидрофобны, легко флокулируют и флотируются, особенно в тех случаях, когда с их поверхности растворена окисленная пленка.
Сила, действующая на два твердых тела, которые разделены жидкой прослойкой для случая H < , имеет вид:
![]() ,
а
,
а
![]() ,
,
где 1, 2 - мнимая часть диэлектрической проницаемости для твердого тела 1 и 2; 3 - для разделяющей жидкой прослойки.
Из формулы видно, что в случае одинаковых тел (1 = 2) разности (1 – 3) и (2 – 3)имеют одинаковый знак, следовательно, сила F > 0, т.е. притяжение всегда существует.
В случае тел различной природы, для которых разности (1 – 3) и (2 – 3) имеют разные знаки, F < 0, следовательно, возможно отталкивание. Например, для системы металл (2 = ), вода (3 = 80) и диэлектрик (1 = 10):
1 – 3 = 10 – 80 = -70;
2 – 3 = - 80 = + ,
следовательно, F < 0, т.е. диэлектрик не должен притягиваться силами Ван-дер-Ваальса к металлу в среде, где его 1 < 3 жидкости.
6.4. Природа ионно-электростатических сил. Закономерность изменения их вглубь раствора
На границе раздела твердое тело - жидкость всегда возникает двойной электрический слой. Механизм его возникновения обусловлен следующими факторами:
а) преимущественным растворением катиона или электрона у металлов, аниона или катиона у солей и окислов;
б) преимущественной адсорбцией катионов или анионов из раствора;
в) направленной ориентацией диполей полярных молекул в пограничном слое;
г) образованием полярных химических связей.
Электростатическое взаимодействие связано с перекрытием внешних (диффузионных) обкладок двойного электрического слоя.
Результаты теоретических расчетов для трех практически важных случаев:
когда заряды взаимодействующих поверхностей противоположны;
когда заряды одноименны, но сильно отличаются по своей величине;
когда заряды одноименные и примерно одинаковые по своей величине, можно качественно проиллюстрировать ходом кривых зависимости расклинивающего давления от расстояния между частицами (рис. 6.5).
В первом случае, естественно, электростатические силы являются силами притяжения, а во втором - силами отталкивания. Не тривиален третий случай. До расстояния Н0 одноименно заряженные поверхности, но с сильно различающимися величинами зарядов, притягиваются, а, начиная с расстояния не менее Н0 - отталкиваются. Рмах на расстоянии Нмах - характеризует величину энергетического барьера, который должны преодолеть такие частицы, чтобы прилипнуть друг к другу.
Ч
Рис.6.5. Зависимость
ионно-электростатической слагающей
расклинивающего давления в трех
случаях: а)
противоположные
знаки зарядов поверхностей; б) одноименно
заряженные поверхности, заряды примерно
одинаковые; в)
одноименно заряженные поверхности,
заряды сильно отличаются.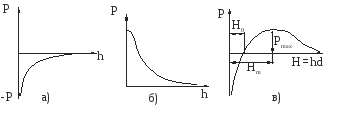
Главной особенностью электростатических сил является то, что радиус действия их является функцией концентрации электролита. При отсутствии электролита или при малой его концентрации вторая обкладка двойного электрического слоя носит диффузионный характер из-за теплового размытия и скачок межфазного потенциала распределен по всей толщине двойного слоя. Радиус действия электростатических сил можно оценить по толщине ионной атмосферы, параметра, вводимого в теорию сильных электролитов Дебая-Хюккеля
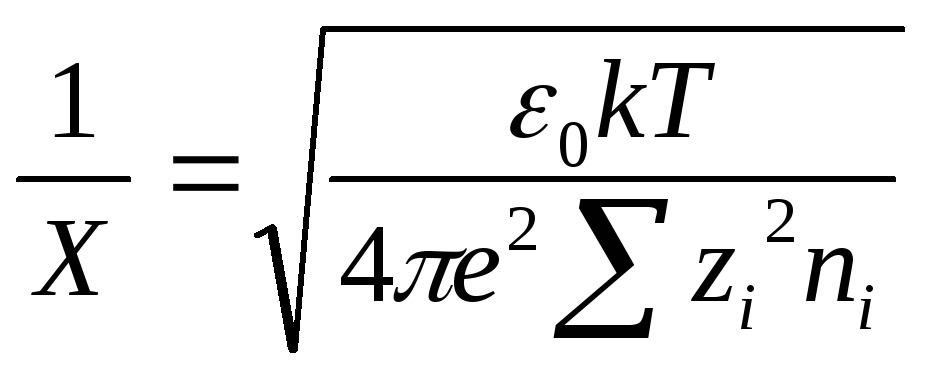 ,
,
где ε0 - диэлектрическая проницаемость; k- постоянная Больцмана; е - заряд электрона; zi - валентность i иона; ni - частичная концентрация i-го электролита, которая с молярной концентрацией связана соотношением
![]() ,
,
где N - число Авогадро.
Для одновалентного электролита зависимость приобретает простой вид:
![]() ,
,
где С - концентрация в г∙эквив/л.
Из этого уравнения следует, что для раствора 0,01N 1/Х=10-7 см. Так как ионный радиус - величина порядка 10-8 см, то толщина ионной атмосферы будет в 10 раз больше, чем радиус иона r. При 0,0001N 1/X=100 и т.д.
В однонормальном растворе толщина ионной атмосферы сравнима с радиусом иона. Все эти размеры являются оценками толщины диффузионного облака и двойного электрического слоя.
В случае большого заряда поверхностей механизмы коагуляции при прибавлении электролита можно объяснить сжатием двойного электрического слоя. В этом случае увеличением или снижением заряда поверхности, вследствие адсорбции ионов, можно пренебречь.
На рис. 6.6 видно, что прилипание обусловлено уменьшением радиуса действия электростатических сил отталкивания при сжатии двойного слоя. Радиус действия сил притяжения не зависит от концентрации электролита.
В
Рис.6.6.
Схема действия электростатической и
Ван-дер-ваальсовой слагающих
расклинивающего действия: а - при малой;
б - при большой концентрации электролита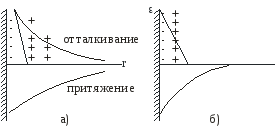
Сила коагулирующего действия электролитов в большой мере определяется валентностью ионов. Экспериментально установленное правило Шульца-Гарди nZ6 = const было выведено теоретически Ландау-Дерягиным. Концентрация электролита, необходимая для достижения порога коагуляции, в Z6 раз меньше для многовалентных электролитов. Например, ионов Ва+2 нужно добавить в 64=26 раз меньше, чем ионов Na+1при коагуляции коллоидов. Это правило лучше всего выполняется для сильноразряженных коллоидных частиц, когда прибавляется неадсорбирующий электролит. В общем случае произвольного заряда поверхности и учете адсорбции электролита критерий коагуляции имеет более сложный вид.
