
- •Учебно-методические разработки для самостоятельной работы студентов по курсу «Теоретические основы защиты окружающей среды»
- •Часть I
- •Обезвоживание и методы очистки сточных вод
- •Введение
- •Глава 1. Основные законы термодинамики. Понятие энтропии как функции обесценивания энергии и стремления системы к хаосу
- •1.1 Понятие «энтропия». Принцип существования и возрастания энтропии
- •1.2. Энергоэнтропийная концепция аварийности и травматизма
- •1.3. Воздействие промышленного производства на природу. Ресурсосберегающая технология. Материальный баланс производства
- •1.4. Классификация основных процессов
- •1.5. Общие принципы анализа и расчета процессов и аппаратов
- •1.5.1. Материальный баланс
- •1.5.2. Энергетический баланс
- •1.5.3. Интенсивность процессов и аппаратов
- •1.5.4. Определение основных размеров аппаратов
- •1.5.5. Моделирование и оптимизация процессов и аппаратов
- •Контрольные вопросы
- •Глава 2. Классификация двухфазных систем
- •2.1. Методы обезвоживания
- •2.2. Формы связи воды с твердым телом. Энергия связи различных форм воды с твердым телом
- •2.3. Влагоудерживающая способность твердых тел. Влияние основных факторов на степень обезвоживания
- •Контрольные вопросы
- •Глава 3. Отделение жидкости под действием механических методов
- •3.1. Обезвоживание кускового материала дренированием
- •3.1.1. Гидродинамика течения жидкости под влиянием собственного веса в порах осадка
- •3.2. Отстаивание под действием силы тяжести
- •3.2.1. Основные понятия. Классификация суспензий
- •3.2.2. Способы выражения и расчета концентрации твердого в пульпе
- •3.2.3. Исследование скорости расслоения суспензий I-го и II-го классов методом длинной трубки
- •3.2.4. Качественное описание процесса расслоения суспензий III и IV классов
- •3.2.5. Расчет удельной поверхности сгущения по методу Коу и Клевенжера
- •3.2.6. Расчет удельной поверхности по методу Кинча
- •3.2.7. Определение высоты сгустителя
- •3.2.8. Пример расчета сгустителя по методу Кинча
- •Контрольные вопросы
- •Глава 4. Применение центробежной силы при обезвоживании
- •4.1. Основные понятия
- •4.2. Особенности применения гидроциклонов для обезвоживания
- •Порядок расчета гидроциклона.
- •4.3. Особенности применения центрифуг для сгущения суспензий
- •4.4. Основные закономерности разделения суспензий в осадительных центрифугах. Индекс производительности
- •4.5. Физические основы разделения суспензий в фильтрующих центрифугах
- •Контрольные вопросы
- •Глава 5. Фильтрование
- •5.1. Основные понятия. Классификация
- •5.2. Физические основы фильтрации с образованием осадка. Гидродинамика течения жидкости через пористые и зернистые слои
- •5.3. Основное уравнение фильтрации
- •5.4. Определение оптимальных условий работы фильтров. Экономически выгодный цикл фильтрации
- •5.5. Применение уравнения фильтрации. Определение удельного сопротивления осадка и его сжимаемости
- •5.6. Фильтровальные перегородки
- •5.7. Конструкции фильтров. Периодически и непрерывно действующие. Классификация. Фильтры, работающие под давлением. Вакуум-фильтры. Способы снятия осадка
- •5.8. Выбор и расчет фильтров
- •5.9. Схемы подсоединения вакуум-фильтров
- •Контрольные вопросы
- •Глава 6. Агрегирование
- •6.1. Теория процесса агрегирования. Механизмы встреч частиц друг с другом. Понятие о расклинивающем давлении Теория процесса агрегации
- •Два механизма соударения или встречи частиц
- •6.2. Три слагающие поверхностных сил (расклинивающего давления). Двучленный закон взаимодействия
- •6.3. Силы Ван-дер-Ваальса. Слагающие сил Ван-дер-Ваальса. Ван-дер-ваальсово взаимодействие между молекулами и конденсированными фазами Силы Ван-дер-Ваальса
- •Электромагнитная теория взаимодействия конденсированных фаз
- •6.4. Природа ионно-электростатических сил. Закономерность изменения их вглубь раствора
- •6.5. Гидратационная слагаемая поверхностных сил (расклинивающего давления)
- •6.6. Три механизма агрегирования: коагуляция, флокуляция, мостиковая флокуляция
- •6.7. Основные принципы селективной агрегации частиц
- •6.8. Характеристика применяемых высокомолекулярных синтетических флокулянтов
- •Контрольные вопросы
- •Глава 7. Абсорбция
- •7.1. Общие сведения
- •7.2. Равновесие при абсорбции
- •7.3. Материальный и тепловой балансы процесса
- •7.4. Скорость процесса
- •Контрольные вопросы
- •Глава 8. Адсорбция
- •8.1. Общие сведения
- •8.2. Характеристики адсорбентов и их виды
- •8.3. Равновесие при адсорбции
- •8.4. Кинетика адсорбции
- •8.5. Десорбция
- •Контрольные вопросы
- •Глава 9. Флотация
- •9.1. Общие сведения
- •9.2. Теоретические основы процесса флотации
- •9.3.Флотационные реагенты и их классификация
- •9.4. Механизм действия собирателей
- •9.5. Реагенты-депрессоры
- •9.6.Реагенты-активаторы
- •9.7. Реагенты-регуляторы среды
- •9.8. Реагенты-пенообразователи
- •Контрольные вопросы
- •Глава 10. Экстракция
- •10.1 Процессы экстракции в системах жидкость-жидкость
- •10.1.1. Общие сведения
- •10.1.2. Равновесие в системах жидкость - жидкость
- •10.1.3. Методы экстракции
- •10.2. Процессы растворения и экстракции в системах твердое тело - жидкость
- •10.2.1. Общие сведения
- •10.2.2. Равновесие и скорость выщелачивания
- •Контрольные вопросы
- •Глава 11. Сушка
- •11.1. Основные понятия. Параметры, подлежащие расчету
- •11.2. Равновесное содержание влаги при сушке. Кинетика сушки. Понятие о напряжении объема сушилки
- •11.3. Основные параметры влажного воздуха
- •11.5. Изображение процессов изменения состояния воздуха на j - X на диаграмме
- •11.6. Материальный и тепловой балансы сушки
- •11.7. Расчет удельных расходов воздуха и тепла на сушку
- •11.8. Расчет сушилки в случае частичной рециркуляции обработанного воздуха
- •11.9. Сушка топочными газами
- •11.10. Конструкции сушилок
- •Контрольные вопросы
- •Литература
- •Оглавление
- •Глава 1. Основные законы термодинамики. Понятие энтропии как функции обесценивания энергии и стремления системы к хаосу 6
- •Глава 2. Классификация двухфазных систем 41
- •Глава 3. Отделение жидкости под действием механических методов 50
- •Глава 4. Применение центробежной силы при обезвоживании 75
- •Глава 5. Фильтрование 86
- •Глава 6. Агрегирование 117
- •Глава 7. Абсорбция 144
6.3. Силы Ван-дер-Ваальса. Слагающие сил Ван-дер-Ваальса. Ван-дер-ваальсово взаимодействие между молекулами и конденсированными фазами Силы Ван-дер-Ваальса
Как известно, силы Ван-дер-Ваальса точно передают взаимодействие отдельных молекул между собой и имеют три слагающие: ориентационную, индукционную и дисперсионную. Энергия взаимодействия соответственно имеет вид
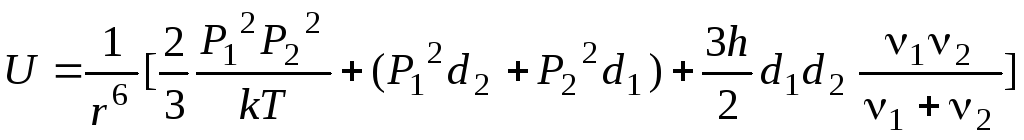 ,
,
где Р1 и Р2 - дипольные моменты молекулы 1 и 2; d1 и d2 - их поляризуемость; 1 и 2 - их собственные главные частоты молекул; h - постоянная Планка; К - постоянная Больцмана; Т - абсолютная температура.
Как видно, энергия
притяжения между двумя молекулами
убывает обратно пропорционально
![]() независимо от типа взаимодействия.
независимо от типа взаимодействия.
Первый член отражает ориентационные взаимодействия молекул, у которых есть постоянные «жесткие» диполи. В индукционном взаимодействии основную роль играет поляризуемость молекул, т.е. появление наведенных зарядов. Природа дисперсионного взаимодействия (третий член) - излучательная, связанная с одновременным появлением мгновенных диполей в молекулах (рис. 6.3).
Рис.6.3.
Конфигурация
притяжения (а) и отталкивания (б) двух
атомов водорода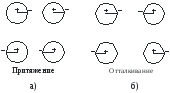
Ван-дер-ваальсово взаимодействие конденсированных фаз
Характерной особенностью сил Ван-дер-Ваальса является то, что они в отличие от валентных химических сил, не насыщаются. Поэтому взаимодействия между твердыми и жидкими телами, которые называют конденсированными фазами и которые состоят из множества атомов, можно в первом приближении рассматривать, как сумму независимых аддитивных взаимодействий между парами молекул или атомов, входящих в состав тел. Силы взаимодействия между конденсированными фазами увеличиваются, так как они являются суммой атомных и молекулярных взаимодействий.
В зависимости от геометрической формы взаимодействующих твердых частичек закон изменения сил Ван-дер-Ваальса с расстоянием имеет вид:
для двух шаров одинакового радиуса R:
![]() ;
;
для плоскости и шара:
![]() ,
,
![]() ;
;
для двух бесконечных плоскостей:
![]() ,
,
![]() .
.
Для расстояний между телами Н, больших, чем длина основной волны поглощения атомов , их образующих, энергия и сила притяжения убывают для этих случаев с расстоянием на порядок быстрее.
Например, для плоскостей уравнения запишутся в виде:
![]() ,
,
![]() .
.
Энергия Ван-дер-Ваальсовского взаимодействия зависит не только от формы твердого тела, но и от его размеров. Энергия взаимодействия двух пластин толщиной имеет вид:
![]() ,
,
где
![]() ;Н
- расстояние между пластинками.
;Н
- расстояние между пластинками.
При формула принимает обычный вид:
![]() .
.
Из хода зависимости U/U от R видно, что при R = /H = 10, т.е. только при очень близких расстояниях между частицами, поправка на размер частиц не существенна.
При = Н (U 0,5 U) энергия взаимодействия частиц конечного размера примерно вдвое меньше, энергии взаимодействия двух бесконечных полупространств. Поэтому сила прилипания к крупным частицам больше и, следовательно, повышение полидисперсности системы должно приводить к более интенсивной агрегации.
Интересно отметить, что аналогичный вывод был получен, когда рассматривали первую стадию образования агрегатов - стадию соударений.
Основная трудность практического использования этих формул заключается в том, что не известны константы А и А1.
