
- •Глава 9. Физико-химические
- •9.1. Анализ состава газовой фазы в зоне столба дуги
- •9.1.2. Образование соединений между компонентами газовой смеси
- •9.1.3. Насыщение расплавленного металла газами в капле и сварной ванне
- •9.2. Влияние атмосферных газов на свойства стали и сплавов при сварке
- •9.2.1. Влияние кислорода на свойства стали
- •9.2.3. Влияние водорода на свойства стали
- •9.2.4 Влияние со2, со и паров н2о на свойства стали
- •9.2.5. Влияние атмосферных газов на свойства цветных металлов
- •9.3. Взаимодействие металла с защитными флюсами при сварке
- •9.3.1. Строение и свойства сварочных флюсов
- •9.3.2. Характеристика важнейших простых оксидов, входящих в состав шлаковой фазы
- •9.3.3. Основные системы сварочных шлаков
- •9.4. Массообмен между расплавленным металлом, газовой средой и шлаком
- •9.5. Расплавление электрода и перенос капель в ванну
- •9.6. Источники водорода при сварке под флюсом
- •9.7. Окисление металла шва флюсом
- •9.8. Переход вредных примесей из флюса в металл шва
- •9.9. Раскисление металла при сварке
- •9.9.1. Виды раскисли тельных процессов
- •9.9.2. Легирование наплавленного металла
- •9.10. Рафинирование сварочной ванны и модифицирование металла шва
- •9.10.1. Влияние серы на структуру и свойства шва
- •9.10.2. Десульфурация сварочной ванны
- •9.10.3. Снижение содержания фосфора в металле шва
- •9.11. Дефекты металлургического происхождения в сварных швах
- •9.11.2. Шлаковые включения в металле шва
- •9.11.3. Ликвационная неоднородность в металле шва
Глава 9. Физико-химические
И МЕТАЛЛУРГИЧЕСКИЕ ПРОЦЕССЫ
ПРИ СВАРКЕ ПЛАВЛЕНИЕМ
Металлургические процессы при сварке плавлением протекают в более сложных условиях по сравнению с условиями выплавки сплавов, поскольку для сварки плавлением характерны:
аномально высокая температура (Т≥ Ткип) перегрева металла;
взаимодействие с газовой средой и флюсами, обладающими высокой химической активностью в условиях дугового разряда;
кратковременность существования металла в жидком реак-ционноспособном состоянии, ограничивающая эффективность типовых металлургических методов обработки металла для сохранения его качества;
одновременность процессов окисления, раскисления, легирования и рафинирования в сварочной ванне;
5) специфичность процессов направленной кристаллизации сварочной ванны, усиливающих ликвацию в металле шва и его структурную неоднородность.
В данной главе рассмотрим процессы взаимодействия металлов в зоне столба дуги с атмосферными газами и защитными средами, а также методы металлургического воздействия, которые позволяют сохранить исходные свойства различных металлов в сварном соединении.
9.1. Анализ состава газовой фазы в зоне столба дуги
Т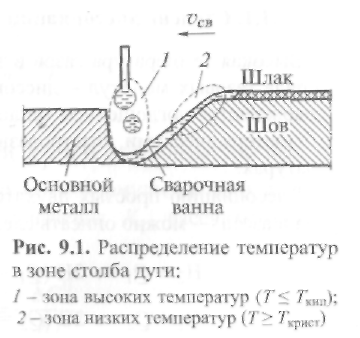 емпература
газов и паров в столбе дуги достигает
6000 К, что чрезвычайно усиливает их
химическую активность и интенсифицирует
процессы взаимодействия с металлами и
между собой отдельных компонентов
газовой среды. Кроме того, активация
взаимодействия газов с металлом
обусловлена высокой температурой
металла в месте сваривания. Принято
различать две зоны (рис. 9.1): зона1
высоких
температур, достигающих температуры
кипения, и зона 2
пониженных
температур, приближающихся к
температуре плавления. В высокотемпературную
зону входят капля на электроде, капля,
проходящая столб дугового разряда, и
активное пятно на передней стенке
сварочной ванны. Кроме того, взаимодействие
металла с газами в зоне дуги усиливается
электрическим потенциалом между
анодом и катодом и движением заряженных
газовых частиц в электрическом поле
дуги.
емпература
газов и паров в столбе дуги достигает
6000 К, что чрезвычайно усиливает их
химическую активность и интенсифицирует
процессы взаимодействия с металлами и
между собой отдельных компонентов
газовой среды. Кроме того, активация
взаимодействия газов с металлом
обусловлена высокой температурой
металла в месте сваривания. Принято
различать две зоны (рис. 9.1): зона1
высоких
температур, достигающих температуры
кипения, и зона 2
пониженных
температур, приближающихся к
температуре плавления. В высокотемпературную
зону входят капля на электроде, капля,
проходящая столб дугового разряда, и
активное пятно на передней стенке
сварочной ванны. Кроме того, взаимодействие
металла с газами в зоне дуги усиливается
электрическим потенциалом между
анодом и катодом и движением заряженных
газовых частиц в электрическом поле
дуги.
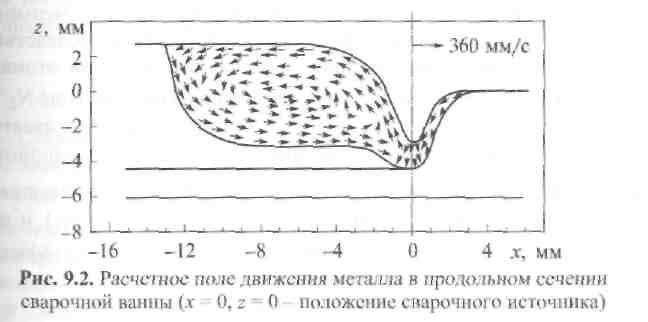
Чрезвычайно важную роль играет и интенсивное перемешивание жидкого металла сварочной ванны (рис. 9.2), увеличивающее площадь соприкосновения газа с жидким металлом и его распределение по объему в зоне пониженных температур. Физико-химические процессы в металле, протекающие с участием газовой среды, оказывают большое влияние на качество сварных соединений. Важнейшими из этих процессов являются диссоциация и ионизация газов, растворение газов в жидком металле, различные химические реакции в самой газовой среде и при ее взаимодействии с металлом.
9.1.1. Степень диссоциации атмосферных газов в дуге
Высокая температура газов в зоне сварки создает условия для распада газовых молекул - диссоциации газов. Эти процессы сопровождаются поглощением теплоты Q диссоциации, т. е. являются эндотермическими, быстроразвивающимися при высоких температурах.
Диссоциацию простых двухатомных газов — водорода, кислорода и азота — можно описать следующими уравнениями:
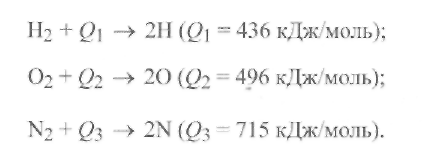 (9.3)
(9.3)
Отсюда следует, что поскольку энергия Q3 , затрачиваемая на диссоциацию молекулы азота, имеет наибольшее значение, его молекула - самая прочная. Азот должен диссоциировать в меньшей степени, чем кислород и водород в тех же условиях. Вследствие более интенсивной диссоциации парциальные давления атомарных частиц О2 и Н2 в смеси выше, чем парциальное давление N2.
Степень диссоциации для данной температуры описывается константой равновесия Кp Для процесса диссоциации, например водорода (см. (9.1)), при постоянном давлении р она равна отношению парциальных давлений продукта диссоциации (рH) и исходного продукта (рH2 ) с учетом стехиометрических коэффициентов, т. е.
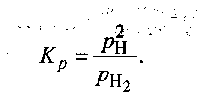 (9-4)
(9-4)
Если учесть, что при степени диссоциации а один объем газа Н2 превращается в смесь, состоящую из полученных продуктов распада (2α) и остатка исходных веществ (1 - α), то согласно расчетам, выполненным в разд. 8.9,
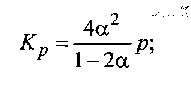 (9.5)
(9.5)
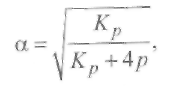
где р - внешнее давление.
Для определения зависимости Кp и α от температуры используют типовые реакции, номограммы и формулы диссоциации газов, приведенные в табл. 8.4, а значения Кp рассчитывают по формуле Вант-Гоффа (8.42):
![]()
![]()
Для вычисления Кp также используют эмпирические формулы, например для реакции диссоциации молекулярного водорода -приближенное уравнение Нернста
![]() (9.7)
(9.7)
Следовательно, задавая значения температуры при постоянном давлении р, можно по эмпирической формуле для соответствующего газа вычислить величину Кp, а затем, пользуясь выражением (9.6), - и степень диссоциации этого газа при выбранной температуре. Если принять, что температура газов в столбе дуги составляет в среднем 5000 К, то в результате расчетов получим: Для молекул водорода α = 0,96, а для молекул азота α = 0,038.
На рис. 8.9, а приведены графические зависимости степени Диссоциации некоторых газов и паров в зоне столба дуги от температуры. Из рисунка следует, что при температуре выше 5000 К все представленные газы и пары имеют значительную степень Диссоциации, т. е. находятся в активном реакционном состоянии.
Диссоциация двухатомных газов в зоне сварки имеет большое значение по следующим причинам:
- в атомарном состоянии газы приобретают высокую химическую активность и легко взаимодействуют с расплавленным металлом капель и сварочной ванны;
атомы газа в зоне столба дуги после диссоциации претерпевают термическую ионизацию. Они становятся ионами и перемещаются в соответствии со своими зарядами к аноду или катоду, т. е. к электроду или к сварочной ванне, что усиливает их растворимость в металле. Зависимость степени термической ионизации различных газов и паров в среде дугового разряда от температуры, полученная по уравнению Саха, приведена на рис. 8,9, б;
параллельно с диссоциацией газов, протекающей в зоне высоких температур с поглощением тепла, вблизи сварочной ванны, где температура значительно ниже, идет обратный процесс образования молекул из ионов атомов, сопровождающийся выделением тепла. Благодаря этим двум процессам осуществляется своеобразное регулирование теплового состояния в зоне сварки - перенос тепла от участка высоких температур столба дуги к жидкому металлу сварочной ванны, имеющему меньшую температуру.
Аналогично диссоциации двухатомных газов протекает диссоциация трехатомных газов, которые в сварочных процессах обычно представлены водяным паром и углекислым газом, входящими в состав атмосферы. Водяной пар диссоциирует по реакции:
![]() (9.8)
(9.8)
для которой зависимость между степенью диссоциации и константой равновесия представлена в виде номограммы на рис. 8.8.
Кроме того, константа равновесия реакции (9.8) при р = 1 может быть подсчитана по эмпирическому уравнению Чипмена -Самарина:
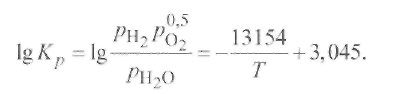 (9.9)
(9.9)
Приняв во внимание, что одновременно при диссоциации выделяются водород и кислород, можно заключить, что диссоциация водяных паров в зависимости от условий протекания реакции (9.8) без участия атмосферного кислорода будет создавать для различных металлов окислительный или восстановительный характер среды. Если упругость диссоциации кислорода, выделяющегося из водяного пара, превышает упругость диссоциации кислорода из оксида металла (рH2O O2 > рMeOO2 ), металл будет окисляться за счет кислорода диссоциированного водяного пара:
![]() H2O
H2O
Если же упругость диссоциации кислорода из водяного пара меньше упругости диссоциации кислорода из оксида металла (рH2OO2< рMeOO2 ), реакция будет идти в обратном направлении, т. е. металл будет восстанавливаться из оксида водородом диссоциированного водяного пара:
![]()
С повышением температуры степень диссоциации водяных паров увеличивается и при 5000 К приближается к единице. Следует учесть, что обычно концентрация водяного пара в воздухе не является достаточной, чтобы обеспечить восстановление металлов. Однако сварка в специально полученном так называемом сухом водяном паре, не содержащем атмосферного кислорода, в принципе возможна - для углеродистых сталей.
Углекислый газ при высоких температурах также активно диссоциирует по реакции
![]() (9.10)
(9.10)
Зависимость константы равновесия реакции (9.10) от температуры определяется по формуле Вант-Гоффа (8.42) либо при р = 1 по уравнению Чипмена - Самарина
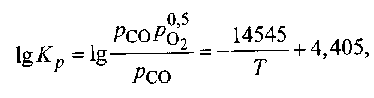 (9.11)
(9.11)
где рCO, рO2, рCO2 - парциальные давления соответственно газов
СО, O2 и СO2.
И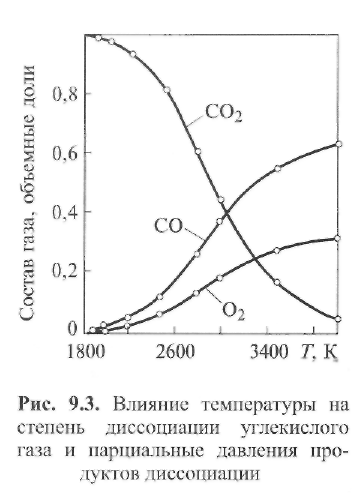 так,
задавая значения температуры, с помощью
уравнений (9.11) и (9.6) или номограммы (см.
рис. 8.8) можно определить константы
равновесия, степень диссоциации и
соответствующий состав газов. На рис.
9.3 приведен результат таких расчетов
для интервала 1800...4000 К. Как видим, в
области температур около 4000 К углекислый
газ почти полностью диссоциирован, а
вблизи поверхности сварочной ванны
(при температуре 1800...2000 К) его степень
диссоциации незначительна.
так,
задавая значения температуры, с помощью
уравнений (9.11) и (9.6) или номограммы (см.
рис. 8.8) можно определить константы
равновесия, степень диссоциации и
соответствующий состав газов. На рис.
9.3 приведен результат таких расчетов
для интервала 1800...4000 К. Как видим, в
области температур около 4000 К углекислый
газ почти полностью диссоциирован, а
вблизи поверхности сварочной ванны
(при температуре 1800...2000 К) его степень
диссоциации незначительна.
В![]() зависимости от соотношения упругости
диссоциации кислорода из оксида и
из СO2
направление реакции (9.10) определяет
окислительный или восстановительный
характер среды, создаваемой для жидкой
сварочной ванны при диссоциации
углекислого газа. Если упругость
диссоциации кислорода из оксида
металла меньше, чем из углекислого
газа, то в среде будут развиваться
окислительные процессы, т. е.
зависимости от соотношения упругости
диссоциации кислорода из оксида и
из СO2
направление реакции (9.10) определяет
окислительный или восстановительный
характер среды, создаваемой для жидкой
сварочной ванны при диссоциации
углекислого газа. Если упругость
диссоциации кислорода из оксида
металла меньше, чем из углекислого
газа, то в среде будут развиваться
окислительные процессы, т. е.
![]()
При обратном
соотношении упрутостей![]() диссоциации
та же среда проявляет восстановительные
свойства:
диссоциации
та же среда проявляет восстановительные
свойства:
![]()
Парциальное давление кислорода в реакции (9.10) зависит от температуры, давления и соотношения концентраций СO2 и СО, т. е.
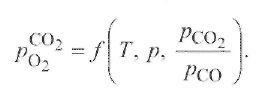
![]() (9.12)
(9.12)
Это значит, что с увеличением температуры Т и отношения а также согласно выражению (9.6) при уменьшении давления р в системе растет окислительная способность диссоциирующего углекислого газа. Лишь при дуговой сварке неплавящимся, но испаряющимся угольным электродом наличие паров твердого углерода весьма существенно снижает эту способность, так как энергично развивается реакция
![]() (9.13)
(9.13)
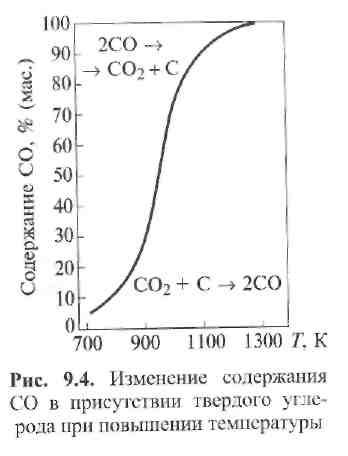
На рис. 9.4 дан график зависимости содержания СО от температуры в присутствии паров твердого углерода. Уже при температуре 1100 К содержание СО в газовой смеси приближается к 100 %. Следовательно, создается восстановительная для металла среда и становится возможной, например, реакция восстановления оксидов железа:
![]()
Поэтому при сварке сталей угольным электродом не требуется дополнительной защиты газом или флюсом.
