
- •1. Химия ғылымының пайда болуы, дамуы және маңызы
- •2. Иондық байланыс Мысалдар 169 бет
- •3. Алюминий гидроксиді (Al(oh)3) құрамындағы элементтердің массалық үлесін есепте
- •1 Заттардың және олардың физикалық қасиеттері
- •2 Ковалентті байланыс дегеніміз не? Мысалдар.
- •3 Темір (III) оксидінің Fe2o3 40 грамында қанша грам темір бар екендігін табыңдар
- •1 Атом молекулалық ілімнің қағидаларын мысалдар келтіре отырып осы ілімнің қалыптасуына қай елдің ғалымдарының үлесі болды?
- •2 Атомның құрамы және құрылысы 143, 145 бет
- •3 Алюминий оксидінің Al2o3 қандай массасында 15.5 г алюминий болады
- •1. Атомдар, молекулалар дегеніміз не? 44 бет
- •2. Тотығу тотықсыздану реакциялары мысалдар 144 бет
- •1. Химиялық элементтер, олардың таңбалары және атауы. Оны кім шығарды?
- •2. Экзотермиялық және эндотермиялық реакциялар дегеніміз не?
- •3. 1.5 Моль натрий сульфаты Na2so4 берілген. Осы тұздың массасын тап.
- •1. Жай және күделі заттар. Салыстырмалы атомдық масса. Салыстырмалы молекулалық масса анықтама және мысал келтір
- •2. Негіздер: құрамы, жіктелуі, химиялық қасиеттері, алынуы. 119 бет
- •1. Химиялық формула. Химиялық элементтердің валенттілігі дегеніміз не және валенттілік термині нені білдіреді? 35 бет.
- •2. Қышқылдар: құрамы, жіктелуі, химиялық қасиеттері, алынуы.Мысал келтір 87, 90, 122 бет
- •Қышқылдардың химиялық қасиеттері
- •3. Массасы 22г көмірқышқыл газының зат мөлшерін есепте.
- •1. Физикалық және химиялық құбылыстар дегеніміз не және айырмашылығы Химиялық реакциялар. Мысалдар
- •2. Оксидтер: алынуы, жіктелуі, химиялық қасиеттері. 114-116 бет.
- •Жай және күрделі заттарды жағу арқылы:
- •3. Құрамындағы элементтердің массалық үлесі мынадай: к39.69% Mn 27.87% o 32.46% тұздың қарапайым формуласын есепте.
- •1. Сутекке жалпы сипаттама. Алыну жолдарын реакция теңдеуі арқылы өрнекте.
- •2. Сілтілік металдар және галогендердің периодтық жүйеге орналасуы. Мысалдар.
- •3. 30Г тұзды 170г суда еріткенде түзілетін ерітіндідегі тұздың массалық үлесі қандай болады?
- •1. Химиялық реакциялардың теңдеулері, зат массасының сақталу заңы.
- •2. Натрий пжо (периодтық жүйедегі орны) және оның маңызды қосылыстары. Мысалдар
- •2. Оттектің аллотропиясы деген не? Озон және озон қабатының жердегі тіршілік үшін маңызы қандай?
- •3. CuSo4 5h2o-ның салыстырмалы молекулалық массасын есепте.
- •1. Химиялық элементтердің қасиеттерінің периодтық орны бойынша сипаттамасы Периодтық жүйедегі орнына қарай элементті және оның қосылыстарын сипаттау
- •Химиялық элементтердің электртерістілігі
- •2. Хлор пжо (периодтық жүйедегі орны) бойынша сипатта. Олардың маңызды қосылыстарының мысалдары
- •Химиялық қасиеттері
- •Cl2-нің алынуы және қолданылуы
- •1. Атомның құрамы және құрылысы дегеніміз не? Ол қандай бөлшектерден тұрады?
- •Мазмұны
- •Электрон
- •Атом құрылысы[өңдеу]
- •2. Тұздар: құрамы, жіктелуі, қасиеттері, алынуы 92 бет.
- •3. 20%-Тік 500г ерітінді даярлау үшін қанша грамм тұз қанша грамм су қажет?
- •1. Химиялық элементтердің жіктелуі мысалдар келтіріп заттардың формуласын жазыңдар.
- •2. Жай және күрделі заттардың жіктелуі. Генетикалық байланысты қалай қалпына келтіруге болады? Металдар және бейметалдар.
- •3. Массасы 12,6 г азот қышқылын бейтараптау үшін мыс(II) гидроксиді қанша массасы және мөлшері қажет екенін есептеңдер.
- •1. Химиялық элементтердің электр терістігі ұғымдарының айырмасы неде?
- •2. Ерігіштік дегеніміз не? Ерігіштік өлшемін қандай шам алар арқылы анықталады?
- •3. Массасы 620г натрий оксиді әрекеттескенде сілтінің қандай массасы және қанша мөлшері түзілетінін есептеңдер.
- •1. Заттың аморфты және кристалды жүйелері
- •2. Ерітінділер концентрациясы дегеніміз не және оны қандай тәсілдермен көрсетуге болады? Тұздардың алыну жолдары ...
- •3. Массасы 7,4 г кальций гидрооксиді қанша грамм фосфор қышқылымен әрекеттеседі.
- •1. Кристалл торларының түрлері және оның түйіндері дегеніміз не? Заттардың қасиеттерінің құрылысына тәуелділігі
- •2. Отттекті зертханада қалай алуға болатынын түсіндір.
- •3. Массасы 4,6 г натрийді 150 г суда еріту арқылы алынған ерітіндідегі натрий сілтісінің массалық үлесі
- •1. Ауа-газдар қоспасын қалай түсінесің? Атмосфералық ауаны ластанудан қалай қорғаймыз?
- •2. Зертханада хлордың алыну жолдарын реакциялар теңдеуі арқылы өрнекте.
- •3. Массасы 28 г. Литий суда ерігенде сутектің қанша көлемі түзіледі?
- •1. Оттегі химиялық элементінің аллотропиясы қалай аталады? Қандай зат екендігін түсіндір.
- •2. Тотықтырғыш және тотықсыздандырғыш туралы түсінік
- •3. Массасы 0,1 моль барий хлориді қанша моль күкірт қышқылымен әрекеттесе алады?
- •1. Табиғаттағы судың маңызы және физикалық/химиялық қасиеті және қолданылуы
- •2. Химиялық реакцияның жылу эффекті деген не? Өлшем бірлігі
- •3. 50 Г 16%-тік сілті ерітіндісін дайындау үшін қанша грамм сілті алу керек?
- •1. Табиғаттағы тірі организмдердегі және адам тіршілігіндегі химиялық реакциялардың биологиялық маңызы қандай? Мысал келтір.
- •2. Изотоп деген не? Сутектің изотоптары қалай аталады? Молекулалық фолрмуласын жаз және аттарын ата.
- •3. 78 Г калий сумен әрекеттескенде калий гидроксидінің қандай массасы және қанша мөлшері түзіледі?
- •1. Химиялық элементтердің тірі және өлі табиғатта таралуы. HCl физикалық-химиялық реакция теңдеуі.
- •2. Зат мөлшері деген не? Өлшем бірлігі. Авагадро саны нені көрсетеді?
- •3. Дәріханада 500 г 9%-тік ерітінді дайындау үшін ас тұзының және судың қандай массасы қажет?
- •1. Бейтараптану реакциясын теңдеулер арқылы көрсет
- •2. Бейорганикалық қосылыстар арасындағы генетикалық байланыс деген не? Мысалдарды теңдеу арқылы өрнекте.
- •1. Галогендердің атом құрылысы қандай агрегаттық күйінде қандай заңдылықтар болады?
- •2. Металдардың кернеу қатарын және оны қалай түсінесің?
Химиялық қасиеттері
Химиялық белсенді, өте күшті тотықтырғыш:сутегімен реакцияласады,металдармен және бейметалдармен де реакцияласады: 3Cl2 + 2Fe = 2FeCl2 2Cl + Si = SiCl4
Суда және сілтілердің судағы ерітінділерінде дисмутацияланады: Cl2 + 2NaOH(суық) = NaClO + NaCl + H2O 3Cl2 + 6NaOH(ыстық) = NaClO3 + 5NaCl + 3H2O
Cl2-нің алынуы және қолданылуы
Хлорды алу: a) өнеркәсіпте 2KCl(балқыма) → 2K + Cl2↑ 2NaCl + 2H2O→ H2↑+Cl2↑ + 2NaOH
ә) зертханада 1) 4HCl(конц.) + MnO2 = Cl2↑ + MnCl2 + 2H2O 2) 16HCl(конц.) + 2KMnO4 = 5Cl2↑ + 2MnCl2 + 8H2O + 2KCl 3) 4HCl(конц.) + Ca(ClO)2 = 2Cl2↑ + 32H2O + CaCl2 4) 6HCl(конц.) + KClO3 = 3Cl2↑ + 3H2O + KCl
Конмутация (3) және (4) реакцияларында әрі тотықсыздандырғыш HCl, әрі тотықтырғыштар Ca(ClO)2 және KClO3 хлор берушілер болып келеді.Хлор - негізгі химиялық өндіріс өнімдерінің бірі, бром мен йодты, хлоридтерді, құрамында оттегі бар туындыларды алу үшін қолданылады. Қағазды ағартады, ауыз суды дезинфекциялауға пайдаланады.
3. 72г суды айырғанда шығатын сутек пен оттектің массасын табыңдар
Шешуі:
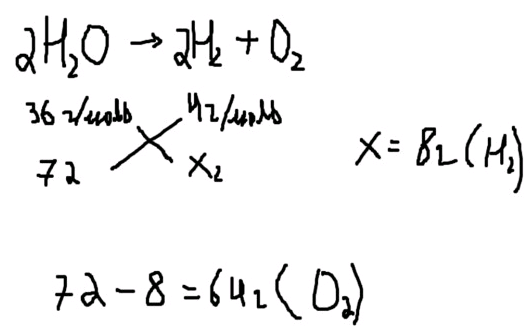
№14 Билет
1. Атомның құрамы және құрылысы дегеніміз не? Ол қандай бөлшектерден тұрады?
том құрылысы - 1897 жылы көптеген электр құбылыстарын түсiндiруге мүмкiндiк беретiн жаңалық ашылды. Ағылшын ғалымы Дж. Дж. Томсонэлементар заряд тасымалдаушысы болып табылатын бөлшектi тапты. Бұл бөлшектіэлектрондеп атады.[1][2]
Мазмұны
1 Электрон
2 Атом құрылысы
3 Басты фактілер
4 Дереккөздер
Электрон
Электрон массасы m=9,1*10-31 кг-ға тең және табиғаттағы ең жеңiл сутегi атомы массасынан 3700 еседей аз болып шықты. Электр зарядын арттыруға және азайтуға болады. Яғни олар әр түрлі мәнге ие болуы мүмкін. Ендеше электр заряды физикалық шама. Екіэлектрометралып олардың біреуін зарядтайық. Сосыноқшаулағыш тұтқасыбар жіңішке сыммен екі электрометрді жалғайық. Сонда біз зарядтың теңдей екіге бөлінгенін көре аламыз. Атом құрылысы1911жылы ағылшын ғалымыЭ. Резерфордбасқарған тәжiрибелер нәтижесiнде ашылған. Электрон заряды терiс: qэл= – е = – 1,6 • 10–19(дәрежесі) Кл.
Бұл заряд электронның ерекше сипаттамасы болып табылады. Жәй денелердi зарядтауға немесе разрядтауғаболады, ал электронды зарядынан “айыру” мүмкiн емес. Сондай-ақ электрон зарядын азайтуға немесе көбейтуге болмайды. Электрон заряды барлық уақытта тек бiр мәнге ие.Химиякурсынан сiздер электронның атом құрамына кiретiнiн бiлесiздер. Электрондар атом ішінде орналасқан оң зарядталған атомдық ядроны айнала қозғалады. Резерфорд тәжiрибелерiн жоғары сыныптарда егжей-тегжейлi қарастырылады. Мұнда бiз оның тәжiрибе нәтижесiнде жасаған қорытындыларымен шектелемiз.[3]
Атом құрылысы[өңдеу]
Резерфорд атомының құрылысын Күн жүйесiнеұқсатты. Күн жүйесiндегiпланеталароған тартылып айналғаны сияқты, электрондар даядроғатартылып оны айнала қозғалады. Осындай ұқсастығы үшiн Резерфорд ұсынған модельдi планетарлық модель деп атаған. Ядро мен электронның ара қашықтығы олардың өлшемдерiне қарағанда өте үлкен. Егер атомды ойша үлкейткенде ядроның диаметрi он теңгелiктей болса, онда ядро мен электрон ара қашықтығы шамамен бiр километрдей болар едi. Егер барлық электрондар атомдық ядроларға тығыз орналасса, онда ересек адамның денесiнiң көлемi бiр куб миллиметрдiң миллионнан бiр бөлiгiндей болатындығы есептелген. Бұдан адам денесiнiң 99%-ын (кез-келген дененiң) бостық жайлайтындығын көремiз. Бiртектi атомдаржиынтығыхимиялық элементдеп аталады. Әр түрлi химиялық элементтердiң атомдары бiр-бiрiненядроларының зарядыменжәне сол ядроны айнала қозғалатын электрондар санымен ерекшеленедi. Мысалы,сутегi атомындажалғыз электрон бар,оттегi атомында– сегiз электрон, алуран атомында– тоқсан екi. Атомдағы электрондар саны элементтiңД.И. Менделеевкестесіндегі реттiк нөмiрiмен сәйкес келедi. Осы нөмiр атом ядросының зарядын да анықтайды. Белгiлеу енгiзейiк: Z – элементтiң реттiк нөмiрi, е = атомдағы электрондар саны. Онда атом ядросының және атомдағы барлық электрондардың жалпы заряды үшiн былай жазуға болады:qядро = + Ze, qэл-н = – Ze. Атомдағы электрондардың жалпы зарядын, атом ядросының зарядына қоссақнөлшығады. Бұл атомның толықтай бейтарап екендiгiн көрсетедi. Бейтарап атомдардан тұратын заттардыңмолекулаларыда бейтарап болады. Кейбiр жағдайларда (мысалы, соқтығысқанда) атомдар бiрнеше электронын жоғалтуы мүмкiн. Атомдар электрондармен бiрге өздерiнiң терiс зарядының бiр бөлiгiн жоғалтып, бейтарап емес жүйеге айналады. Осының салдарынан пайда болған оң зарядталған атомдыоң иондеп атайды. Керi жағдайлар да болуы мүмкiн: бейтарап атом өзiне артық электрон қосып алып, терiс зарядталады. Мұндай атомдытерiс иондеп атайды.
