
химия 2009
.doc$$$ 1
100 мл ерiтiндiде 4,9 г H2SO4 (M(Н2SO4)=98 г/моль) бар болса, осы ерiтiндiнiң нормалдығы қандай?
А)1н;
В)0,02н;
С)2н;
D)0,1н;
Е)0,5н.
$$$ 2
Ерiтiндiнiң эквиваленттiк концентрациясын анықтаңыз, егер 100 мл ерiтiндiде 6,3 г HNO3 болса.
А)0,5;
В)1,0;
С)2,0;
D)0,1;
Е)0,2.
$$$ 3
6,8 г күкіртсутектің көлемін анықтаңыз (қ.ж.).
А)1,2 л;
В)2,4 л;
С)3,2л;
D)5,6л;
Е)4,48л.
$$$ 4
0,01 М HNO3 ерітіндісінің рОН мәнін есептеңіз.
А)10;
В)12;
С)8;
D)2;
Е)6.
$$$ 5
Ерiтiндi сiлтiлiк орта болатын тұзды көрсетiңiз.
А)K2SO4;
В)K2CO3;
С)MgSO4;
D)CuCl2;
Е)NaNO3.
$$$ 6
Гидролизге ұшырамайтын тұзды көрсетiңiз.
А)KNO3;
В)K2S;
С)MgSO4;
D)AlCl3;
Е)Na2CO3.
$$$ 7
Әлсiз электролиттi көрсетiңiз.
А)HNO3;
В)NaOH;
С)Al(OH)3;
D)Na2SO4;
Е)KCl.
$$$ 8
Na3PO4 толық диссоциацияланғанда түзiлетiн ион саны:
А)2;
В)3;
С)4;
D)6;
Е)5.
$$$ 9
Берiлген заттардың қайсысы гидролизiнде қышқыл тұз түзiледi?
А)KNO3;
В)CuSO4;
С)NiCl2;
D)K2S;
Е)Na2SO4.
$$$ 10
Құрамында 50 г тұзбен 200 г суы бар ерiтiндiдегi тұздың массалық ұлесiн (%) есептеңiз.
А)50;
В)20;
С)10;
D)25;
E)15.
$$$ 11
20%-тiк ерiтiндi дайындау үшiн 400 г суда NaNO3-тiң қандай мөлшерiн ерiту керек?
А)50 г;
В)400 г;
С)200 г;
D)100 г;
Е)150 г.
$$$ 12
Қайсы тұз ерiтiндiсi гидролизденгенде сiлтiлiк орта (рН>7) болады?
А)CuSO4+HOH®
В)MgCl2+HOH®
С)KNO3+HOH®
D)CH3COONa+HOH®
Е)Na2SO4+HOH®
$$$ 13
Қайсы тұз ерiтiндiсi гидролизденгенде қышқыл орта (рН<7) болады?
А)Na2CO3;
В)K2SO4;
С)CuCl2;
D)NaCl;
Е)FeS.
$$$ 14
Ерiтіндiнiң рОН-ы 3-ке тең болса, сутегi иондары концентрациясы неге тең?
А)10-3;
В)10-5;
С)10-7;
D)10-9;
Е)10-11.
$$$ 15
Құрамында 3,46 г мочевина (CO(NH2)2), 100 мл суы бар ерiтiндiнiң қайнау температурасын анықтаңыз. Судың эбулиоскопиялық константасы 0,520 (Е=0,520С).
А)100,8;
В)100,3;
С)103,0;
D)100,5;
Е)97,0.
$$$ 16
Кальций сульфатының ЕК математикалық өрнегі қайсы?
А)![]()
Ca2+][SO42-];
Ca2+][SO42-];
В)
![]()
Ca+2SO-2;
Ca+2SO-2;
С)
![]()
Ca+2SO4-22;
Ca+2SO4-22;
D)
![]()
Ca+22SO4-2;
Ca+22SO4-2;
Е)
![]()
Ca+22SO4-22.
Ca+22SO4-22.
$$$ 17
Көлемі 200 мл ерітіндідегі сахарозаның (С12Н22О11) массасы қандай, егер 00С-да оның осмос қысымының мәні 6,61105 Па тең болса.
А)169,7г;
В)19,93г;
С)12,34г;
D)23,45г;
Е)34,56г.
$$$ 18
Массасы 5,0 г затты 200 г суда ерiту нәтижесiнде электр тогын өткiзбейтiн және кристалдану температурасы -1,450С-тең ерiтiндi алынады. Ерiген заттың молекулалық массасын (г/моль) анықта. Судың криоскопиялық тұрақтысы 1,860 тең.
А)20;
В)24;
С)30;
D)32;
Е)38;
$$$ 19
Қайсы электролит диссоциацияланғанда гидроксокатион түзiледi?
А)CuSO4;
В)NaHCO3;
С)Al(Ac)3;
D)CuOHCl;
Е)NaH2PO4.
$$$ 20
Қайсы электролит диссоциацияланғанда гидроанион түзiледi?
А)AlOHCl2;
В)Na2SO4;
С)NH4OH;
D)(CuOH)2SO4;
Е)Na2HPO4.
$$$ 21
Қайсы түз ерiтiндiсiнiң гидролизiнде реакция ортасы нейтралды болады, яғни рН=7?
А)NaHCO3;
В)NH4CN;
С)Cu(NO3)2;
D)K2S;
Е)AlCl3.
$$$ 22
Күшті электролитті көрсетіңіз.
А)HNO3 a=94 %;
В)СН3СОOH a= 2 %;
С)НCN a=0,15 %;
D)NH4OH a=1,35 % ;
Е)H2CO3 a=0,17 %.
$$$ 23
Қайсы реакция ерімейтін қосылыс түзе жүреді?
А)Ni(OH)2+HNO3®…
В)CaCO3+HCl®…
С)Zn(OH)2+NaOH®…
D)FeCl3+NaOH®…
Е)H2SO4+KOH®…
$$$ 24
Қайсы зат ерiтiндiсiнде күмiс ионы (Ag+) көп мөлшерде, егер ол заттардың ерiгiштiк көбейтiндiсi (ЕК) белгiлi болса?
А)AgBr 7,710-13;
В)AgCl 1,710-10;
С)Ag2CO3 5,710-12;
D)AgCN 1,010-21;
Е)Ag2S2O3 1,010-28.
$$$ 25
Берiлген схемадан, тотығу процесiн көрсетiңiз.
А)NO2-®NO3-;
В)SO42-®SO32-;
С)Cl2®2Cl-;
D)MnO4-® MnO2;
Е)Cu2+®Cu0.
$$$ 26
Берiлген схемадан тотықсыздану процесiн көрсетiңiз.
А)SO32-® SO42-;
В)S2-®S0;
С)MnO4-®MnO2;
D)NH3®NO3- ;
Е)Cr3-®Cr0.
$$$ 27
Азоттың төменгi және жоғарғы тотығу дәрежесi неге тең?
А)-3; +5
В)-3; +3
С) 0; +5
D)+2; +4
Е)+1; +5
$$$ 28
Орталық ионының тотығу дәрежесi “+6” болатын қосылысты көрсетiңiз.
А)HNO3;
В)KMnO4;
С)K2Cr2O7;
D)H2S;
Е)H2O2.
$$$ 29
P+H2O®H3PO3+PH3 реакция қай типiне жатады:
А)молекулааралық;
В)ішкімолекулалық;
С)тотығу-тотықсыздануға жатпайды;
D)диспропорциалану;
Е)орынбасу реакция.
$$$ 30
Mg+HNO3®Mg(NO3)2+NH4NO3+H2O реакция теңдеуiн аяқтап, тотықсыздандырғыш алдындағы коэффициентiн анықтаңыз:
А)2;
В)4;
С)8;
D)10;
Е)12.
$$$ 31
Тотығу процесiн көрсетiңiз.
А)H3AsO3®H3AsO4;
В)As2O5®As2O3;
С)As2O3®AsH3;
D)H3AsO4®As2O5;
Е)As2O3®HАsO2.
$$$ 32
AgNO3 ерiтiндiсiнен массасы 108 г күмiстi 6 мин iшiнде бөлiп алу үшiн кандай ток күшiн жұмсау керек?
А)670А;
В)268А;
С)123А;
D)78А;
Е)90А.
$$$ 33
Мырышты-күмiстi гальваникалық элементтiң стандартты Э.Қ.К. (В) есептеңiз.
Е0(Zn2+/Zn)=-0,76B. E0(Ag+/Ag)=+0,80B.
А)+1,56;
В)-1,56;
С)+0,04;
D)-0,04;
Е)0.
$$$ 34
Mg(NO3)2 тұзы ерiтiндiсi электролизiнде анодта бөлiнетiн затты көрсетiңiз
А)Mg;
В)O2;
С)H2;
D)NO;
Е)NO2.
$$$ 35
Қай электродтың стандартты потенциалы нөлге тең деп алынады?
А)медного;
В)кислорода;
С)водородного;
D)каломельного;
Е)золотого.
$$$ 36
0,01М ZnSO4 тұзы ерiтiндiсiндегi мырыштың электрод потенциалын есептеңiз
E0(Zn2+/Zn)=-0,76B.
А)+0,10;
В)-0,10;
С)-0,82;
D)+0,82;
Е) 0.
$$$ 37
Фарадей заңы бойынша электролиз кезiнде зат массасы қандай формуламен анықталынады?
А)m=V;
В)m=It;
С)m=PMV/RT;
D)m=rV;
Е)m=M(X)n(X).
$$$ 38
AuCl3 ерiтiндiсiн 30 минут бойы электролиздегенде катодта 0,5 г Au бөлiну үшiн қажеттi ток күшiн анықтаңыз .
А)0,1А;
В)0,2А;
С)0,4А;
D)0,6А;
Е)1,0А.
$$$ 39
Қай тұз ерітіндісі электролизденгенде анодта О2 бөлініп шығады.
А)CuCl2;
В)NaI;
С)NaBr;
D)KCl;
Е) K2SO4.
$$$ 40
Қай қатарда тек амфотерлі гидроксидтер жазылған?
А)Mn(OH)2, Cu(OH)2, Mg(OH)2;
В)Be(OH)2, Zn(OH)2, Cr(OH)3;
С)Co(OH)3, Fe(OH)3, Al(OH)3;
D)KOH, NH4OH, LiOH;
Е)NaOH, AgOH, AuOH;
$$$ 41
S(к)+O2(г)=SO2(г) гетерогенді реакцияның жылдамдығына сәйкес келетін өрнектердің қайсысы дұрыс?
А)
= k CS![]() ;
;
В)
= k ![]() ;
;
С)
= k CS+![]() ;
;
D)
= k ![]() ;
;
Е)
= k CS![]()
![]() .
.
$$$ 42
Берiлген реакция бойынша Н3РО4+Са(ОН)2=СаНРО4+2Н2О фосфор қышқылының эквивалентiнiң молярлық массасын (г/моль) табыңыз:
А)49;
В)32,7;
С)196;
D)98;
Е)16,3.
$$$ 43
Газдың ауа бойынша тығыздығы 2,2 тең. Осы газдың салыстырмалы молекулалық массасын табыңыз. Мауа=29 г/моль.
А)49;
В)29;
С)64;
D)36;
Е)56.
$$$ 44
Оттегiнiң және сутегiнiң эквиваленттік көлемдерiн анықтаңыз (қ.ж.)?
А)11,2 л/моль и 5,6 л/моль;
В)11,2 л/моль и 11,2 л/моль;
С)11,2 л/моль и 22,4 л/моль;
D)22,4 л/моль и 22,4 л/моль;
Е)22,4 л/моль и 11,2 л/моль.
$$$ 45
56 г азоттың (N2) қ.ж. моль санын көрсетiңiз.
А)2,0;
В)1,0;
С)2,5;
D)3,0;
Е)3,5.
$$$ 46
Қайсысында қ.ж. молекула саны көп болады.
А)10 г N2;
В)10 г O2;
С)10 г SO3;
D)10 г NH3;
Е)10 г SO2.
$$$ 47
Вант-Гофф ережесiне сәйкес, температураны әрбiр 100С-ке көтергенде реакция жылдамдығы?
А)өзгермейді;
В)2-4 есе өседі;
С)төмендейді;
D)10-20 есе артады;
Е)5-10 есе төмендейді.
$$$ 48
Ковалентті полюссіз байланыс қай келтірілген затта болады:
А)НF;
B)NaOH;
C)H2S;
D)H2;
E)H2O.
$$$ 49
Электрондық формуласы …4s24p3 элемент қай топта орналасқан?
А)1;
В)2;
С)5;
D)4;
Е)3.
$$$ 50
Кеңiстiкте электрон бұлтының пiшiнiн көрсететiн квант саны қалай аталады:
А)орбитальдік;
В)спиндік;
С)магниттік;
D)бас квант саны;
Е)қосымша.
$$$ 51
Әрекеттесушi атомдардың ядросын қосатын сызықтың бойымен атомдық орбитальдардың қабысуынан түзiлетiн коваленттiк байланыс қалай аталады:
А)ковалентті полюссыз;
В)p-байланыс;
С)d-байланыс;
D)ковалентті полюсты;
Е)s-байланыс.
$$$ 52
Көрсетiлген электрондық бұлттардың қабаттасуының қайсысы -байланыс түзiлуге сәйкес келедi.
А)
![]()
В)
![]()
С)
![]()
D)

Е)

$$$ 53
Күйi шексiз аз шамаға өзгеретiн система үшiн термодинамиканың 1-заңының математикалық өрнегiн табыңыз.
А) S = Q/Т;
В) dU = TdS -pdV;
С) G = -SdT + VdP;
D) Д) H = TdS; + VdP
Е) Q= dU+ A.
$$$ 54
Изотермиялық жағдайда (T=const) идеал газдың атқарған ұлғаю жұмысының шамасын есептеуге қажеттi теңдеудi табыңыз.
А) A = Cv (T1 - T2);
В) A = P(V2 - V1);
С) A = n RT ln(V2/V1);
D)
![]() ;
;
Е)
![]() .
.
$$$ 55
Қайтымсыз процестiң энтропиясы мен жылуы арасындағы қатынасты көрсететiн математикалық өрнектi табыңыз.
А)
![]() ;
;
В)![]() ;
;
С)
![]() ;
;
D)
![]()
Е)
![]() .
.
$$$ 56
Химиялық реакция үшiн КР және КС константаларының арасындағы байланысты өрнектейтiн теңдеудi жазыңыз.
А) КР = (Кс)1/2;
В) KP = Kс(RT)n, n - реакция барысында газды заттардың моль
сандарының өзгерiсi;
С) KP = Kс +RT;
D) KP = KсР, мұндағы Р – жалпы қысым;
Е) KP = (Kс)3.
$$$ 57
Fe2O3(қ) + 3H2O(г) 2Fe(қ) + 3H2O(c )
реакциясының
стандартты жағдайдағы (Т=298К)
Гиббс энергиясының өзгерiсiн
есептеп, реакцияның жүретiндiгiн
немесе жүрмейтiндiгiн
анықтаңыз. Реакцияның энтальпиясы
![]() кДж/моль, ал энтропиясы
кДж/моль, ал энтропиясы
![]() кДж/моль К .
кДж/моль К .
А)
![]() -1000 кДж/моль, реакция жүредi;
-1000 кДж/моль, реакция жүредi;
В)
![]() 8047 кДж/моль, реакция жүрмейдi;
8047 кДж/моль, реакция жүрмейдi;
С)
![]() 0 кДж/моль, реакция жүрмейдi;
0 кДж/моль, реакция жүрмейдi;
D)
![]() -10259 кДж/моль, реакция жүредi;
-10259 кДж/моль, реакция жүредi;
Е)
![]() 63677 кДж/моль, реакция жүрмейдi.
63677 кДж/моль, реакция жүрмейдi.
$$$ 58
H2(г) +CI2(г) 2HCI(г) қайтымды реакциясының тепе-теңдік константасын жазыңыз.
А)
![]() ;
;
В)
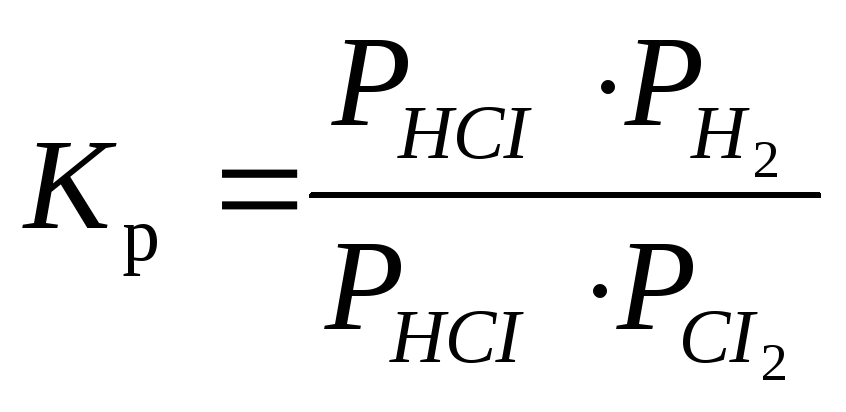 ;
;
С)
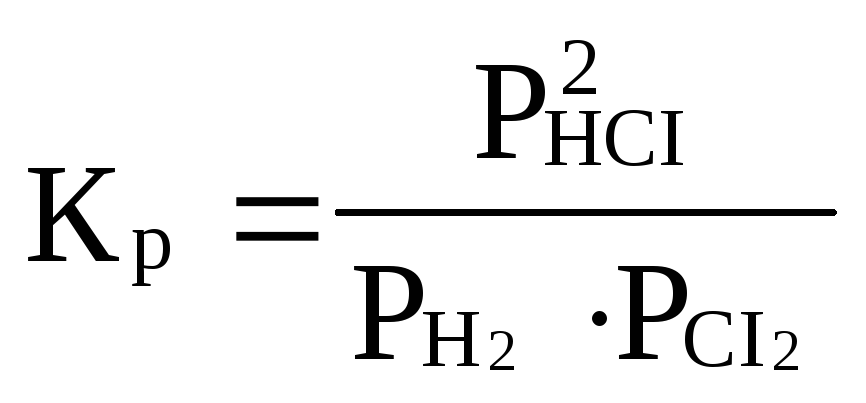 ;
;
D)
![]() ;
;
Е)
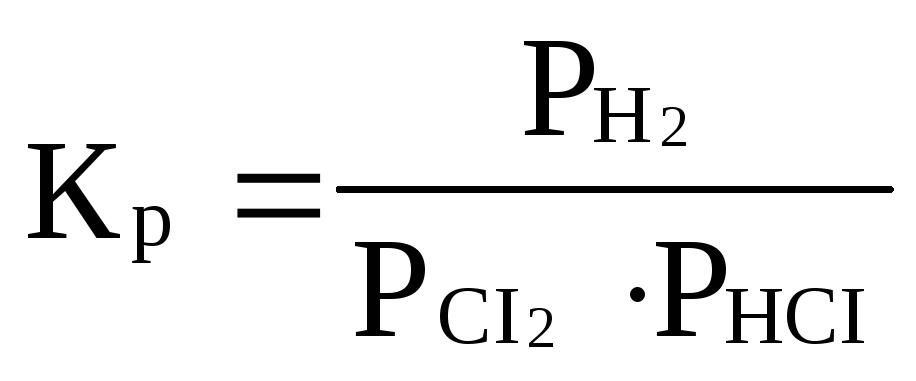 .
.
$$$ 59
Заттардың
стандартты түзiлу
жылулары (![]() )
арқылы төменде
берiлген
реакцияның жылу
эффектiсiн
(
)
арқылы төменде
берiлген
реакцияның жылу
эффектiсiн
(![]() )
есептеуге қажеттi
теңдеудi
көрсетiңiз:
CO + 3Н2
= CН4
+ Н2O(г).
)
есептеуге қажеттi
теңдеудi
көрсетiңiз:
CO + 3Н2
= CН4
+ Н2O(г).
A)
![]() ;
;
B)
![]() ;
;
C)![]() ;
;
D)
![]() ;
;
Е)
![]() .
.
$$$ 60
Н2(г) + CI2(г) = 2HCI(г) реакциясының тепе-теңдiк константалары (КР мен КС) өзара қандай байланыста болады?
А) КР = КС RT;
В) KP = KC(RT)2;
С) KP = KC;
D) KP = KC/(RT);
Е) KP = KC/(RT)2.
$$$ 61
2NO
+ O2 = 2NO2
реакциясының стандартты Гиббс энергиясының
өзгерiсiн
![]() және реакцияның еркiн жүру бағытын
анықтаңыз, егер заттардың
298К температурадағы еркiн түзiлу
энергиялары төмендегiдей болса:
және реакцияның еркiн жүру бағытын
анықтаңыз, егер заттардың
298К температурадағы еркiн түзiлу
энергиялары төмендегiдей болса:
![]() Дж/моль;
Дж/моль;
![]() Дж/моль.
Дж/моль.
А)![]() Дж; реакция керi бағытта жүредi;
Дж; реакция керi бағытта жүредi;
В)
![]() Дж; реакция тура бағытта жүредi;
Дж; реакция тура бағытта жүредi;
С)
![]() ;
реакция жүрмейдi;
;
реакция жүрмейдi;
D)
![]() Дж;
реакция тура бағытта жүредi;
Дж;
реакция тура бағытта жүредi;
Е)
![]() Дж; реакция керi бағытта жүредi.
Дж; реакция керi бағытта жүредi.
$$$ 62
H2(г)+ J2(г) 2HJ(c) системасы тепе-теңдік күйде. Жалпы қысымды арттырғанда тепе-теңдік қай бағытта ығысады?
А) тепе-теңдік HJ(c) түзілу бағытына қарай ығысады;
В) тепе-теңдік H2(г) мен J2(г) түзілу бағытына қарай ығысады;
С) жалпы қысымның өзгерісі тепе-теңдік күйге әсер етпейді;
D) тепе-теңдік H2(Г) түзілу бағытына қарай ығысады;
Е) тепе-теңдік HJ(c) азаюбағытына қарай ығысады
$$$ 63
Процестiң тұрақты көлем (V = const) және тұрақты температура
(T = const) жағдайында өз еркiмен жүру критериясы ретiнде қандай термодинамикалық потенциалды таңдап алу керек?
А) Гельмгольц энергиясы (F);
В) Гиббс энергиясы (G);
С) iшкi энергия (U);
D) энтальпия (H);
E) энтропия (S).
$$$ 64
Процестiң тұрақты қысым (Р = const) және тұрақты температура
(T=const) жағдайында өз еркiмен жүру критериясы ретiнде қандай термодинамикалық потенциалды таңдап алу керек?
А) Гельмгольц энергиясы (F);
В) Гиббс энергиясы (G);
С) iшкi энегГия (U);
D) энтальпия (H);
E) энтропия (S).
$$$ 65
Бензол үш агрегаттық күйде (қатты, сұйық, бу) болғанда, осы заттардың энтропиялары өзара қандай қатынаста болады?
А) S(с) > S(қ) > S(бу);
В) S(бу) > S(с) > S(қ);
С) S(қ) > S(бу) > S(с );
D) S(қ) > S(с ) > S(бу );
Е) S)бу) = S)қ) = S)с ).
$$$ 66
А + В Е + Д химиялық реакциясының жылдамдығын өрнектеп жазыңыз.
A)
![]() ;
;
B)
![]() ;
;
C)
![]() ;
;
D)
![]() ;
;
Е)
![]() .
.
$$$ 67
3А В + С 3 - реттi реакциядағы СА = 0,1 моль/л, k= 100 л2/(моль2мин). Реакцияның жылдамдығын анықтаңыз.
А) 1000;
В) 10;
С) 1;
D) 0,1;
Е) 10000.
