
- •1.4 Организация работ в цехе
- •Кварцитовые бункера ,дозировочного отделения Кварцит фракции 100-25 мм
- •1.5 Объемно-планировочные решения цеха
- •2.6.1 Статьи прихода тепла
- •2.6.2.5 Тепло эндотермических реакций
- •2.6.2.6 Потери тепла через футеровку
- •2.6.2.7 Потери тепла с охлаждающей водой
- •2.6.2.8 Расчет удельного расхода электроэнергии
- •Расход электроэнергии соответствует литературным данным [13].
- •2.6.2.9 Сводная таблица теплового баланса
2.6.1 Статьи прихода тепла
Приход тепла при выплавке СМн17 складывается из трех статей:
Химическая энергия, выделяемая при сгорании восстановителя
1)
по реакции
![]() (61)
(61)
![]()
![]() (62)
(62)
2)
по реакции
![]() (63)
(63)
![]()
![]() (64)
(64)
Суммарный тепловой эффект реакций:
![]() (65)
(65)
2.6.1.2 Электроэнергия
Количество тепла, вносимой электроэнергией Q2 подлежит определению из теплового баланса.
2.6.1.3 Тепло экзотермических реакций
образование силицида марганца по реакции:
Mn + Si = MnSi (66)
![]()
![]() (67)
(67)
2) образование силикатов марганца, алюминия, кальция и магния по реакциям:
|
MnO+SiO2=MnSiO3 |
|
|
Al2O3+SiO2=Al2SiO5 |
|
|
CaO+SiO2=CaSiO3 |
|
|
MgO+SiO2=MgSiO3 |
|
![]() (68)
(68)
Приход тепла от экзотермических реакций равен:
![]() (69)
(69)
Итого приход тепла составит:
![]() (70)
(70)
2.6.2 Статьи расхода тепла
2.6.2.1 Тепло металла
Энтальпия металла при температуре Т может быть подсчитана по уравнению:
 (71)
(71)
где Gмет – масса металла;
![]()
средняя молекулярная масса металла
средняя молекулярная масса металла ![]() ;
;
Mi – атомный вес i-ого компонента сплава;
Хi – атомная доля i-ого компонента сплава;
Нм – относительная интегральная молярная энтальпия сплава Mn–Si (теплота, смешение компонентов при образовании 1 моля сплава).
Нi – изменение энтальпии при нагревании i–ого компонента сплава от стандартной температуры до температуры выпуска сплава из печи,
![]()
Состав металла в атомных долях (таблица 12) рассчитывается по формуле:
 (72)
(72)
где Gi – масса i-ого компонента сплава;
к – количество компонентов сплава.
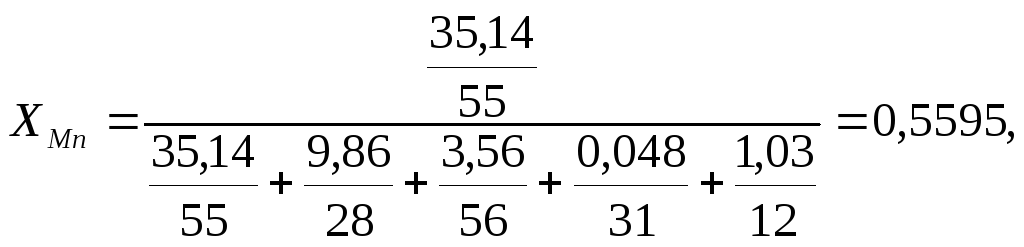
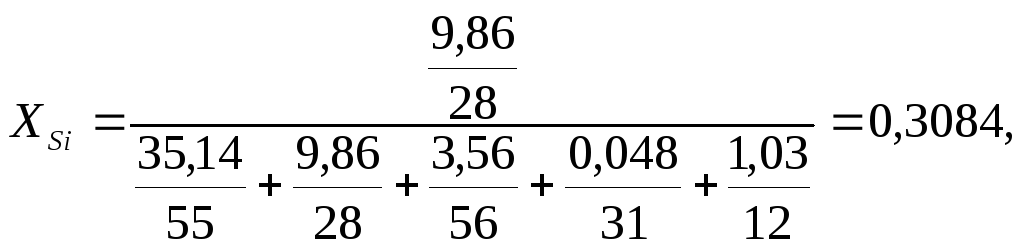



Таблица 12 – Состав металла в атомных долях
|
Компонент сплава |
Mn |
Si |
Fe |
P |
C |
|
Атомная доля |
0,5595 |
0,3084 |
0,0557 |
0,0014 |
0,0752 |
Средняя молекулярная масса металла равна:
![]()
Примем
температуру силикомарганца марки СМн17
в печи, равной 1650ºC. Тогда:
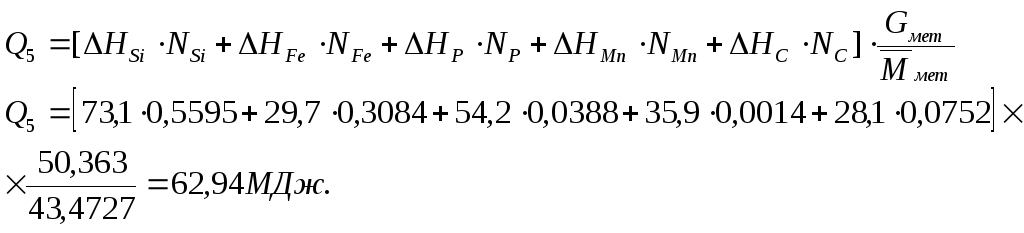
2.6.2.2 Тепло шлака
Температура шлака в печи может быть приравнена температуре металла. Энтальпия жидкого шлака может быть рассчитана по уравнению
 (73)
(73)
где Gшл – вес шлака;
![]() средний молекулярный вес
шлака
средний молекулярный вес
шлака ![]() ;
;
Mi – атомный вес i-ого компонента шлака;
Хi – атомная доля i-ого компонента шлака;
Нi
– теплосодержание i-ого
компонента шлака, причем, если tшл
tпл
i-ого компонента, нужно
учитывать теплоту плавления компонента,
т.е. ![]() .
.
Состав шлака в мольных долях (таблица 13) рассчитывается по формуле:
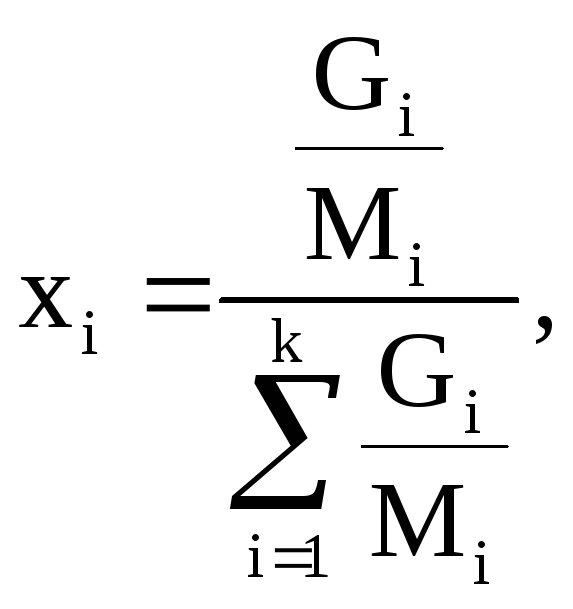 (74)
(74)
где Gi – масса i-ого компонента шлака;
к – количество компонентов шлака.



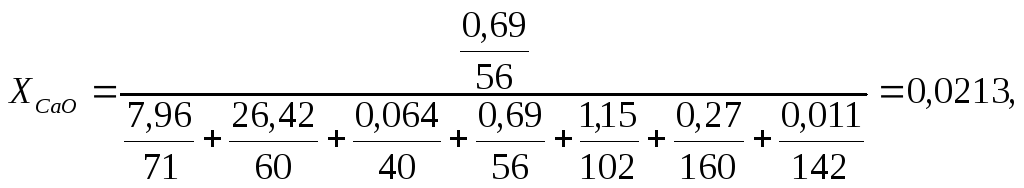



Состав шлака в мольных долях приведен в таблице13.
Таблица 13 – Состав шлака в мольных долях
|
Компонент шлака |
MnO |
SiO2 |
MgO |
CaO |
Al2O3 |
Fe2O3 |
P2O5 |
|
Мольная доля |
0,1935 |
0,7600 |
0,0028 |
0,0213 |
0,0195 |
0,0029 |
0,0001 |
![]()
Тепло шлака выражается величиной
![]()
![]()
![]()
2.6.2.3 Тепло газов
Примем температуру отходящих газов 600 К, тогда
![]()
2.6.2.4 Тепло пыли
![]()
![]()
