
- •Физико-химические свойства белков
- •Первичная структура
- •Вторичная структура белков
- •Третичная структура белков
- •22) Сахароза. Строение. Способы получения. Свойства.
- •27) Углеводы как природно-сырьевой источник.
- •28) Невосстанавливающие углеводы. Особенности строения.
- •29) Изомерия моносахаридов.
- •30) Явление таутомерии и мутаротации у моносахаридов.
- •31) Олигосахариды.
- •32) Гликозидная связь в структуре углеводов и их производных.
- •10.4. Сложные липиды
- •10.4.1. Фосфолипиды
- •10.4.2. Сфинголипиды
- •10.4.3. Гликолипиды
- •10.4. Сложные липиды
- •10.4.1. Фосфолипиды
- •10.4.2. Сфинголипиды
- •10.4.3. Гликолипиды
№1. Белки: пептидная связь, их обнаружение.
Белки – макромолекулы линейных полиамидов, образованных а-аминокислотами в результате реакции поликонденсации в биологических объектах.
Белки – это высокомолекулярные соединения, построенные из аминокислот. В создание белков участвует 20 аминокислот. Они связываются между собой в длинные цепи, которые образуют основу белковой молекулы большой молекулярной массы.
Функции белков в организме
Сочетание своеобразных химических и физических свойств белков обеспечивает именно этому классу органических соединений центральную роль в явлениях жизни.
Белки имеют следующие биологические свойства, или осуществляют следующие основные функции в живых организмах:
1. Каталитическая функция белков. Все биологические катализаторы - ферменты являются белками. В настоящее время охарактеризовано тысячи ферментов, многие из них выделены в кристаллической форме. Почти все ферменты - мощные катализаторы, повышающие скорости реакций, по крайней мере, в миллион раз. Эта функция белков является уникальной, не свойственной другим полимерным молекулам.
2. Питательная (резервная функция белков). Это, прежде всего белки, предназначенные для питания развивающегося зародыша: казеин молока, овальбумин яиц, запасные белки семян растений. Ряд других белков, несомненно, используется в организме в качестве источника аминокислот, которые, в свою очередь, являются предшественниками биологически активных веществ, регулирующих процесс обмена веществ.
3. Транспортная функция белков. Транспорт многих небольших молекул и ионов осуществляется специфическими белками. Например, дыхательная функция крови, а именно перенос кислорода, выполняется молекулами гемоглобина - белка эритроцитов. В транспорте липидов принимают участие альбумины сыворотки крови. Ряд других сывороточных белков образует комплексы с жирами, медью, железом, тироксином, витамином А и другими соединениями, обеспечивая их доставку в соответствующие органы.
4. Защитная функция белков. Основную функцию защиты выполняет иммуннологическая система, которая обеспечивает синтез специфических защитных белков - антител - в ответ на поступление в организм бактерий, токсинов или вирусов (антигенов). Антитела связывают антигены, взаимодействуя с ними, и тем самым нейтрализуют их биологическое действие и сохраняют нормальное состояние организма. Свертывание белка плазмы крови - фибриногена - и образование сгустка крови, предохраняющего от потери крови при ранениях - еще один пример защитной функции белков.
5. Сократительная функция белков. В акте мышечного сокращения и расслабления участвует множество белков. Главную роль в этих процессах играют актин и миозин - специфические белки мышечной ткани. Сократительная функция присуща также и белкам субклеточных структур, что обеспечивает тончайшие процессы жизнедеятельности клеток,
6. Структурная функция белков. Белки с такой функцией занимают первое место среди других белков тела человека. Широко распространены такие структурные белки, как коллаген в соединительной ткани; кератин в волосах, ногтях, коже; эластин - в сосудистых стенках и др.
7. Гормональная (регуляторная) функция белков. Обмен веществ в организме регулируется разнообразными механизмами. В этой регуляции важное место занимают гормоны, вырабатываемые железами внутренней секреции. Ряд гормонов представлен белками, или полипептидами, например гормоны гипофиза, поджелудочной железы и др.
Пептидная связь
Формально образование белковой макромолекулы можно представить как реакцию поликонденсации α-аминокислот.
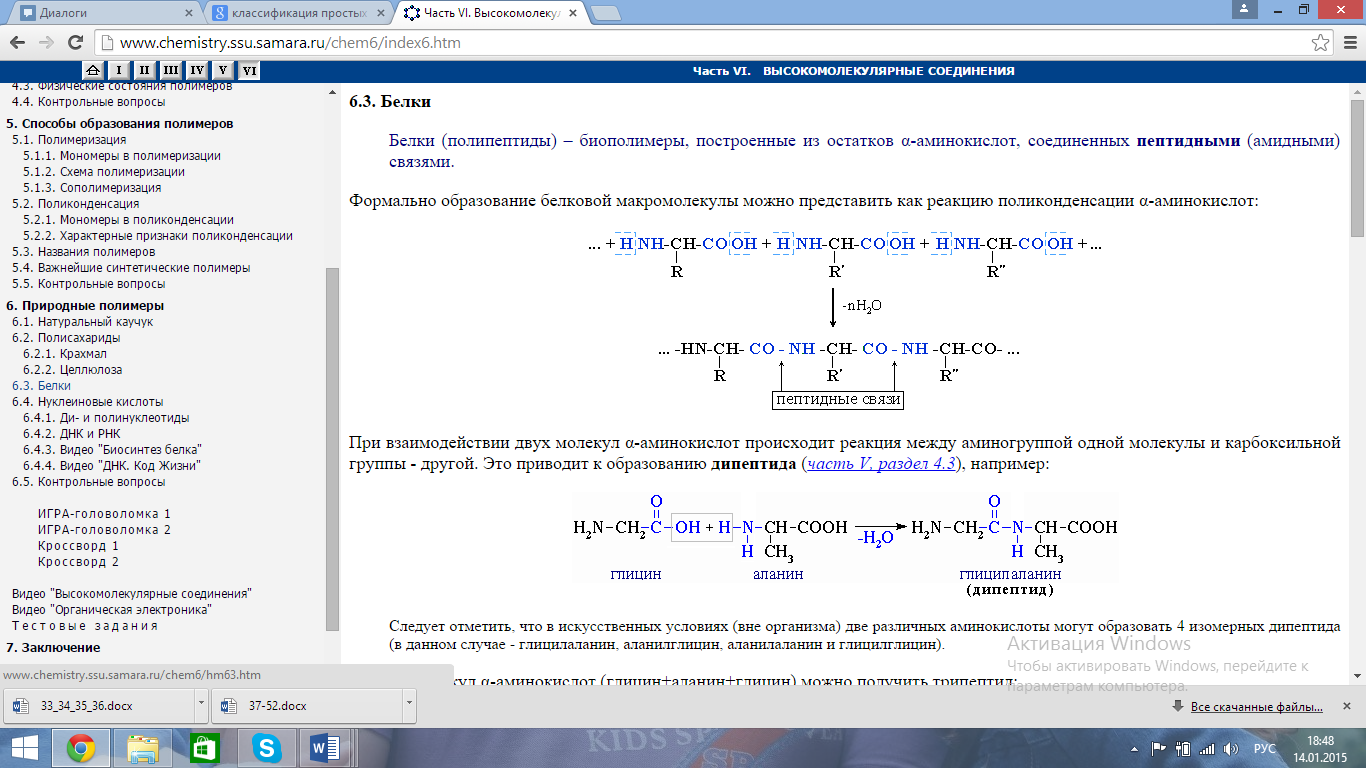
С химической точки зрения белки - это высокомолекулярные азотсодержащие органические соединения (полиамиды), молекулы которых построены из остатков аминокислот. Мономерами белков служат α-аминокислоты, общим признаком которых является наличие карбоксильной группы -СООН и аминогруппы -NH2 у второго углеродного атома (α-углеродный атом):
Исходя из результатов изучения продуктов гидролиза белков и выдвинутых А.Я. Данилевским идей о роли пептидных связей -CO-NH- в построении белковой молекулы, немецкий ученый Э. Фишер предложил в начале XX века пептидную теорию строения белков. Согласно этой теории, белки представляют собой линейные полимеры α-аминокислот, связанных пептидной связью - полипептиды:
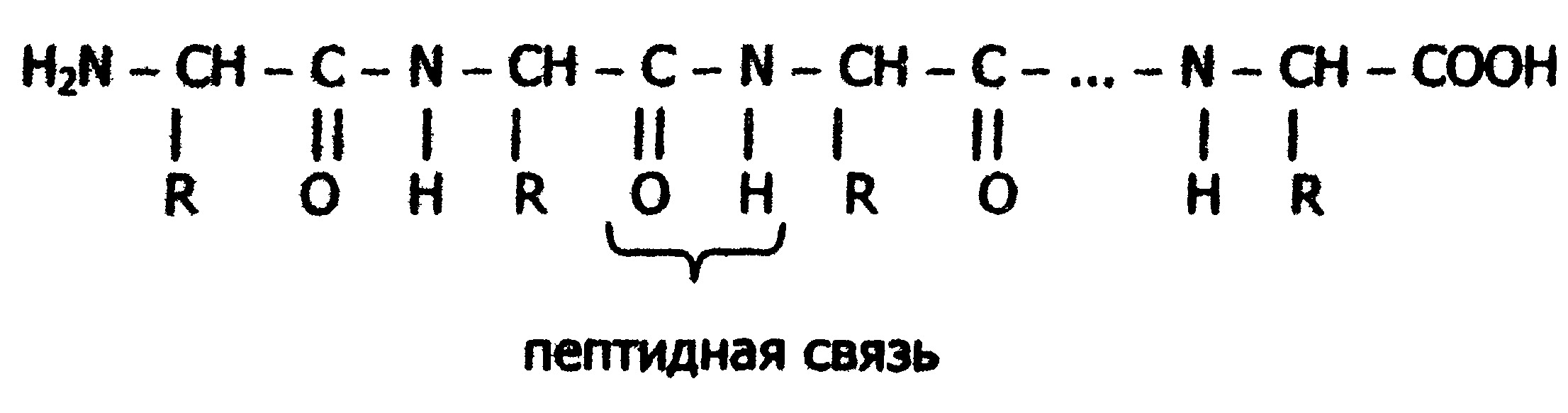
В каждом пептиде один концевой аминокислотный остаток имеет свободную α-аминогруппу (N-конец), а другой - свободную α-карбоксильную группу (С-конец). Структуру пептидов принято изображать, начиная с N-концевой аминокислоты. При этом аминокислотные остатки обозначаются символами. Например: Ala-Tyr-Leu-Ser-Tyr- •••-Cys. Этой записью обозначен пептид, в котором N-концевой α-аминокислотой является аланин, а С-концевой - цистеин. При чтении такой записи окончания названий всех кислот, кроме последних меняются на - "ил": аланил-тирозил-лейцил-серил-тирозил-••• -цистеин. Длина пептидной цепи в пептидах и белках, встречающихся в организме, колеблется от двух до сотен и тысяч аминокислотных остатков.
№2. Классификация простых белков.
К простым (протеинам) относят белки, дающие при гидролизе только аминокислоты.
Протеиноиды____простые белки животного происхождения, нерастворимые вводе, растворах солей, разбавленных кислотах и щелочах. Выполняют главным образом опорные функции (например, Коллаген, кератин
протамины – положительно заряженные ядерные белки, с молекулярной массой 10-12 kDa. Примерно на 80% состоят из щелочных аминокислот, что дает им возможность взаимодействовать с нуклеиновыми кислотами посредством ионных связей. Принимают участие в регуляции генной активности. Хорошо растворимы в воде;
гистоны – ядерные белки, играющие важную роль в регуляции генной активности. Они найдены во всех эукариотических клетках, и разделены на 5 классов, различающихся по молекулярной массе и аминокислотному. Молекулярная масса гистонов находится в интервале от 11 до 22 kDa, а различия в аминокислотном составе касаются лизина и аргинина, содержание которых варьирует от 11 до 29% и от 2 до 14% соответственно;
проламины – не растворимы в воде, но растворимы в 70% спирте, особенности хим.строения – много пролина, глутаминовой кислоты нет лизина,
глутелины – растворимы в щелочных растворах,
глобулины – белки, не растворимые в воде и в полунасыщенном растворе сернокислого аммония, но растворимые в водных растворах солей, щелочей и кислот. Молекулярная масса – 90-100 kDa;
альбумины – белки животных и растительных тканей, растворим в воде и солевых растворах. Молекулярнаяя масса равна 69 kDa;
склеропротеины – белки опорных тканей животных
В качестве примеров простых белков могут служить фиброин шелка, яичный сывороточный альбумин, пепсин и др.
№3. Способы выделения и осаждения (очистки) белков.





№4. Белки как полиэлектролиты. Изоэлектрическая точка белка.
Белки являются амфотерными полиэлектролитами, т.е. проявляют как кислотные, так и основные свойства. Это обусловлено наличием в молекулах белков аминокислотных радикалов, способных к ионизации, а также свободных α-амино- и α-карбоксильных групп на концах пептидных цепей. Кислотные свойства белку придают кислые аминокислоты (аспарагиновая, глутаминовая), а щелочные свойства - основные аминокислоты (лизин, аргинин, гистидин).
Заряд белковой молекулы зависит от ионизации кислых и основных групп аминокислотных радикалов. В зависимости от соотношения отрицательных и положительных групп молекула белка в целом приобретает суммарный положительный или отрицательный заряд. При подкислении раствора белка степень ионизации анионных групп снижается, а катионных повышается; при подщелачивании - наоборот. При определенном значении рН число положительно и отрицательно заряженных групп становится одинаковым, возникает изоэлектрическое состояние белка (суммарный заряд равен 0). Значение рН, при котором белок находится в изоэлектрическом состоянии, называют изоэлектрической точкой и обозначают pI, аналогично аминокислотам. Для большинства белков pI лежит в пределах 5,5-7,0, что свидетельствует о некотором преобладании в белках кислых аминокислот. Однако есть и щелочные белки, например, сальмин - основной белок из молок семги (pl=12). Кроме того, есть белки, у которых pI имеет очень низкое значение, например, пепсин - фермент желудочного сока (pl=l). В изоэлектрической точке белки очень неустойчивые и легко выпадают в осадок, обладая наименьшей растворимостью.
Если белок не находится в изоэлектрическом состоянии, то в электрическом поле его молекулы будут перемещаться к катоду или аноду, в зависимости от знака суммарного заряда и со скоростью, пропорциональной его величине; в этом заключается сущность метода электрофореза. Этим методом можно разделять белки с различным значением pI.
Белки хотя и обладают свойствами буфера, но емкость их при физиологических значениях рН ограничена. Исключение составляют белки, содержащие много гистидина, так как только радикал гистидина обладает буферными свойствами в интервале рН 6-8. Таких белков очень мало. Например, гемоглобин, содержащий почти 8% гистидина, является мощным внутриклеточным буфером в эритроцитах, поддерживая рН крови на постоянном уровне.
№5. Физико-химические свойства белков.
Белки имеют различные химические, физические и биологические свойства, которые определяются аминокислотным составом и пространственной организацией каждого белка. Химические реакции белков очень разнообразны, они обусловлены наличием NH2-, СООН-групп и радикалов различной природы. Это реакции нитрования, ацилирования, алкилирования, этерификации, окисления-восстановления и другие. Белки обладают кислотно-основными, буферными, коллоидными и осмотическими свойствами.
Кислотно-основные свойства белков
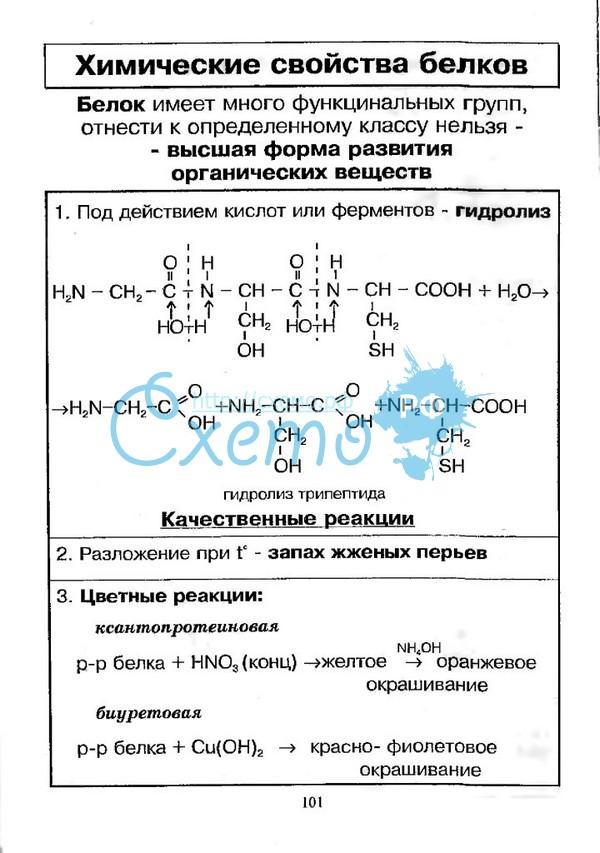
Химические свойства. При слабом нагревании водных растворов белков происходит денатурация. При этом образуется осадок.
При нагревании белков с кислотами происходит гидролиз, при этом образуется смесь аминокислот.
Физико-химические свойства белков
Белки имеют высокий молекулярный вес.
Заряд белковой молекулы. Все белки имеют хоть одну свободную -NH и - СООН группы.
Белковые растворы - коллоидные растворы с разными свойствами. Белки бывают кислыми и основными. Кислые белки содержат много глу и асп, у которых есть дополнительные карбоксильные и меньше аминогрупп. В щелочных белках много лиз и арг. Каждая молекула белка в водном растворе окружена гидратной оболочкой, так как у белков за счет аминокислот есть много гидрофильных группировок (-СООН, -ОН, -NH2, -SH). В водных растворах белковая молекула имеет заряд. Заряд белка в воде может меняться в зависимости от РН.
Осаждение белков. У белков есть гидратная оболочка, заряд, препятствующий склеиванию. Для осаждения необходимо снять гидратную оболочку и заряд.
1.Гидратация. Процесс гидратации означает связывание белками воды, при этом они проявляют гидрофильные свойства: набухают, их масса и объем увеличивается. Набухание белка сопровождается его частичным растворением. Гидрофильность отдельных белков зависит от их строения. Имеющиеся в составе и расположенные на поверхности белковой макромолекулы гидрофильные амидные (–CO–NH–, пептидная связь), аминные (NH2) и карбоксильные (COOH) группы притягивают к себе молекулы воды, строго ориентируя их на поверхность молекулы. Окружая белковые глобулы гидратная (водная) оболочка препятствует устойчивости растворов белка. В изоэлектрической точке белки обладают наименьшей способностью связывать воду, происходит разрушение гидратной оболочки вокруг белковых молекул, поэтому они соединяются, образуя крупные агрегаты. Агрегация белковых молекул происходит и при их обезвоживании с помощью некоторых органических растворителей, например этило- вого спирта. Это приводит к выпадению белков в осадок. При изменении pH среды макромолекула белка становится заряженной, и его гидратационная способность меняется.
Реакции осаждения делят на два вида.
Высаливание белков: (NH4)SO4 - снимается только гидратная оболочка, белок сохраняет все виды своей структуры, все связи, сохраняет нативные свойства. Такие белки можно затем вновь растворить и использовать.
Осаждения с потерей нативных свойств белка - процесс необратимый. С белка снимается гидратная оболочка и заряд, нарушаются различные свойства в белке. Например соли меди, ртути, мышьяка, железа, концентрированные неорганические кислоты - HNO3, H2SO4, HCl, органические кислоты, алкалоиды - танины, йодистая ртуть. Добавление органических растворителей понижает степень гидратации и приводит к осаждению белка. В качестве таких растворителей используют ацетон. Осаждают белки также с помощью солей, например, сульфата аммония. Принцип этого метода основан на том, что при повышении концентрации соли в растворе происходит сжатие ионных атмосфер, образуемых противоионами белка, что способствует сближению их до критического расстояния, на котором межмолекулярные силы ван-дер-ваальсова притяжения перевешивают кулоновские силы отталкивания противоионов. Это приводит к слипанию белковых частиц и их выпадению в осадок.
При кипячении молекулы белков начинают хаотично двигаться, сталкиваются, снимается заряд, уменьшается гидратная оболочка.
Для обнаружения белков в растворе применяются:
цветные реакции;
реакции осаждения.
Методы выделения и очистки белков.
гомогенизация - клетки растираются до однородной массы;
экстракция белков водными или водно-солевыми растворами;
диализ;
высаливание;
электрофорез;
хроматография: адсорбция, расщепление;
ультрацентрифугирование.
Структурная организация белков.
Первичная структура - определяется последовательностью аминокислот в пептидной цепочке, стабилизируется ковалентными пептидными связями (инсулин, пепсин, химотрипсин).
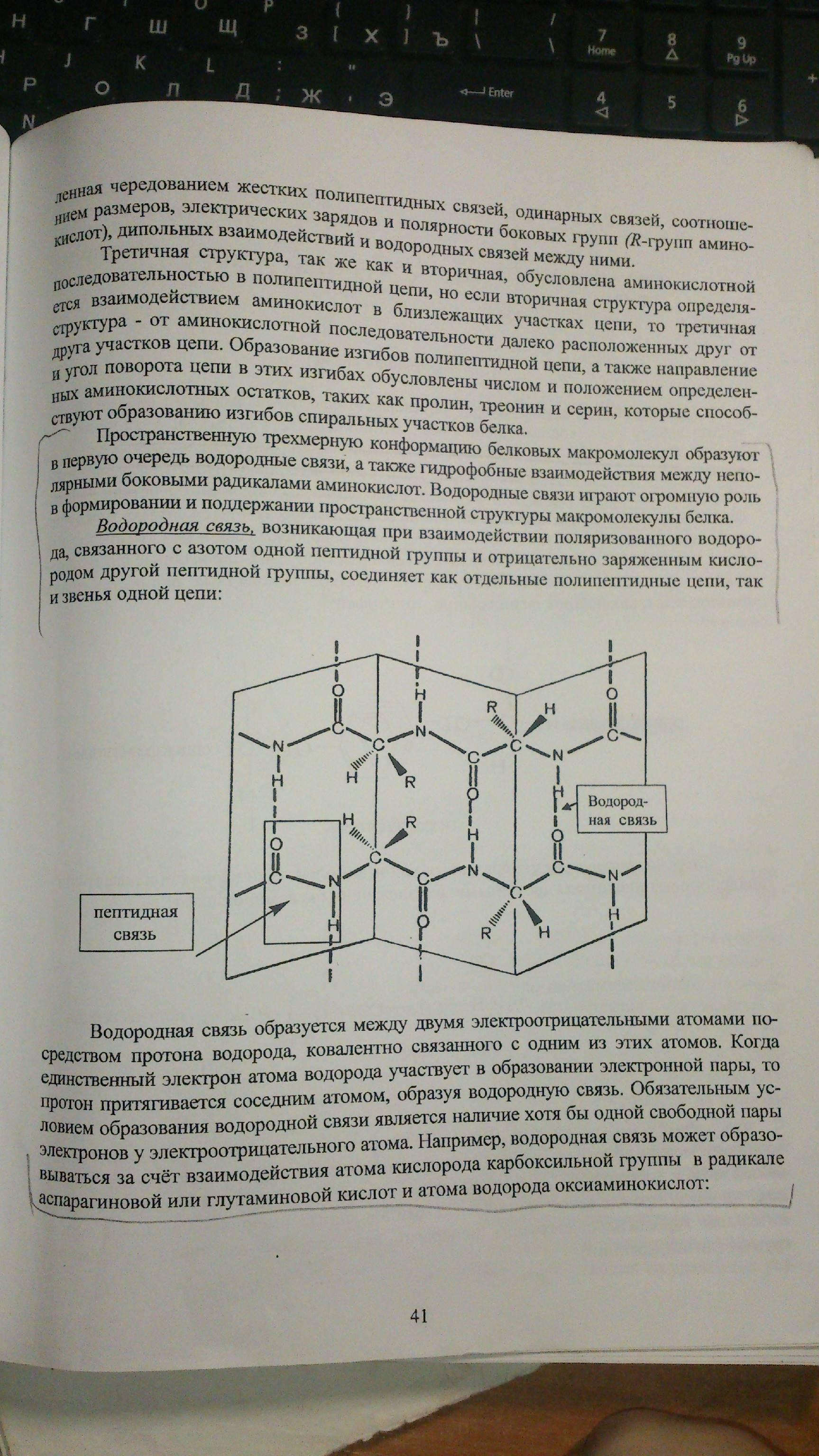
Вторичная структура - пространственная структура белка. Это либо -спираль, либо -складчатость. Создаются водородные связи.
Третичная структура - глобулярные и фибриллярные белки. Стабилизируют водородные связи, электростатические силы (СОО-, NН3+), гидрофобные силы, сульфидные мостики, определяются первичной структурой. Глобулярные белки - все ферменты, гемоглобин, миоглобин. Фибриллярные белки - коллаген, миозин, актин.
Четвертичная структура - имеется только у некоторых белков. Такие белки построены из нескольких пептидов. Каждый пептид имеет свою первичную, вторичную, третичную структуру, называются протомерами. Несколько протомеров соединяются вместе в одну молекулу. Один протомер не функционирует как белок, а только в соединении с другими протомерами.
Пример: гемоглобин = -глобула + -глобула - переносит О2 в совокупности, а не по раздельности.
Белок может ренатурировать. Для этого необходимо очень короткое воздействие агентов.
6) Способы обнаружения белков.
Белки – высокомолекулярные биологические полимеры, структурными (мономерными) звеньями которых служат -аминокислоты. Аминокислоты в белках соединены друг с другом пептидной связью,образование которой происходит за счет карбоксильной группы, стоящей у -углеродного атома одной аминокислоты и -аминной группы другой аминокислоты с выделением молекулы воды. Мономерные звенья белков называют остатками аминокислот.
Пептиды, полипептиды и белки отличаются не только количеством, составом но и последовательностью аминокислотных остатков, физико-химическими свойствами и функциями, выполняемыми в организме. Молекулярная масса белков варьирует от 6 тыс. до 1 млн. и более. Химические и физические свойства белков обусловлены химической природой и физико-химическими свойствами радикалов, входящих в них остатков аминокислот. Способы обнаружения и количественного определения белков в биологических объектах и продуктах питания, а также выделения их из тканей и биологических жидкостей основаны на физических и химических свойствах этих соединений.
Белки при взаимодействии с некоторыми химическими веществами дают окрашенные соединения. Образование этих соединений происходит при участии радикалов аминокислот, их специфических групп или пептидных связей. Цветные реакции позволяют установитьналичие белка в биологическом объектеили растворе и доказать присутствиеопределенных аминокислот в белковой молекуле. На основе цветных реакций разработаны некоторые методы количественного определения белков и аминокислот.
Универсальными считают биуретовую и нингидриновую реакции, так как их дают все белки.Ксантопротеиновая реакция, реакция Фоляи др. являются специфическими, так как они обусловлены радикальными группами определенных аминокислот в молекуле белка.
Цветные реакции позволяют установить наличие белка в исследуемом материале и присутствие определенных аминокислот в его молекулах.
Биуретовая реакция. Реакция обусловлена наличием в белках, пептидах, полипептидахпептидных связей, которые в щелочной среде образуют сионами меди (II)комплексные соединения, окрашенные вфиолетовый (с красным или с синим оттенком) цвет. Окраска обусловлена наличием в молекуле не менее двух групп-CO-NH-, связанных непосредственно между собой или при участии атома углерода или азота.
Ионы меди (II) соединяются двумя ионными связями с группами =С─Оˉ и четырьмя координационными связями с атомами азота (=N―).
Итенсивность окраски зависит от количества белка в растворе. Это позволяет использовать данную реакцию для количественного определения белка. Цвет окрашенных растворов зависит от длины полипептидной цепи.Белки дают сине-фиолетовое окрашивание; продукты их гидролиза (поли- и олигопептиды) – красную или розовую окраску. Биуретовую реакцию дают не только белки, пептиды и полипептиды но и биурет (NH2-CO-NH-CO-NH2) , оксамид (NH2-CO-CO-NH2), гистидин.
Образующееся в щелочной среде комплексное соединение меди (II) с пептидными группами имеет следующее строение:
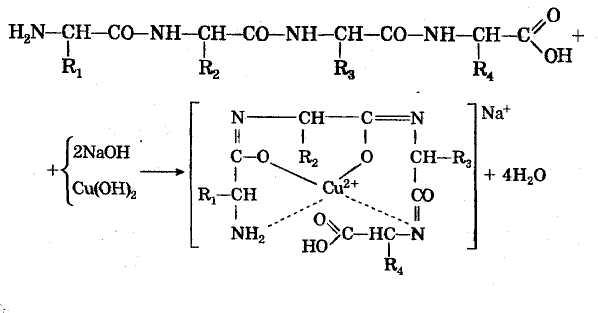
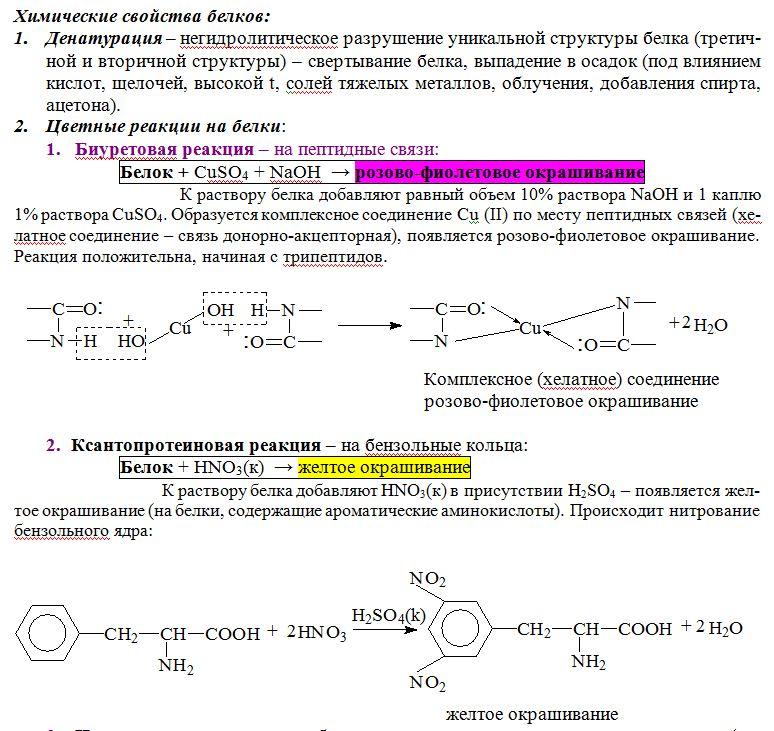
Нингидриновая реакция. В этой реакции растворы белка, полипептидов, пептидов и свободных α-аминокислот при нагревании с нингидрином дают синее, сине-фиолетовое или розово-фиолетовое окрашивание. Окраска в этой реакции развивается за счет α-аминогруппы.


Очень легко реагируют с нингидрином -аминокислоты. Наряду с ними сине-фиолетовый Руэмана образуют также белки, пептиды, первичные амины, аммиак и некоторые другие соединения. Вторичные амины, например пролин и оксипролин, дают желтую окраску.
Нингидриновую реакцию широко используют для обнаружения и количественного определения аминокислот.
Ксантопротеиновая реакция.Эта реакция указывает на наличие в белках остатков ароматических аминокислот – тирозина, фенилаланина, триптофана. Основана на нитровании бензольного кольца радикалов этих аминокислот с образованием нитросоединений, окрашенных в желтый цвет (греческое «Ксантос» – желтый). На примере тирозина эту реакцию можно описать в виде следующих уравнений.
В щелочной среде нитропроизводные аминокислот образуют соли хиноидной структуры, окрашенные в оранжевый цвет. Ксантопротеиновую реакцию дают бензол и его гомологи, фенол и другие ароматические соединения.

Реакции на аминокислоты, содержащие тиоловую группу в восстановленном или окисленном состоянии (цистеин, цистин).
Реакция Фоля. При кипячении со щелочью от цистеина легко отщепляется сера в виде сероводорода, который в щелочной среде образует сульфид натрия:
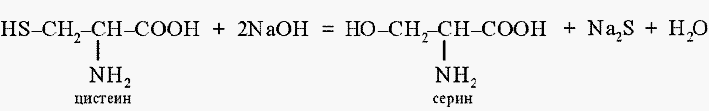
В связи с этим реакции определения тиолсодержащих аминокислот в растворе подразделяют на два этапа:
Переход серы из органического состояния в неорганическое
Обнаружение серы в растворе
Для выявления сульфида натрия используют ацетат свинца, который при взаимодействии с гидроксидом натрия превращается в его плюмбит:
Pb(CH3COO)2 + 2NaOH Pb(ONa)2 + 2CH3COOH
В результате взаимодействия ионов серы и свинца образуется сульфид свинца черного или бурого цвета:
Na2S + Pb(ONa)2 + 2H2O PbS (черный осадок) + 4NaOH
Для определения серусодержащих аминокислот к исследуемому раствору добавляют равный объем гидроксида натрия и несколько капель раствора ацетата свинца. При интенсивном кипячении в течение 3-5 минут жидкость окрашивается в черный цвет.
Наличие цистина может быть определено с помощью этой реакции, так как цистин легко восстанавливается в цистеин.
Реакция Миллона:
Это реакция на аминокислоту тирозин.
Свободные фенольные гидроксилы молекул тирозина при взаимодействии с солями дают соединения ртутной соли нитропроизводного тирозина, окрашенной в розовато-красный цвет:

Реакция Паули на гистидин и тирозин. Реакция Паули позволяет обнаружить в белке аминокислоты гистидин и тирозин, которые образуют с диазобензолсульфоновой кислотой комплексные соединения вишнево-красного цвета. Диазобензолсульфоновая кислота образуется в реакции диазотирования при взаимодействии сульфаниловой кислоты с нитритом натрия в кислой среде:

К исследуемому раствору прибавляют равный объем кислого раствора сульфаниловой кислоты (приготовленного с использованием соляной кислоты) и двойной объем раствора нитрита натрия, тщательно перемешивают и сразу прибавляют соду (карбонат натрия). После перемешивания смесь окрашивается в вишнево-красный цвет при условии наличия гистидина или тирозина в исследуемом растворе.
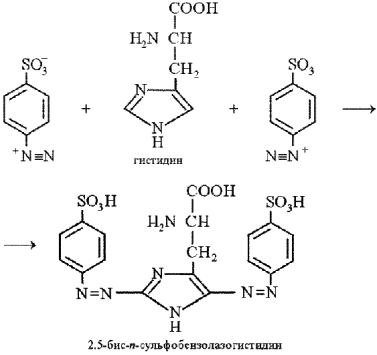
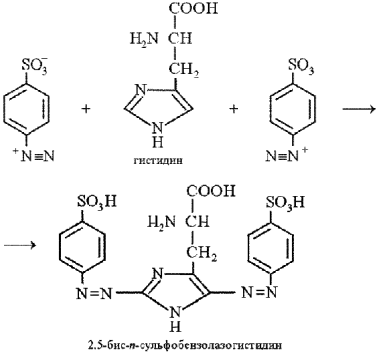
Реакция Адамкевича-Гопкинса-Коля (Шульца - Распайля) на триптофан (реакция на индоловую группу). Триптофан реагирует в кислой среде с альдегидами, образуя окрашенные продукты конденсации. Реакция протекает за счет взаимодействия индольного кольца триптофана с альдегидом. Известно, что из глиоксиловой кислоты в присутствии серной кислоты образуется формальдегид:
Р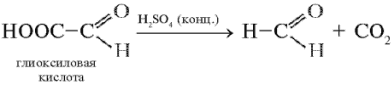 астворы,
содержащие триптофан, в присутствии
глиоксиловой и серной кислот дают
красно-фиолетовое окрашивание.
астворы,
содержащие триптофан, в присутствии
глиоксиловой и серной кислот дают
красно-фиолетовое окрашивание.
Глиоксиловая кислота всегда присутствует в небольшом количестве в ледяной уксусной кислоте. Поэтому реакцию можно проводить, используя уксусную кислоту. При этом к исследуемому раствору добавляют равный объем ледяной (концентрированной) уксусной кислоты и осторожно нагревают до растворения осадка.После охлаждения к смеси осторожно по стенке (во избежание смешивания жидкостей) добавляют объем концентрированной серной кислоты, равный добавленному объему глиоксиловой кислоты. Через 5-10 минут на границе раздела двух слоев наблюдают образование красно-фиолетового кольца. Если перемешать слои, содержимое посуды равномерно окрасится в фиолетовый цвет.
К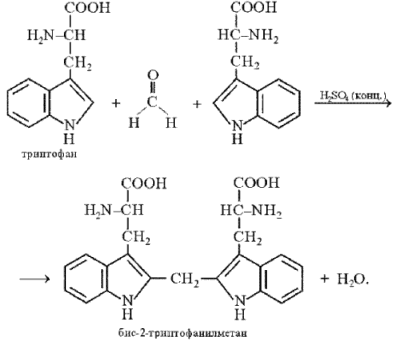
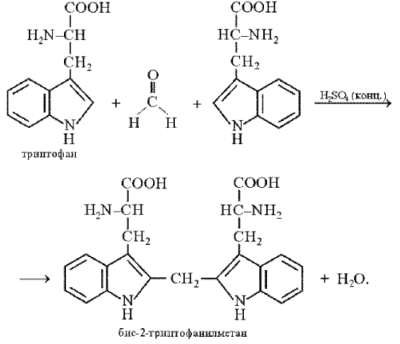 онденсация
триптофана с формальдегидом:
онденсация
триптофана с формальдегидом:
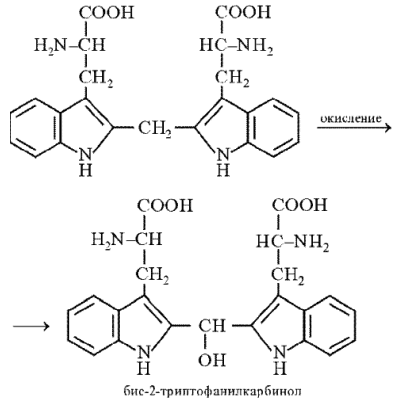
Продукт конденсации окисляется до бис-2-триптофанилкарбинола, который в присутствии минеральных кислот образует соли, окрашенные в сине-фиолетовый цвет:

7) Классификация белков. Способы исследования аминокислотного состава.
Строгой номенклатуры и классификации белков до сих пор не существует. Названия белков дают по случайным признакам, чаще всего принимая во внимание источник выделения белка или же учитывая растворимость его в тех или иных растворителях, форму молекулы и др.
Классификация белков проводится по составу, по форме частиц, по растворимости, по аминокислотному составу, по происхождению и т.д.
1. По составу белки делят на две большие группы: простые и сложные белки.
К простым (протеинам) относят белки, дающие при гидролизе только аминокислоты (протеиноиды, протамины, гистоны, проламины, глутелины, глобулины, альбумины). В качестве примеров простых белков могут служить фиброин шелка, яичный сывороточный альбумин, пепсин и др.
К сложным (к протеидам) относят белки, составленные из простого белка и добавочной (простетической) группы небелковой природы. Группу сложных белков делят на несколько подгрупп в зависимости от характера небелкового компонента:
- металлопротеиды, содержащие в своем составе металлы (Fe, Си, Mg и др.), связанные непосредственно с полипептидной цепью;
- фосфопротеиды - содержат остатки фосфорной кислоты, которые сложноэфирными связями присоединены к молекуле белка по месту гидроксильных групп серина, треонина;
- гликопротеиды - их простетическими группами являются углеводы;
- хромопротеиды - состоят из простого белка и связанного с ним окрашенного небелкового соединения, все хромопротеиды биологически очень активны; в качестве простетических групп в них могут быть производные порфирина, изоаллоксазина и каротина;
- липопротеиды - простетическая группа липиды - триглицериды (жиры) и фосфатиды;
- нуклеопротеиды - белки, состоящие из простого белка и соединенной с ним нуклеиновой кислоты. Эти белки играют колоссальную роль в жизнедеятельности организма и будут рассмотрены ниже. Они входят в состав любой клетки, некоторые нуклеопротеиды существуют в природе в виде особых частиц, обладающих патогенной активностью (вирусы).
2. По форме частиц - белки делят на фибриллярные (нитеподобные) и глобулярные (сферические) (см. стр 30).
3. По растворимости и особенностям аминокислотного состава выделяют следующие группы простых белков:
- протеиноиды - белки опорных тканей (костей, хрящей, связок, сухожилий, волос, ногтей, кожи и т.д.). Это в основном фибриллярные белки с большой молекулярной массой (> 150000 Да), нерастворимые в обычных растворителях: воде, солевых и водно-спиртовых смесях. Они растворяются только в специфических растворителях;
- протамины (простейшие белки) - белки, растворимые в воде и содержащие 80-90% аргинина и ограниченный набор (6-8) других аминокислот, представлены в молоках различных рыб. Вследствие высокого содержания аргинина имеют основные свойства, их молекулярная масса сравнительно мала и примерно равна 4000-12000 Да. Они являются белковым компонентом в составе нуклеопротеидов;
- гистоны - хорошо растворимы в воде и разбавленных растворах кислот (0,1Н), отличаются высоким содержанием аминокислот: аргинина, лизина и гистидина (не менее 30%) и поэтому обладают основными свойствами. Эти белки в значительных количествах содержатся в ядрах клеток в составе нуклеопротеидов и играют важную роль в регуляции обмена нуклеиновых кислот. Молекулярная масса гистонов невелика и равна 11000-24000 Да;
- глобулины - белки, нерастворимые в воде и солевых растворах с концентрацией соли более 7%. Глобулины полностью осаждаются при 50%-ном насыщении раствора сульфатом аммония. Эти белки отличаются высоким содержанием глицина (3,5%), их молекулярная масса > 100000 Да. Глобулины - слабокислые или нейтральные белки (р1=6-7,3);
- альбумины - белки, хорошо растворимые в воде и крепких солевых растворах, причем концентрация соли (NH4)2S04 не должна превышать 50 % от насыщения. При более высокой концентрации альбумины высаливаются. По сравнению с глобулинами эти белки содержат глицина в три раза меньше и имеют молекулярную массу, равную 40000-70000 Да. Альбумины имеют избыточный отрицательный заряд и кислые свойства (pl=4,7) из-за большого содержания глутаминовой кислоты;
- проламины - группа растительных белков, содержащаяся в клейковине злаковых растений. Они растворимы только в 60-80%-ном водном растворе этилового спирта. Проламины имеют характерный аминокислотный состав: в них много (20-50%) глутаминовой кислоты и пролина (10-15%), в связи с чем они и получили свое название. Их молекулярная масса более 100000 Да;
- глютелины - растительные белки нерастворимые в воде, растворах солей и этаноле, но растворимы в разбавленных (0,1Н) растворах щелочей и кислот. По аминокислотному составу и молекулярной массе сходны с проламинами, но аргинина содержат больше, а пролина меньше.
Способы исследования аминокислотного состава
Под действием ферментов пищеварительных соков белки расщепляются на аминокислоты. Были сделаны два важных вывода: 1) в состав белков входят аминокислоты; 2) методами гидролиза может быть изучен химический, в частности амнокислотный, состав белков.
Для изучения аминокислотного состава белков пользуются сочетанием кислотного (НСl), щелочного [Ва(ОН)2] и, реже, ферментативного гидролиза или одним из них. Установлено, что при гидролизе чистого белка, не содержащего примесей, освобождаются 20 различных α-аминокислот. Все другие открытые в тканях животных, растений и микроорганизмов аминокислоты (более 300) существуют в природе в свободном состоянии либо в виде коротких пептидов или комплексов с другими органическими веществами.
Первый этап в определении первичной структуры белков заключается в качественной и количественной оценке аминокислотного состава данного индивидуального белка. Необходимо помнить, что для исследования нужно иметь определённое количество чистого белка, без примесей других белков или пептидов.
Кислотный гидролиз белка
Для определения аминокислотного состава необходимо провести разрушение всех пептидных связей в белке. Анализируемый белок гидролизуют в 6 мол/л НС1 при температуре около 110 °С в течение 24 ч. В результате такой обработки разрушаются пептидные связи в белке, а в гидролизате присутствуют только свободные аминокислоты. Кроме того, глутамин и аспарагин гидролизуются до глутаминовой и аспарагиновой кислот (т.е. разрывается амидная связь в радикале и от них отщепляется аминогруппа).
Разделение аминокислот с помощью ионообменной хроматографии
Смесь аминокислот, полученных кислотным гидролизом белков, разделяют в колонке с катионообменной смолой. Такая синтетическая смола содержит прочно связанные с ней отрицательно заряженные группы (например, остатки сульфоновой кислоты -SO3-), к которым присоединены ионы Na+ (рис. 1-4).
В катионообменник вносят смесь аминокислот в кислой среде (рН 3,0), где аминокислоты в основном представляют катионы, т.е. несут положительный заряд. Положительно заряженные аминокислоты присоединяются к отрицательно заряженным частицам смолы. Чем больше суммарный заряд аминокислоты, тем прочнее её связь со смолой. Так, аминокислоты лизин, аргинин и гистидин наиболее прочно связываются с катионообменником, а аспарагиновая и глутаминовая кислоты - наиболее слабо.
Высвобождение аминокислот из колонки осуществляют вымыванием (элюированием) их буферным раствором с увеличивающейся ионной силой (т.е. с увеличением концентрации NaCl) и рН. При увеличении рН аминокислоты теряют протон, в результате уменьшается их положительный заряд, а следовательно и прочность связи с отрицательно заряженными частицами смолы.
Каждая аминокислота выходит из колонки при определённом значении рН и ионной силы. Собирая с нижнего конца колонки раствор (элюат) в виде небольших порций, можно получить фракции, содержащие отдельные аминокислоты.
(подробнее «гидролиз» см вопрос №10)
8) Химические связи в структуре белка.


9) Понятие об иерархии и структурной организации белков. (см. вопрос №12)
10) Гидролиз белка. Химизм реакции (ступенчатость, катализаторы, реагенты, условия протекания реакции) – полное описание гидролиза.
11) Химические превращения белков.
Денатурация и ренатурация
При нагревании растворов белков до 60-80% или при действии реагентов, разрушающих нековалентные связи в белках, происходит разрушение третичной (четвертичной) и вторичной структуры белковой молекулы, она принимает в большей или меньшей степени форму беспорядочного случайного клубка. Этот процесс называют денатурацией. В качестве денатурирующих реагентов могут быть кислоты, щелочи, спирты, фенолы, мочевина, гуанидинхлорид и др. Сущность их действия в том, что они образуют водородные связи с =NH и =СО - группами пептидного остова и с кислотными группами радикалов аминокислот, подменяя собственные внутримолекулярные водородные связи в белке вследствие чего вторичная и третичная структуры изменяются. При денатурации падает растворимость белка, он "свертывается" (например, при варке куриного яйца), утрачивается биологическая активность белка. На этом основано, например, применение водного раствора карболовой кислоты (фенола) в качестве антисептика. В определенных условиях при медленном охлаждении раствора денатурированного белка происходит ренатурация - восстановление исходной (нативной) конформации. Это подтверждает тот факт, что характер укладки пептидной цепи определяется первичной структурой.
Процесс денатурации отдельной белковой молекулы, приводящий к распаду её «жёсткой» трёхмерной структуры, иногда называют плавлением молекулы. Практически любое заметное изменение внешних условий, например, нагревание или существенное изменение pH приводит к последовательному нарушению четвертичной, третичной и вторичной структур белка. Обычно денатурация вызывается повышением температуры, действием сильных кислот и щелочей, солей тяжелых металлов, некоторых растворителей (спирт), радиации и др.
Денатурация часто приводит к тому, что в коллоидном растворе белковых молекул происходит процесс агрегации частиц белка в более крупные. Визуально это выглядит, например, как образование «белка» при жарке яиц.
Ренатурация — процесс, обратный денатурации, при котором белки возвращают свою природную структуру. Нужно отметить, что не все белки способны ренатурировать; у большинства белков денатурация необратима. Если при денатурации белка физико-химические изменения связаны с переходом полипептидной цепи из плотно упакованного (упорядоченного) состояния в беспорядочное, то при ренатурации проявляется способность белков к самоорганизации, путь которой предопределён последовательностью аминокислот в полипептидной цепи, то есть её первичной структурой, детерминированной наследственной информацией. В живых клетках данная информация, вероятно, является решающей для преобразования неупорядоченной полипептидной цепи во время или после её биосинтеза на рибосоме в структуру нативной молекулы белка. При нагревании двухцепочечных молекул ДНК до температуры около 100°C водородные связи между основаниями разрываются, и комплементарные цепи расходятся — ДНК денатурирует. Однако при медленном охлаждении комплементарные цепи могут вновь соединяться в регулярную двойную спираль. Эта способность ДНК к ренатурации используется для получения искусственных гибридных молекул ДНК.
Природные белковые тела наделены определенной, строго заданной пространственной конфигурацией и обладают рядом характерных физико-химических и биологических свойств при физиологических значениях температуры и рН среды. Под влиянием различных физических и химических факторов белки подвергаются свертыванию и выпадают в осадок, теряя нативные свойства. Таким образом, под денатурацией следует понимать нарушение общего плана уникальной структуры нативной молекулы белка, преимущественно ее третичной структуры, приводящее к потере характерных для нее свойств (растворимость, электрофоретическая подвижность, биологическая активность и т.д.). Большинство белков денатурирует при нагревании их растворов выше 50–60°С.
Внешние проявления денатурации сводятся к потере растворимости, особенно в изоэлектрической точке, повышению вязкости белковых растворов, увеличению количества свободных функциональных SH-групп и изменению характера рассеивания рентгеновских лучей. Наиболее характерным признаком денатурации является резкое снижение или полная потеря белком его биологической активности (каталитической, антигенной или гормональной). При денатурации белка, вызванной 8М мочевиной или другим агентом, разрушаются в основном нековалентные связи (в частности, гидрофобные взаимодействия и водородные связи). Дисульфидные связи в присутствии восстанавливающего агента меркаптоэтанола разрываются, в то время как пептидные связи самого остова полипептидной цепи не затрагиваются. В этих условиях развертываются глобулы нативных белковых молекул и образуются случайные и беспорядочные структуры (рис.)
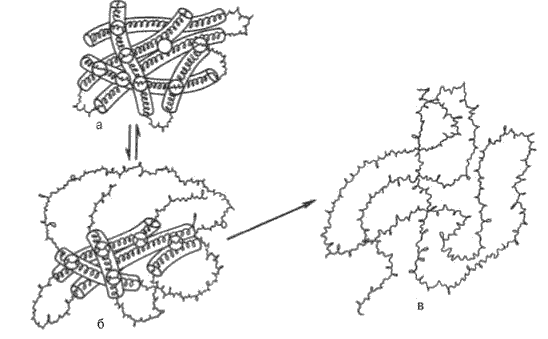
Денатурация белковой молекулы (схема).
а - исходное состояние; б - начинающееся обратимое нарушение молекулярной структуры; в - необратимое развертывание полипептидной цепи.
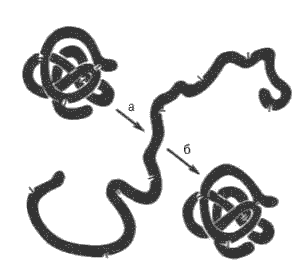
Денатурация и ренатурация рибонуклеазы (по Анфинсену).
а - развертывание (мочевина + меркаптоэтанол); б - повторное свертывание.

1. Гидролиз белков: H+
[− NH2─CH─ CO─NH─CH─CO − ]n +2nH2O → n NH2 − CH − COOH + n NH2 ─ CH ─ COOH
│ │ │ │
R1 R2 R1 R2
Аминокислота 1 аминокислота 2
2. Осаждение белков:
а) обратимое
Белок в растворе ↔ осадок белка. Происходит под действием растворов солей Na+, K+
б) необратимое (денатурация)
При денатурации под действием внешних факторов (температура; механическое воздействие – давление, растирание, встряхивание, ультразвук; действия химических агентов – кислот, щелочей и др.) происходит изменение вторичной, третичной и четвертичной структур белковой макромолекулы, т.е её нативной пространственной структуры. Первичная структура, а, следовательно, и химический состав белка не меняются.
При денатурации изменяются физические свойства белков: снижается растворимость, теряется биологическая активность. В тоже время увеличивается активность некоторых химических групп, облегчается воздействие на белки протеолитических ферментов, а, следовательно, он легче гидролизуется.
Например, альбумин — яичный белок — при температуре 60—70° осаждается из раствора (свертывается), теряя способность растворяться в воде.
Схема процесса денатурации белка (разрушение третичной и вторичной структур белковых молекул)
3. Горение белков
Белки горят с образованием азота, углекислого газа, воды , а также некоторых других веществ. Горение сопровождается характерным запахом жженых перьев
4. Цветные (качественные) реакции на белки:
а) ксантопротеиновая реакция (на остатки аминокислот, содержащих бензольные кольца):
Белок + HNO3 (конц.) → желтое окрашивание
б) биуретовая реакция (на пептидные связи):
Белок + CuSO4 (насыщ) + NaOH (конц) → ярко-фиолетовое окрашивание
в) цистеиновая реакция (на остатки аминокислот, содержащих серу):
Белок + NaOH + Pb(CH3COO)2 → Черное окрашивание
Белки являются основой всего живого на Земле и выполняют в организмах многообразные функции.
Высаливание белков
Высаливанием называется процесс выделения белков из водных растворов нейтральными растворами концентрированных солей щелочных и щелочноземельных металлов. При добавлении больших концентраций солей к раствору белка происходит дегидратация белковых частиц и снятие заряда, при этом белки выпадают в осадок. Степень выпадения белков в осадок зависит от ионной силы раствора осадителя, размера частиц белковой молекулы, величины ее заряда, гидрофильности. Разные белки осаждаются при различных концентрациях солей. Поэтому в осадках, полученных путем постепенного повышения концентрации солей, отдельные белки находятся в различных фракциях. Высаливание белков является обратимым процессом, и после удаления соли белок вновь приобретает природные свойства. Поэтому высаливанием пользуются в клинической практике при разделении белков сыворотки крови, а также при изолировании, очистке различных белков.
Добавляемые анионы и катионы разрушают гидратную белковую оболочку белков, являющуюся одним из факторов устойчивости белковых растворов. Чаще всего применяются растворы сульфатов Na и аммония. Многие белки отличаются по размеру гидратной оболочки и величине заряда. Для каждого белка есть своя зона высаливания. После удаления высаливающего агента белок сохраняет свою биологическую активность и физико-химические свойства. В клинической практике применяется метод высаливания для разделения глобулинов ( при добавлении 50% раствора сульфата аммония (NH4)2SO4 выпадает осадок) и альбуминов ( при добавлении 100% раствора сульфата аммония (NH4)2SO4 выпадает осадок).
На величину высаливания оказывают влияние:
1) природа и концентрация соли;
2) рН-среды;
3) температура.
Главную роль при этом играют валентности ионов.
12) Особенности организации первичной, вторичной, третичной структуры белка.
В настоящее время экспериментально доказано существование четырёх уровней структурной организации белковой молекулы: первичной, вторичной, третичной и четвертичной структуры.
